Clear Sky Science · es
Una estrategia de radiomarcado en un solo paso para PET, SPECT y radionúclidos terapéuticos usando nanopartículas como quelante universal
Por qué importan las partículas radiactivas diminutas
La atención del cáncer moderna depende cada vez más de ver y tratar tumores con fármacos radiactivos que los iluminan en las exploraciones y, en algunos casos, los queman desde dentro. Sin embargo, fabricar cada nuevo medicamento radiactivo es lento y delicado, porque la mayoría de los diseños deben construirse a medida alrededor de un metal radiactivo específico. Este estudio explora un enfoque muy distinto: usar un único tipo de nanopartícula a base de hierro como un "enchufe universal" que puede alojar muchos isótopos médicos diferentes para imagen y terapia, acelerando potencialmente la creación y el ajuste fino de esos fármacos.
De muchas llaves a una sola cerradura
Los fármacos radiactivos actuales suelen depender de garras químicas llamadas quelantes que sujetan átomos metálicos y los unen a anticuerpos u otras moléculas dirigidas. Cada metal radiactivo tiende a necesitar su propio quelante y su propia receta: condiciones como temperatura, acidez y tiempo de reacción cambian. Para algunos metales de interés médico, especialmente los usados en terapias con partículas alfa potentes, aún no existe un quelante ideal. Los autores sostienen que este enfoque metal por metal se ha convertido en un cuello de botella: la lista de isótopos útiles sigue creciendo, pero la química para manejarlos con seguridad no puede mantenerse al ritmo.
Nanopartículas como enchufe universal
Para abordar esto, los investigadores recurrieron a nanopartículas muy pequeñas de óxido de hierro, un material ya explorado como contraste para MRI. Diseñaron partículas con un núcleo de óxido de hierro de aproximadamente tres nanómetros de ancho, recubiertas con citrato para mantenerlas estables en el torrente sanguíneo. Durante un único paso de síntesis asistida por microondas de 10 minutos, incorporaron en el núcleo uno de diez metales radiactivos diferentes empleados comúnmente en PET, SPECT o radioterapia interna. Este proceso en una sola mezcla produjo partículas de tamaño consistente con altos rendimientos y, lo que es crucial, excelente estabilidad en suero humano—incluso para isótopos terapéuticos desafiantes como el radio‑223 y el actinio‑225, cuyos productos de decaimiento suelen escapar de los quelantes tradicionales.
Imágenes de coágulos y tumores cerebrales
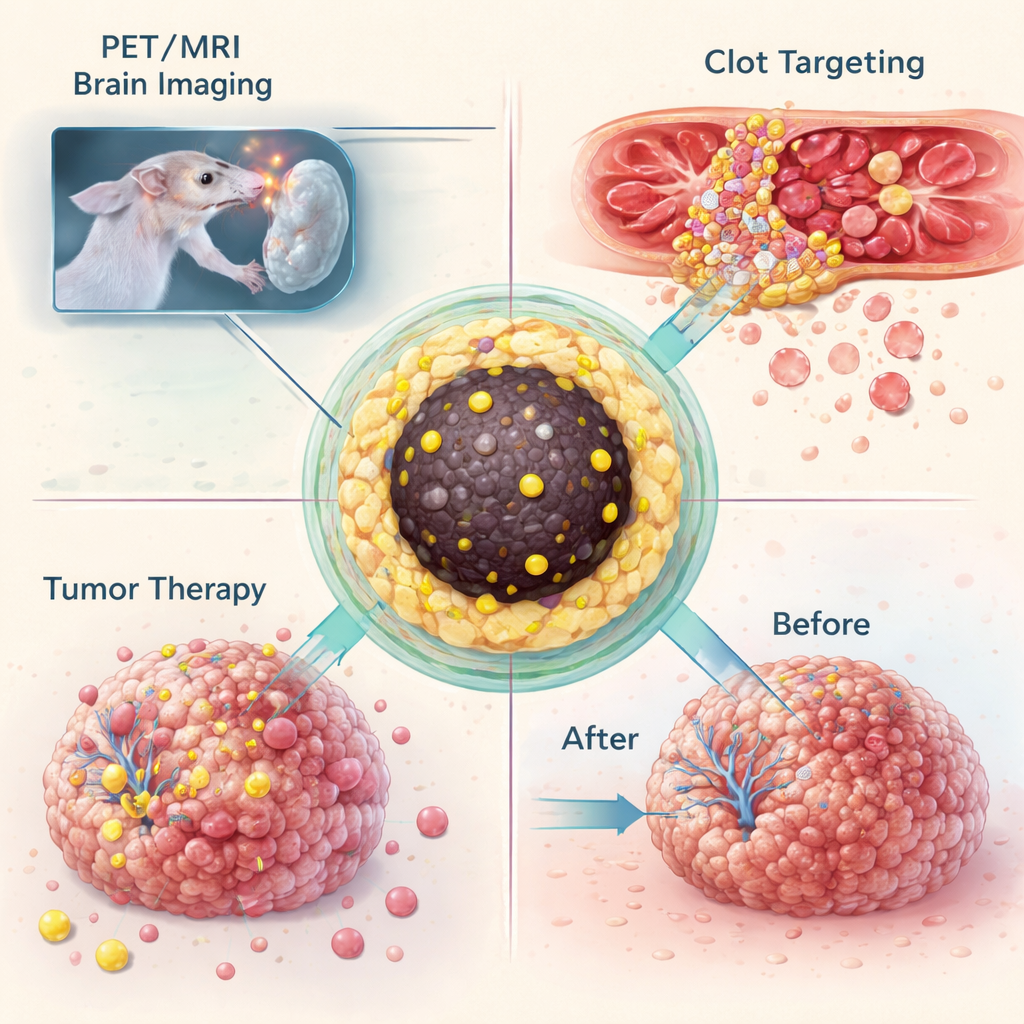
Habiendo demostrado que podían atrapar muchos isótopos diferentes en el mismo diseño de nanopartícula, el equipo probó qué podían hacer estos "nanotrazadores" en animales vivos. En un modelo murino de glioblastoma, un tumor cerebral letal, se inyectaron partículas marcadas con galio‑68 en el torrente sanguíneo y se visualizaron con PET combinado con MRI. Las partículas se acumularon en tumores lo bastante grandes como para alterar la barrera hematoencefálica, permitiendo que la misma formulación ofreciera tanto un contraste brillante en MRI como una señal PET sensible. En un experimento separado, las partículas se modificaron químicamente para que pudieran unirse, mediante una reacción de click altamente selectiva, a un anticuerpo que se dirige a plaquetas activadas dentro de coágulos sanguíneos. En ratones con lesión en la arteria carótida, esta estrategia de "preobjetivación" en dos pasos produjo señales PET claras en el sitio del coágulo, mientras que los animales de control no mostraron tal punto caliente.
Del diagnóstico al tratamiento y una eliminación más segura
La misma plataforma también se utilizó para administrar tratamiento. Cuando nanopartículas cargadas con lutecio‑177 se inyectaron directamente en tumores de glioblastoma en ratones, las partículas permanecieron en gran medida confinadas a la masa tumoral durante al menos dos semanas. Durante ese tiempo, los tumores no tratados crecieron varias veces su tamaño original, mientras que los tumores tratados dejaron de crecer, lo que sugiere que la dosis de radiación localizada fue suficiente para detener la progresión. Reconociendo que tratamientos repetidos podrían sobrecargar con hierro el hígado y el bazo, el equipo ajustó las condiciones de síntesis para fabricar partículas aún más pequeñas—alrededor de cuatro a cinco nanómetros—lo bastante pequeñas para ser filtradas por los riñones. Estas partículas reducidas seguían reteniendo su carga radiactiva de forma segura pero se excretaban rápidamente en la vejiga, reduciendo la acumulación a largo plazo en órganos principales.
Qué podría significar esto para la atención del cáncer en el futuro
Para los no especialistas, el mensaje clave es que los investigadores han construido una plataforma de nanopartículas única y flexible que puede emparejarse con muchos metales radiactivos diferentes sin tener que reinventar la química cada vez. En modelos animales, la misma partícula básica puede ayudar a detectar tumores cerebrales, resaltar coágulos sanguíneos, administrar radiación directamente dentro de los tumores e incluso ajustarse para salir del cuerpo por los riñones. Aunque se necesita más trabajo antes de que este enfoque llegue a pacientes, ofrece una vía prometedora para diseñar familias de agentes diagnósticos y terapéuticos que compartan el mismo comportamiento en el organismo, diferenciándose solo por el tipo de radiación que portan. Esa consistencia podría simplificar el desarrollo, mejorar las pruebas de seguridad y, en última instancia, hacer que las herramientas avanzadas de medicina nuclear estén más ampliamente disponibles.
Cita: Herraiz, A., Rodríguez-San-Pedro, A., Casquero-Veiga, M. et al. A single-step radiolabeling strategy for PET, SPECT, and therapeutic radionuclides using nanoparticles as a universal chelator. npj Imaging 4, 8 (2026). https://doi.org/10.1038/s44303-026-00142-1
Palabras clave: radioteranósticos, nanopartículas, imágenes PET, glioblastoma, radioterapia dirigida