Clear Sky Science · es
Sinucleinopatía acelerada y localizada en un modelo híbrido de ratón: implicaciones para estudios con tomografía por emisión de positrones
Por qué importa esta investigación
La enfermedad de Parkinson es más conocida por los temblores y los problemas de movimiento, pero en lo más profundo del cerebro comienza con pequeños cambios que son difíciles de detectar. Los médicos necesitan con urgencia métodos para identificar esos cambios de forma temprana y para evaluar nuevos fármacos con rapidez. Este estudio describe un modelo de ratón refinado que reproduce características clave del daño cerebral parecido al Parkinson en apenas unas semanas y en una región cerebral muy específica, diseñado para su uso con técnicas avanzadas de imagen cerebral llamadas PET. 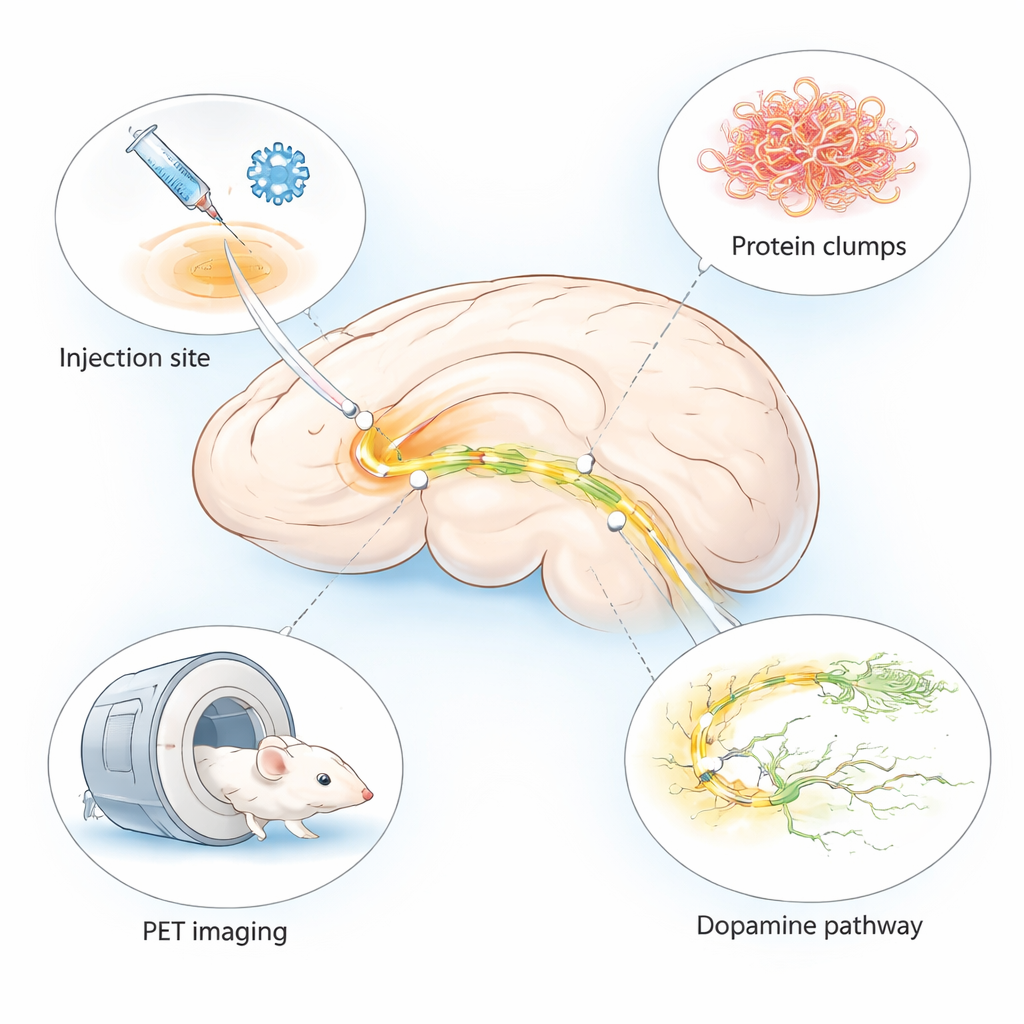
Construyendo un modelo de enfermedad más rápido y focalizado
Muchos de los modelos animales existentes de la enfermedad de Parkinson tardan meses en desarrollar síntomas o no muestran toda la gama de cambios cerebrales observados en los pacientes. Los autores combinaron dos enfoques ya establecidos en un único modelo “híbrido”. Inyectaron un virus inofensivo que induce a las células cerebrales a producir alfa‑sinucleína humana —una proteína que se agrupa en el Parkinson— junto con fibrillas preformadas, que actúan como semillas que desencadenan más agregación. Ambos se administraron en una pequeña región relacionada con el movimiento llamada sustancia negra, en un solo lado del cerebro del ratón. Este diseño produce cambios locales pero intensos parecidos a la enfermedad en el lado inyectado, mientras que el lado opuesto permanece relativamente sano para su comparación.
Rastreando agregados proteicos y neuronas moribundas
Apenas dos semanas después de la inyección, los ratones mostraron altos niveles de alfa‑sinucleína humana y de su forma anormal fosforilada en la zona cerebral objetivo. Al microscopio, los investigadores observaron estructuras que recordaban a los cuerpos de Lewy y las neuritas de Lewy, que son signos distintivos de la enfermedad de Parkinson. En las semanas siguientes, estos depósitos anormales se incrementaron. Al mismo tiempo, las neuronas que producen el mensajero químico dopamina —crucial para el movimiento suave— comenzaron a desaparecer. Los marcadores de estas células cayeron hasta aproximadamente el 60 por ciento del nivel observado en el lado intacto a la semana cinco, confirmando una pérdida progresiva y clara del sistema dopaminérgico.
Inflamación, sinapsis en declive y centrales energéticas agotadas
Las células inmunitarias del cerebro, llamadas microglía, también pasaron a un estado altamente activo e inflamatorio alrededor de la región dañada. Las tinciones para varias proteínas relacionadas con la inflamación fueron mucho más intensas cerca de los depósitos de alfa‑sinucleína que en el lado opuesto del cerebro. Más adelante en el proceso, el equipo detectó una pérdida de sinapsis —los diminutos puntos de contacto donde las neuronas se comunican— y señales de que las mitocondrias, las fábricas de energía celular, no funcionaban correctamente. En conjunto, estos hallazgos muestran que el modelo no solo genera agregados proteicos; también captura la reacción en cadena de inflamación, fallos en las conexiones y problemas energéticos que contribuyen a la muerte neuronal en la enfermedad de Parkinson. 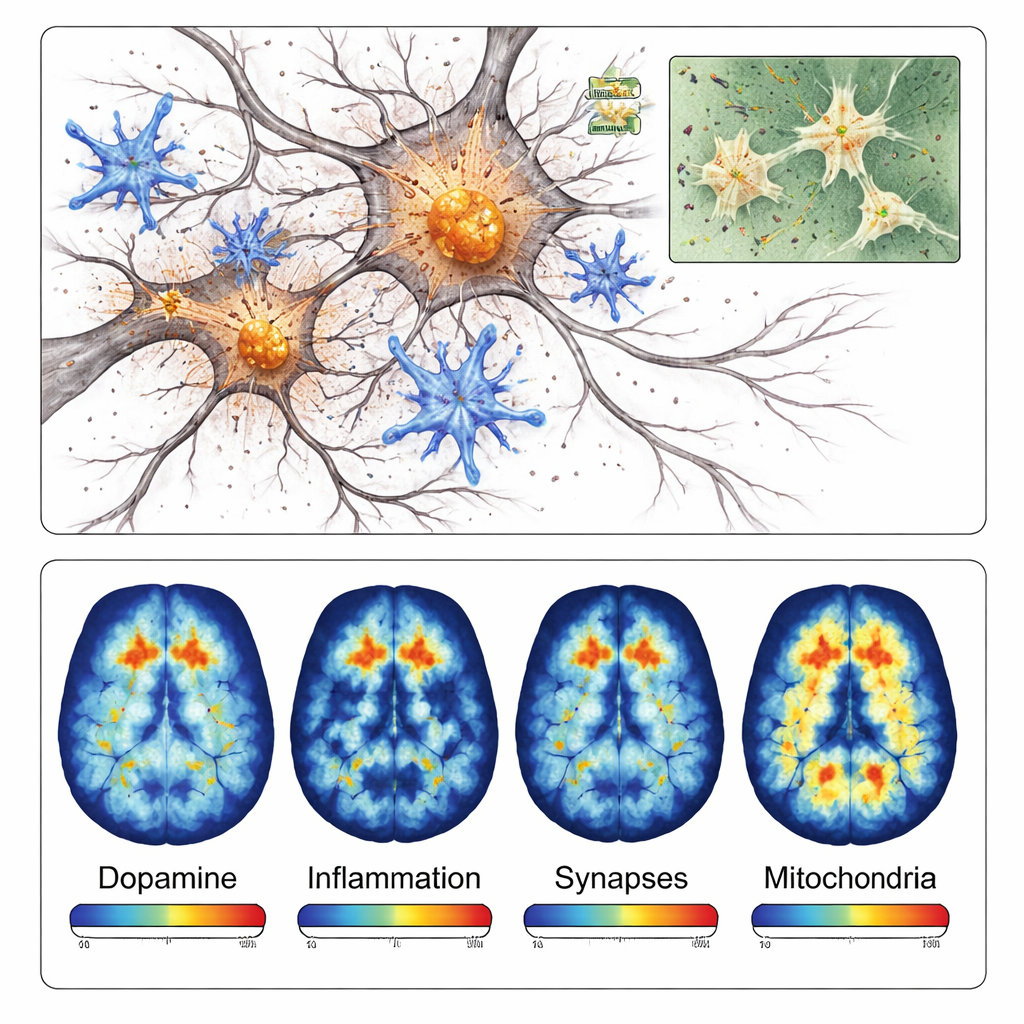
Poniendo en marcha los escáneres PET
Debido a que este modelo es localizado y se desarrolla rápidamente, es especialmente adecuado para la tomografía por emisión de positrones (PET), una técnica de imagen que puede medir moléculas concretas en cerebros vivos. Los investigadores probaron cuatro trazadores PET distintos que se unen a terminales nerviosas dopaminérgicas, microglía inflamatoria, proteínas sinápticas y enzimas mitocondriales. En cada caso, las exploraciones PET mostraron señales más bajas o más altas en el lado inyectado en correspondencia con los hallazgos microscópicos. Por ejemplo, el trazador dirigido a las vías dopaminérgicas mostró aproximadamente un 40 por ciento menos señal en el lado dañado, mientras que el trazador de la inflamación mostró más de un 40 por ciento de aumento de señal en la región afectada.
Qué supone esto para los pacientes y futuros tratamientos
Este nuevo modelo de ratón reúne, en un marco temporal breve, muchos de los cambios clave que ocurren durante años en los cerebros de las personas con enfermedad de Parkinson. Debido a que el daño está confinado a un área pequeña y bien definida y puede seguirse con exploraciones PET, los investigadores pueden evaluar de forma más eficiente nuevos trazadores de imagen y posibles terapias. Si bien ningún ratón puede reproducir completamente la condición humana, este enfoque ofrece una herramienta potente y práctica para cerrar la brecha entre el trabajo básico de laboratorio y los estudios en humanos, ayudando en última instancia a refinar el diagnóstico y a acelerar la búsqueda de mejores tratamientos.
Cita: Xia, C.A., Tsai, HM., Diaz Garcia, S. et al. Accelerated and localized synucleinopathy in a hybrid mouse model: implications for positron emission tomography studies. npj Imaging 4, 7 (2026). https://doi.org/10.1038/s44303-026-00138-x
Palabras clave: Enfermedad de Parkinson, alfa-sinucleína, sinucleinopatía, imagen PET, modelo de ratón