Clear Sky Science · es
Modelos de ecuaciones diferenciales ordinarias de la dinámica de replicación de SARS-CoV-2 y la eficacia de los fármacos antivirales
Por qué importan los números para un virus nuevo
Cuando apareció la COVID-19, los médicos podían observar lo que el virus hacía a los pacientes, pero no podían predecir fácilmente quién se iba a poner muy grave ni cuándo debía administrarse un fármaco para lograr el mejor efecto. Este artículo de revisión examina cómo los investigadores convirtieron mediciones virales de pacientes, animales y cultivos celulares en “películas” matemáticas de la infección dentro del cuerpo. Estos modelos usan ecuaciones para seguir cómo crece el virus, cómo reaccionan nuestras células y el sistema inmune, y cómo los antivirales y las vacunas pueden inclinar la balanza a nuestro favor.
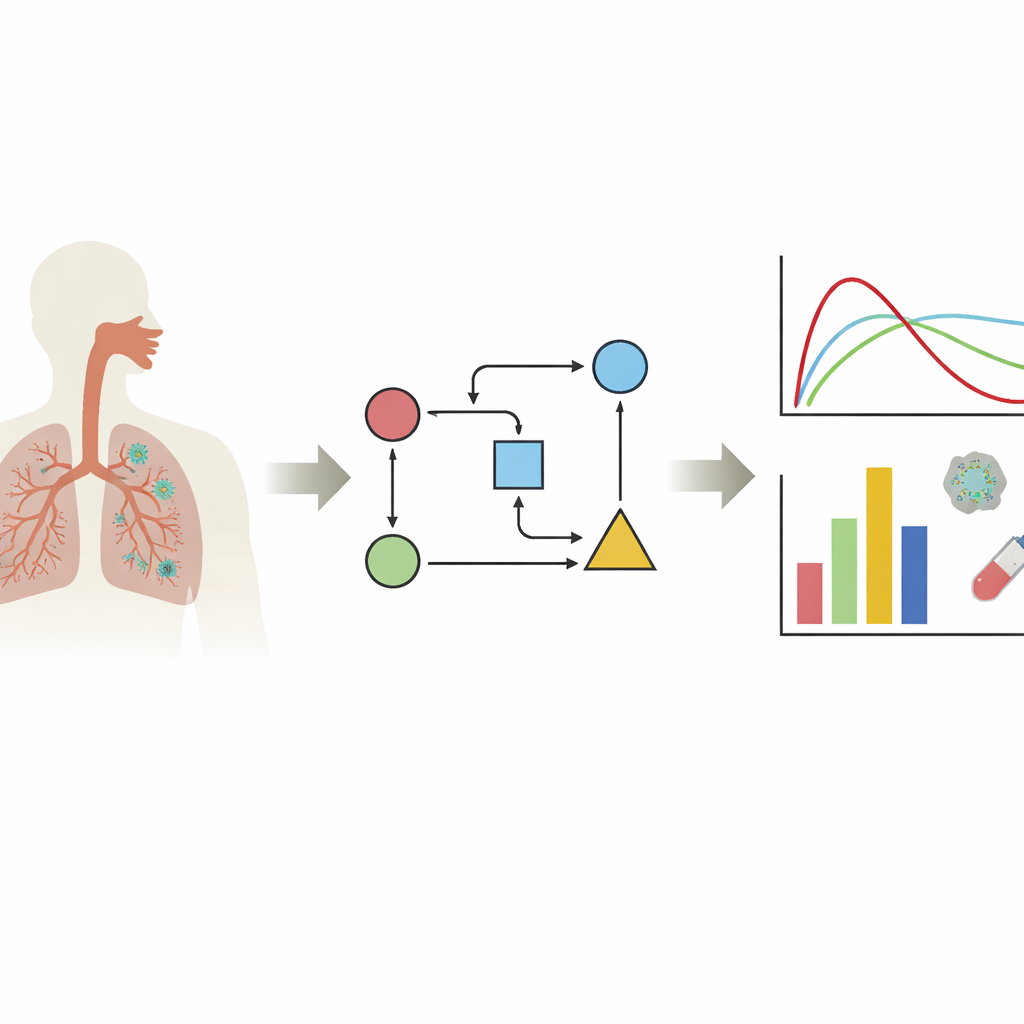
Siguiendo el virus dentro del cuerpo
Los autores se centran en una familia de modelos llamados modelos limitados por células diana. En términos sencillos, estos modelos siguen a tres protagonistas principales: células sanas susceptibles de infección, células ya infectadas y partículas virales libres. Al introducir datos reales de niveles virales en estas ecuaciones, los investigadores pueden estimar características ocultas de la infección: con qué rapidez el virus infecta células, cuánto tiempo una célula infectada produce virus y qué velocidad se elimina el virus. La revisión muestra que la mayor parte del trabajo se centra en los tejidos que importan más para la COVID-19—la nariz y las vías respiratorias superiores e inferiores—mientras que solo unos pocos modelos examinan otros órganos. Un mensaje clave es que el comportamiento viral puede parecer muy distinto según el tejido, la variante viral y la línea celular de laboratorio estudiada, por lo que no existe una curva de infección “típica” única.
Lo que aprendemos sobre el sistema inmune
Muchos modelos añaden capas que representan las defensas tempranas del sistema inmune y su respuesta más lenta y dirigida. Los estudios centrados en la primera línea de defensa sugieren que una actividad rápida y bien sincronizada de las células innatas y las moléculas de señalización puede atenuar la infección, pero rara vez la elimina por sí sola. Otros trabajos subrayan el papel crucial de las células T y los anticuerpos para finalmente controlar el virus. Los modelos también capturan un lado oscuro: si la respuesta inmune dirigida llega tarde o está mal orientada, las mismas herramientas que deberían protegernos pueden alimentar “tormentas de citoquinas” dañinas, en las que señales inflamatorias en exceso perjudican tejido sano. En estas simulaciones, el delicado equilibrio entre la actividad inmune útil y la perjudicial a menudo decide si la enfermedad permanece leve o se vuelve potencialmente mortal.
Cuándo funcionan mejor los fármacos y las vacunas
Porque las ecuaciones pueden ejecutarse una y otra vez bajo distintas hipótesis, son herramientas potentes para probar estrategias de tratamiento en el ordenador antes de ensayarlas en personas. En muchos estudios, los modelos coinciden en un punto central: los antivirales funcionan mejor cuando se administran muy temprano, antes de que el virus alcance su pico e infecte la mayor parte de las células disponibles. Los tratamientos que bloquean la copia del material genético viral resultan especialmente prometedores, en particular cuando se combinan con otros fármacos que actúan por mecanismos distintos. El tratamiento tardío, en contraste, tiende a tener poco impacto en las simulaciones a menos que se usen juntos varios fármacos potentes. La vacunación se predice de forma consistente que supera al uso de fármacos aislados, principalmente porque prepara al sistema inmune para reconocer el virus rápidamente y acortar el tiempo de niveles virales elevados.
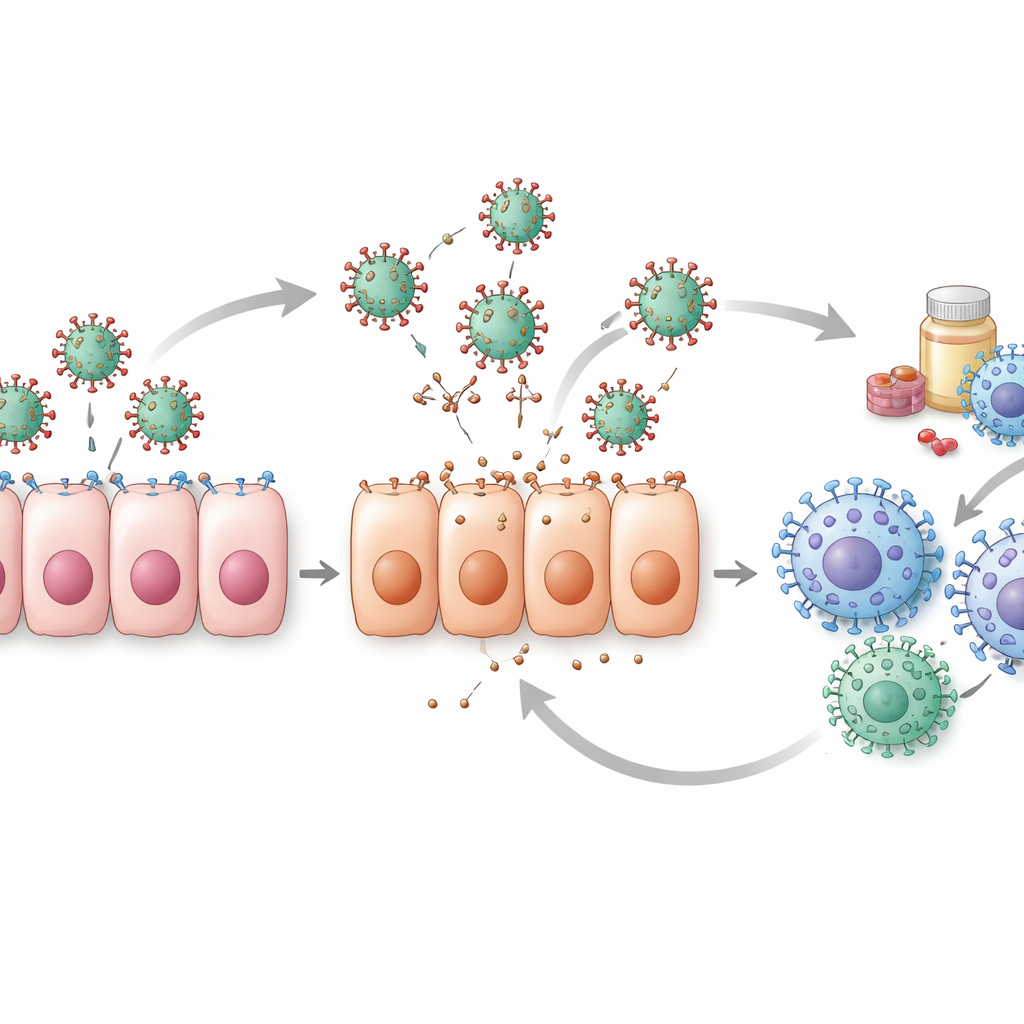
Desafíos ocultos en los datos
La revisión también arroja luz sobre las debilidades que hay detrás de los números. La mayoría de los conjuntos de datos clínicos comienzan solo después de que las personas ya se sienten enfermas, lo que significa que los modelos a menudo pierden los primeros días cruciales de la infección cuando los niveles virales están ascendiendo con más rapidez. Sin esas mediciones tempranas, distintas combinaciones de parámetros del modelo pueden explicar los mismos datos, lo que dificulta estar seguro de cuál es la explicación correcta. Solo una minoría de estudios realiza comprobaciones rigurosas para ver si sus estimaciones de parámetros son realmente únicas y fiables. Los estudios en animales y los experimentos en cultivos celulares ayudan a llenar algunos vacíos, especialmente en los primeros puntos temporales, pero las diferencias entre especies y sistemas de laboratorio limitan la aplicabilidad directa de esos resultados a humanos.
Qué significa esto de cara al futuro
Para un público no especializado, la conclusión es que los modelos matemáticos bien construidos han mejorado notablemente nuestra comprensión de cómo se comporta el SARS-CoV-2 dentro del cuerpo y cómo el momento, las combinaciones de fármacos y la vacunación previa moldean los resultados. Los modelos coinciden en términos generales en que una intervención temprana y sólida—especialmente mediante la vacunación y antivirales administrados a tiempo—ofrece al sistema inmune la mejor oportunidad para ganar, mientras que las respuestas retrasadas, ya sean del propio organismo o del tratamiento, se asocian con enfermedad más grave. Al mismo tiempo, los autores subrayan que estas herramientas solo son tan buenas como los datos que se introducen en ellas. Para prepararse ante variantes futuras o nuevos virus, piden muestreos clínicos más ricos y más tempranos y mediciones inmunes más amplias, de modo que los “números detrás de la infección” puedan orientar decisiones más rápidas y precisas en brotes reales.
Cita: Kapischke, T., Herrmann, S.T., Bertzbach, L.D. et al. Ordinary differential equation models of SARS-CoV-2 replication dynamics and antiviral drug efficacies. npj Viruses 4, 17 (2026). https://doi.org/10.1038/s44298-026-00183-8
Palabras clave: dinámica viral de SARS-CoV-2, modelado intra-huésped, tiempos de la terapia antiviral, respuesta inmune, vacunación contra la COVID-19