Clear Sky Science · es
Roles divergentes de las chaperonas Hsp70 en la secreción de proteínas de ortoflavivirus y la formación de viriones
Por qué importan los pequeños ayudantes de choque térmico para los virus que infectan el cerebro
Los virus transmitidos por garrapatas y mosquitos, como el virus de la encefalitis transmitida por garrapatas y el virus del Nilo Occidental, pueden invadir el cerebro y causar enfermedades graves, pero aún no existen medicamentos específicos para detenerlos. Este estudio examina cómo estos virus secuestran un conjunto de «ayudantes» proteicos de nuestro propio organismo, llamados chaperonas Hsp70, para ensamblar y liberar nuevas partículas virales. Dado que las proteínas Hsp70 ya se están explorando como dianas farmacológicas en cáncer, comprender esta relación podría abrir nuevas vías para tratar infecciones virales peligrosas sin atacar directamente a los virus.
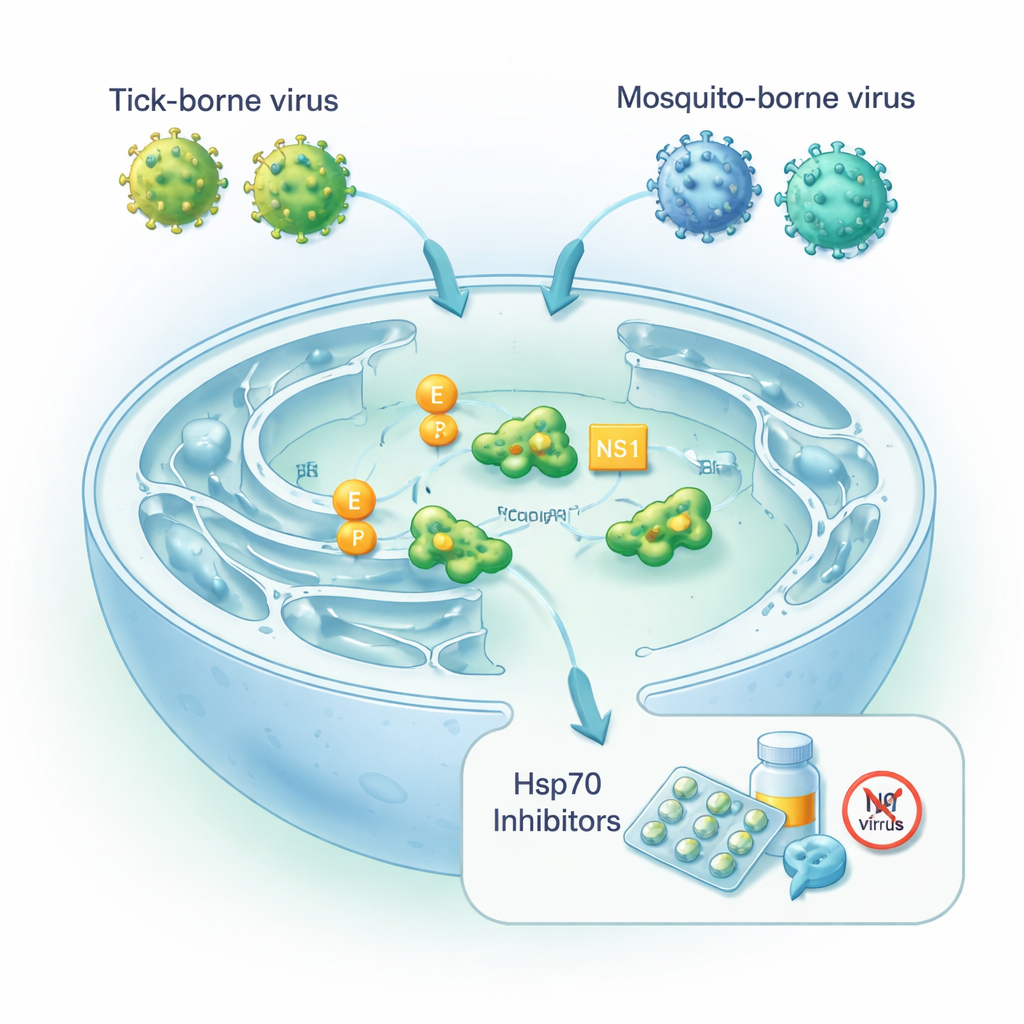
Virus que dependen de la maquinaria de plegamiento de la célula
Los ortoflavivirus son virus pequeños de ARN cuyo material genético codifica una poliproteína larga que debe ser cortada y plegada en varias piezas funcionales. Dos componentes virales clave son la proteína de envoltura E, que recubre la partícula viral y le permite entrar en células nuevas, y la proteína no estructural NS1, que ayuda al virus a copiar su genoma y puede ser secretada para manipular el sistema inmunitario. Todo esto ocurre en el retículo endoplásmico, la parte de la célula donde muchas proteínas se pliegan y se preparan para la exportación. Allí, la célula depende de las chaperonas Hsp70, incluida una forma residente llamada BiP, para evitar que las proteínas recién sintetizadas se plieguen mal bajo estrés. Los autores preguntaron hasta qué punto los ortoflavivirus neurotrópicos transmitidos por garrapatas y mosquitos dependen de estas chaperonas para ensamblar partículas infecciosas.
Apretones directos entre proteínas virales y Hsp70
Usando células diseñadas para sobreproducir proteínas virales específicas, así como células infectadas con virus auténticos, los investigadores precipitaron BiP o Hsp70 y analizaron qué socios virales venían asociados. Encontraron que BiP y Hsp70 formaban de manera consistente complejos con la proteína de envoltura E de varios ortoflavivirus, tanto transmitidos por garrapatas como por mosquitos. Esto sugiere que el plegamiento de E dentro del retículo endoplásmico está guiado por estas chaperonas. El panorama fue más selectivo para NS1: BiP y Hsp70 se unieron con fuerza a NS1 de los virus transmitidos por garrapatas, como el virus de la encefalitis transmitida por garrapatas y el virus Langat, pero no a NS1 de los virus transmitidos por mosquitos, como el virus del Nilo Occidental y Usutu. Estas diferencias probablemente reflejan variaciones en la glicosilación y en el plegamiento de NS1, lo que indica que no todos los virus afines emplean las mismas vías del huésped.
Bloquear las chaperonas reduce drásticamente la producción viral
Como las proteínas Hsp70 son dirigibles por fármacos, el equipo probó dos pequeñas moléculas que interfieren con diferentes partes de la maquinaria de chaperonas. YM‑1 se dirige al dominio de unión a nucleótidos, inmovilizando las Hsp70 en un estado inactivo, mientras que PES‑Cl bloquea el bolsillo de unión al sustrato que normalmente agarra a las proteínas clientes. A dosis que dejaron vivas a la mayoría de las células, YM‑1 redujo drásticamente la cantidad de virus infeccioso liberado por los cuatro ortoflavivirus probados y disminuyó la cantidad de proteína de envoltura encontrada en los fluidos de cultivo, lo que apunta a un bloqueo general en la formación o liberación de partículas. PES‑Cl, en cambio, tuvo poco efecto sobre los títulos infecciosos o los niveles de proteína de envoltura, aunque debilitó la interacción física entre Hsp70/BiP y la proteína de envoltura en ensayos de unión. Esto sugiere que interferir brevemente con el sitio de agarre no basta para paralizar el ensamblaje viral, mientras que detener el ciclo energético de la chaperona sí lo hace.
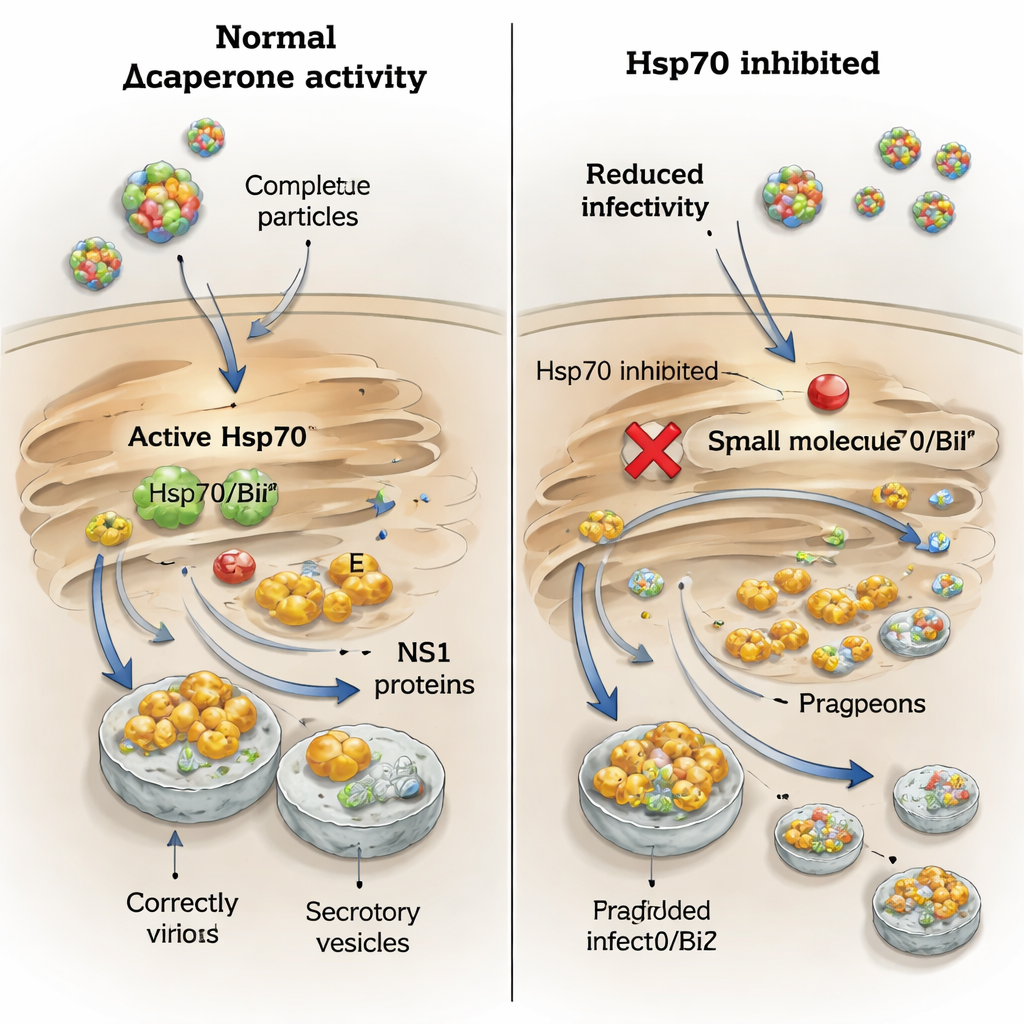
Una dependencia especial de los virus transmitidos por garrapatas de BiP para NS1
La historia para NS1 fue más matizada. Cuando las células infectadas se trataron con PES‑Cl, la secreción de NS1 de los virus de la encefalitis transmitida por garrapatas y Langat se redujo drásticamente, pero NS1 de los virus del Nilo Occidental y Usutu no se vio afectada. Esto refleja el hallazgo anterior de que solo las NS1 transmitidas por garrapatas se unen fuertemente a BiP y Hsp70. Para profundizar en el papel de BiP, los autores utilizaron ARN interferente pequeño para reducir específicamente los niveles de BiP. Esto disminuyó las cantidades de las proteínas de envoltura y NS1 tanto dentro de las células como en el fluido circundante para el virus de la encefalitis transmitida por garrapatas y para el virus del Nilo Occidental, si bien los títulos de virus infeccioso cayeron solo modestamente. Cuando las células con depleción de BiP se trataron con fármacos que bloquean la degradación de proteínas, los niveles de NS1 dentro de la célula se recuperaron pero su secreción no, lo que demuestra que BiP no solo protege a NS1 de la degradación sino que también la guía a lo largo de la vía secretora.
Qué significa esto para futuras estrategias antivirales
Para un público general, el mensaje principal es que estos virus que infectan el cerebro dependen fuertemente de los ayudantes celulares de plegamiento de proteínas para construir su cubierta externa y, en algunas especies, para secretar NS1 como arma extracelular. Un inhibidor amplio de chaperonas como YM‑1 puede, por tanto, reducir drásticamente la producción de partículas infecciosas de varios virus relacionados a la vez, aunque sus efectos potentes probablemente abarcan más de una chaperona y podrían dañar también células sanas. Enfoques más dirigidos, posiblemente centrados en cómo BiP y Hsp70 manejan clientes virales específicos como NS1, podrían algún día ayudar a diseñar tratamientos menos susceptibles a la resistencia viral y que preserven la mayoría del plegamiento proteico normal del huésped.
Cita: Blank, L., Lorenz, C. & Steffen, I. Divergent roles of Hsp70 chaperones in orthoflavivirus protein secretion and virion formation. npj Viruses 4, 8 (2026). https://doi.org/10.1038/s44298-026-00175-8
Palabras clave: orthoflavivirus, chaperona Hsp70, virus de la encefalitis transmitida por garrapatas, virus del Nilo Occidental, dianas farmacológicas antivirales