Clear Sky Science · es
La proteína G soluble del virus respiratorio sincitial promueve la diseminación viral mediante el cebado del NLRP3 mediado por TLR2 y la piroptosis
Por qué este virus pulmonar importa a todo el mundo
El virus respiratorio sincitial, o VRS, es más conocido como una amenaza invernal para los bebés, pero también provoca hospitalizaciones en muchas personas mayores y en quienes tienen el sistema inmunitario debilitado. Incluso con nuevas vacunas y anticuerpos protectores, el VRS sigue reinfectando a las personas una y otra vez y puede causar daño pulmonar grave. Este estudio examina una proteína viral poco conocida, una forma soluble de la proteína G del VRS, y revela cómo puede preparar silenciosamente a las células pulmonares para una inflamación explosiva y ayudar al virus a propagarse más eficazmente por las vías respiratorias.
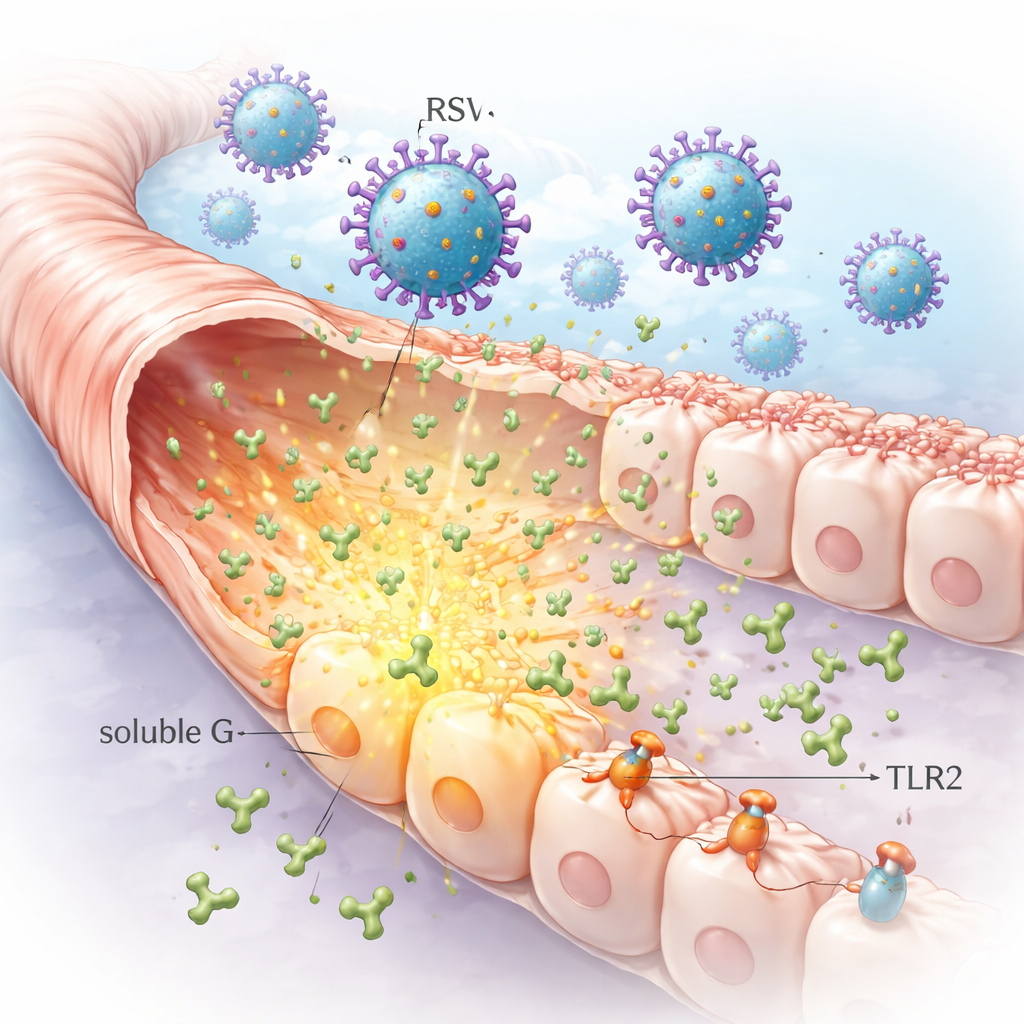
Una proteína viral secretada que viaja por delante de la infección
El VRS presenta en su superficie una proteína de adhesión llamada G que le ayuda a fijarse a las células de las vías respiratorias. De forma inusual, las células infectadas también liberan grandes cantidades de una versión libre de esta proteína, conocida como G soluble. Los investigadores mostraron que las células pulmonares infectadas en el laboratorio pueden desprender niveles muy altos de G soluble en su entorno. Dado que esta forma puede difundirse desde el sitio original de infección, puede alcanzar a células vecinas que aún no están infectadas, preparando el terreno para cambios más amplios en el revestimiento pulmonar de los que causaría solo el virus.
La G soluble como una llave de doble uso para las superficies celulares
Mediante la combinación de microscopía, ensayos bioquímicos de captura y tratamientos enzimáticos, el equipo trazó cómo la G soluble se adhiere a las células. Encontraron que puede unirse a cadenas azucaradas llamadas glicosaminoglucanos, así como a un receptor conocido del VRS llamado CX3CR1. De manera crucial, la G soluble también se une a una molécula sensora de patrones en células inmunitarias y de las vías respiratorias llamada TLR2. Un pequeño motivo en la proteína G, conocido como CX3C, resultó importante para la unión fuerte a CX3CR1 y para la reclutación robusta de TLR2. Esto significa que la G soluble puede primero ser capturada de forma laxa en la superficie celular y luego activar receptores más específicos que controlan cómo responden las células a las amenazas.
Cebado de las células pulmonares para un tipo inflamatorio de muerte celular
La activación de TLR2 por la G soluble resultó estar lejos de ser inofensiva. En células inmunitarias informadoras y líneas celulares pulmonares humanas, la G soluble activó la vía de señalización MyD88–NF-κB aguas abajo de TLR2, conduciendo a la liberación de mensajeros inflamatorios como IL-6 e IL-8. Al mismo tiempo, aumentó la producción de componentes de un “sistema de alarma” molecular llamado inflamasoma NLRP3 y de enzimas que generan moléculas reactivas como el óxido nítrico y radicales de oxígeno. Por sí solos, estos cambios causaron solo daños leves. Pero cuando las células cebadas fueron posteriormente infectadas con VRS, el segundo impacto desencadenó el montaje completo del inflamasoma, la activación de la enzima caspasa‑1, la formación de poros en la membrana celular y una forma ardiente de muerte celular conocida como piroptosis. Este proceso perforó las células, derramó contenidos inflamatorios y coincidió con mayores cantidades de virus infeccioso liberado al medio de cultivo.
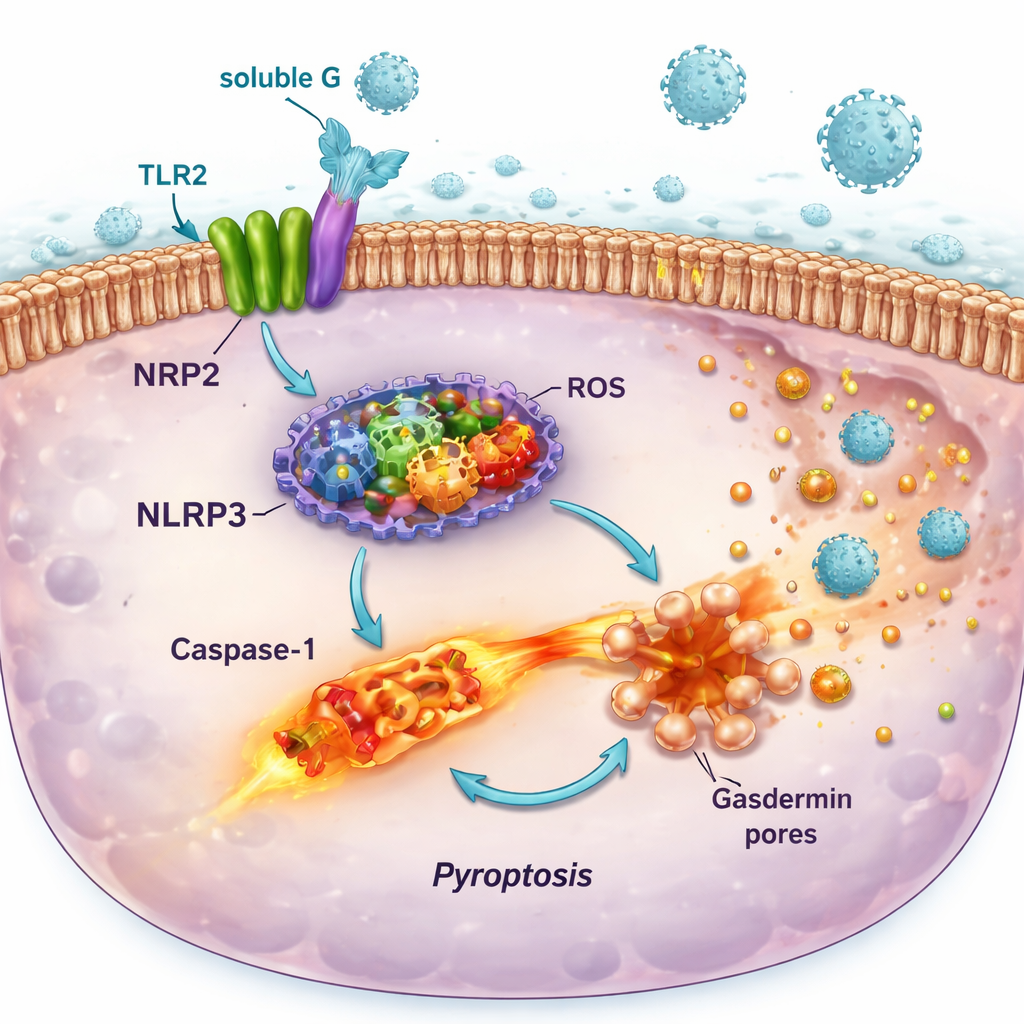
Cómo esta reacción en cadena puede empeorar la enfermedad pulmonar
El efecto pro‑letal de la G soluble fue más fuerte en las células epiteliales de las vías respiratorias—las mismas células que el VRS prefiere infectar—y dependió del inflamasoma NLRP3, porque un inhibidor específico de NLRP3 recuperó en gran medida la viabilidad celular. En contraste, ciertas células inmunitarias ricas en TLR2 pero pobres en el receptor CX3CR1 no sufrieron una muerte lítica intensa en las mismas condiciones. Este patrón sugiere que el VRS utiliza la G soluble para debilitar y destruir selectivamente el revestimiento protector de las vías respiratorias mientras preserva algunas células inmunitarias que pueden seguir emitiendo señales. El resultado es un entorno pulmonar con más inflamación, más desechos celulares y más oportunidades para que nuevas partículas virales escapen e infecten células vecinas.
Qué significa esto para futuros tratamientos
Para un no especialista, el mensaje clave es que el VRS no depende únicamente del daño directo por invasión viral. Al liberar grandes cantidades de proteína G soluble, puede “ablandar” las células cercanas a través de TLR2, haciéndolas más propensas a morir de forma inflamatoria y a derramar virus. Este trabajo identifica varios pasos en esa cadena—la G soluble en sí, su motivo CX3C, TLR2 y el inflamasoma NLRP3—como posibles dianas farmacológicas. En principio, terapias que bloqueen la interacción entre la G soluble y TLR2, o que modulen la actividad de NLRP3, podrían reducir tanto la lesión pulmonar como la propagación viral. Tales enfoques podrían algún día complementar las vacunas y anticuerpos existentes contra el VRS, ofreciendo mejor protección para los pacientes más jóvenes y vulnerables.
Cita: Meineke, R., Agac, A., Knittler, MC. et al. The soluble G protein of respiratory syncytial virus promotes viral dissemination via TLR2-mediated NLRP3 priming and pyroptosis. npj Viruses 4, 6 (2026). https://doi.org/10.1038/s44298-026-00172-x
Palabras clave: virus respiratorio sincitial, proteína G soluble, inflamasoma TLR2, piroptosis, inflamación pulmonar