Clear Sky Science · es
Evaluación STAR (stroma-tumor AI risk): asociación de la proporción tumor‑estroma derivada por IA con la supervivencia de los pacientes aporta valor pronóstico adicional más allá de KELIM en el cáncer epitelial de ovario
Por qué importa el “vecindario” alrededor de un tumor
Cuando pensamos en el cáncer, solemos imaginar una masa de células fuera de control. Pero los tumores conviven en un vecindario ocupado por tejido de soporte, vasos sanguíneos y células inmunitarias, denominado estroma. Este estudio plantea una pregunta sencilla pero poderosa: ¿podemos usar el equilibrio entre las células tumorales y este tejido circundante, medido mediante inteligencia artificial (IA) en las muestras habituales al microscopio, para predecir qué pacientes con cáncer de ovario tendrán mejores o peores resultados—antes incluso de comenzar el tratamiento?
Una nueva forma de leer las biopsias estándar
Las mujeres con cáncer epitelial de ovario suelen someterse a extracción de tejido en cirugía o biopsia. Esas muestras se tiñen y se examinan al microscopio en todos los hospitales. Los investigadores se centraron en una característica llamada proporción tumor–estroma (TSP): cuánto de la imagen está ocupado por tejido de soporte en comparación con las células cancerosas. En trabajos previos, los patólogos estimaban esta proporción a simple vista y observaron que los tumores ricos en estroma con frecuencia se comportaban de forma más agresiva y resistían la quimioterapia estándar basada en platino. En el estudio actual, el equipo empleó un sistema de IA de aprendizaje profundo para medir automáticamente la TSP en láminas digitalizadas, con el objetivo de convertir una tarea manual y algo subjetiva en una lectura rápida y reproducible disponible desde el diagnóstico.
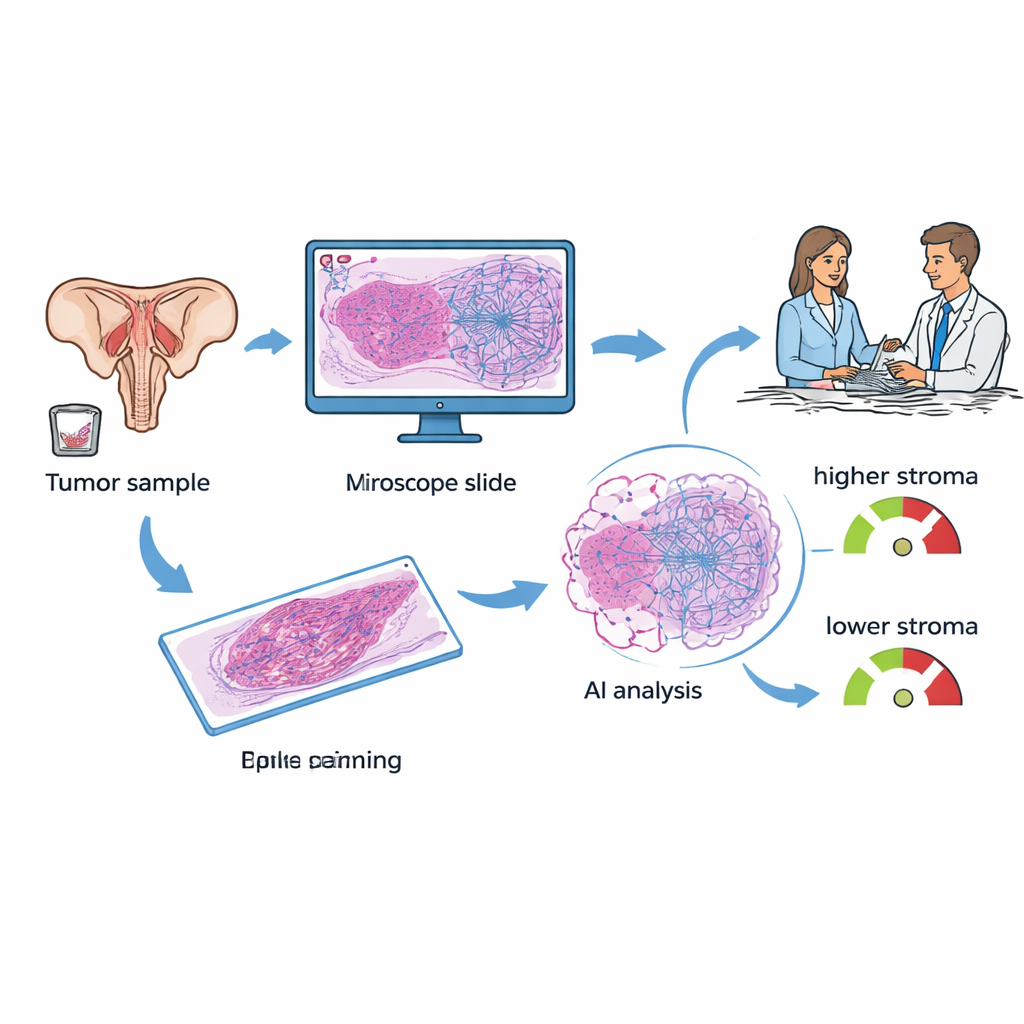
Comparando el análisis tisular por IA con una puntuación basada en sangre
Hoy en día, una herramienta ampliamente discutida para el cáncer de ovario es KELIM, una puntuación basada en la rapidez con que un marcador sanguíneo llamado CA‑125 disminuye durante los primeros 100 días de quimioterapia. KELIM es económica y útil, pero solo puede calcularse después de varias semanas de tratamiento, y no todas las pacientes tienen suficientes análisis tempranos para generar la puntuación. Los investigadores reunieron datos de 89 mujeres tratadas en un único centro oncológico que disponían tanto de láminas tisulares como de al menos tres mediciones de CA‑125. Calcularon KELIM para cada paciente, un patólogo etiquetó las regiones tumorales en las láminas y luego el modelo de IA estimó la TSP, clasificando cada caso como “baja en estroma” (menos del 50% de estroma) o “alta en estroma” (50% o más).
La IA iguala a los expertos y señala tumores de mayor riesgo
El criterio de la IA coincidió estrechamente con el de patólogos experimentados: en el 94% de los casos, la clasificación automatizada de TSP concordó con la manual, un nivel de concordancia considerado excelente. Al analizar los resultados clínicos, encontraron que las mujeres cuyos tumores fueron clasificados como altos en estroma por la IA tuvieron una supervivencia global significativamente peor que las de tumores bajos en estroma. En términos estadísticos, una TSP alta casi dobló el riesgo de muerte durante el periodo de seguimiento, y este efecto persistió incluso al ajustar por la puntuación KELIM. Por el contrario, en este grupo de pacientes del mundo real, KELIM se asoció con si los tumores eran resistentes a los fármacos con platino, pero no se vinculó de forma clara con la duración de la supervivencia.
Lo que esto podría significar para las decisiones terapéuticas
Puesto que la TSP puede medirse a partir de láminas rutinarias tomadas al diagnóstico, la TSP basada en IA ofrece una forma de evaluar el riesgo antes de iniciar la quimioterapia, potencialmente meses antes que KELIM. Un resultado de TSP alto podría alertar a los clínicos de que un tumor es más probable que sea agresivo y más difícil de tratar, lo que podría motivar un seguimiento más estrecho, la consideración anticipada de terapias adicionales o estrategias quirúrgicas distintas. El método también es relativamente de bajo coste: se basa en imágenes patológicas existentes y un modelo de software en lugar de nuevas pruebas de laboratorio. Los autores sostienen que la TSP automatizada podría complementar otros marcadores, como pruebas genéticas y las tendencias del CA‑125, para afinar el pronóstico sin añadir una carga sustancial a las pacientes ni a los equipos de patología.
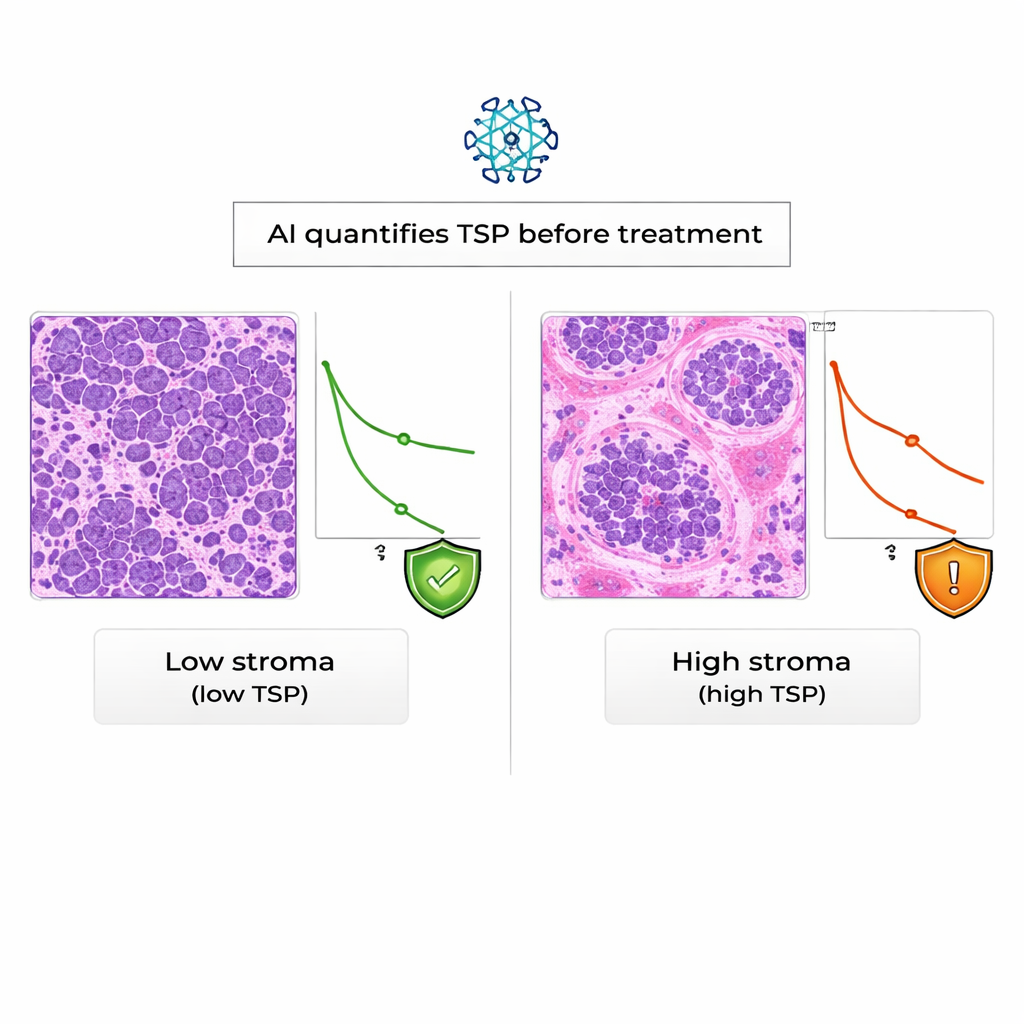
Mirando hacia adelante: orientación más inteligente y temprana para las pacientes
Para un público general, el mensaje principal es que no todos los cánceres de ovario son iguales y que el tejido de soporte alrededor del tumor contiene pistas importantes sobre cómo se comportará la enfermedad. Este estudio demuestra que la IA puede leer esas pistas de forma fiable en las biopsias estándar y que un tumor con predominio de estroma tiende a asociarse con una supervivencia peor, independientemente de las puntuaciones basadas en sangre existentes. Aunque se necesitan estudios más amplios y diversos antes de que este enfoque forme parte de la práctica habitual, la TSP derivada por IA promete ser una señal de alerta temprana que podría ayudar a los médicos a personalizar los planes de tratamiento y ofrecer a las pacientes expectativas más claras desde el inicio.
Cita: Aggarwal, A., Madill, M., Jana, M. et al. STAR (stroma-tumor AI risk) assessment: association of AI-derived tumor-stroma proportion with patient survival provides added prognostic value beyond KELIM in epithelial ovarian cancer. BJC Rep 4, 4 (2026). https://doi.org/10.1038/s44276-026-00205-1
Palabras clave: cáncer de ovario, inteligencia artificial, microambiente tumoral, biomarcador pronóstico, patología digital