Clear Sky Science · es
Estudio genómico descubre la aparición de una línea dominante multirresistente en poblaciones de Proteus mirabilis
Por qué este germen hospitalario te importa
Para muchas personas, las infecciones del tracto urinario son una molestia dolorosa ocasional. Pero en hospitales y residencias de ancianos, algunas infecciones las provocan bacterias resistentes que se adhieren a los catéteres, resisten múltiples antibióticos y se propagan silenciosamente entre personas y animales. Este estudio sigue a uno de esos culpables, Proteus mirabilis, a escala global, usando su ADN como un diario de viaje para revelar cómo una única línea familiar difícil de tratar ha ascendido silenciosamente hasta dominar durante el último siglo.
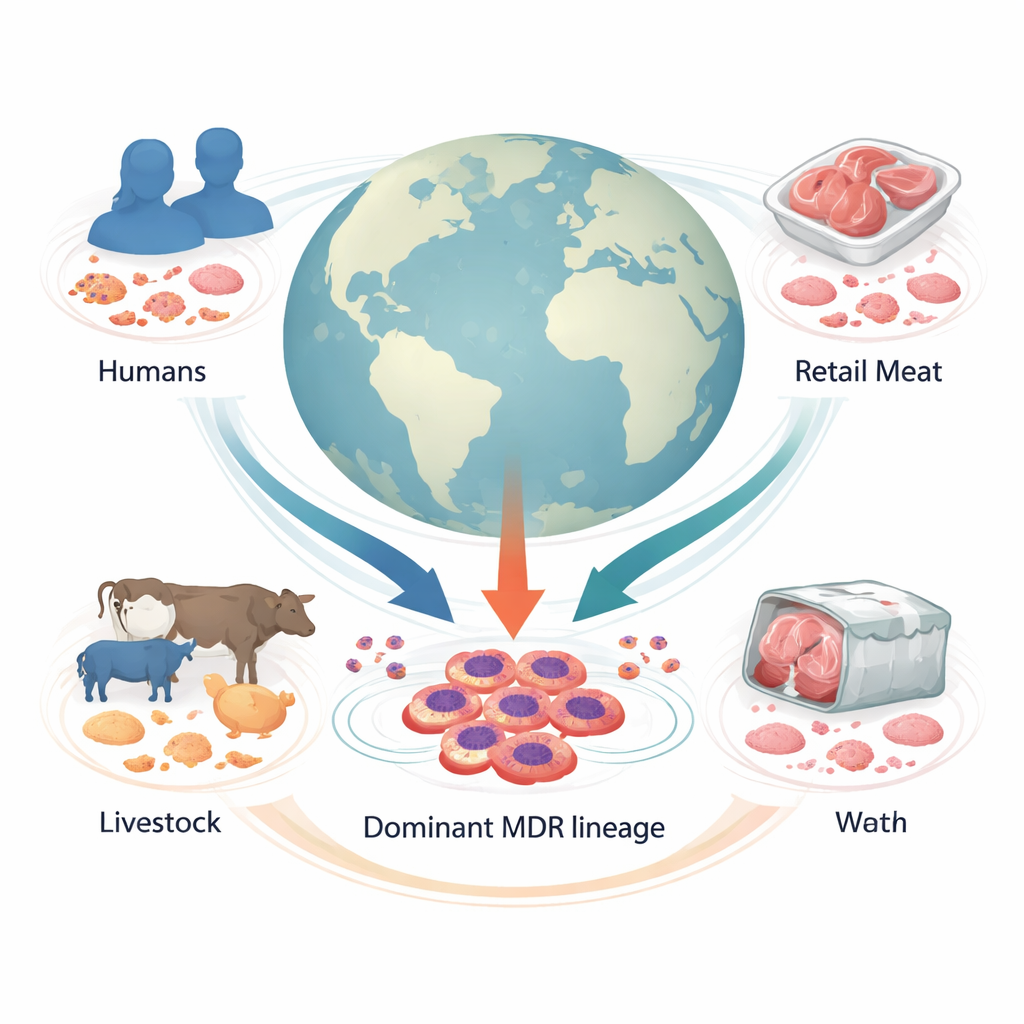
Una mirada global a una amenaza oculta
Los investigadores ensamblaron genomas de 1.142 muestras de Proteus mirabilis recogidas en 34 países procedentes de humanos, ganado, carne de venta al por menor y otros entornos. Al comparar genomas completos, clasificaron las bacterias en 178 familias genéticas. Una destacó: el “Clúster-1”, una línea principal que representó una de cada cinco muestras e incluía cepas de hospitales en varios continentes. La mayoría de estas cepas procedían de personas, pero una proporción considerable también provenía de animales de granja y carne, lo que indica que esta línea se mueve entre especies y a lo largo de la cadena alimentaria.
Una línea armada con numerosos escudos contra fármacos
Cuando el equipo escaneó los genomas en busca de genes de resistencia a antibióticos, el Clúster-1 presentó una carga claramente mayor. En promedio, sus miembros albergaban casi 18 genes de resistencia cada uno, muy por encima de otras líneas. Entre ellos había genes que desactivan algunos de nuestros antibióticos más potentes, como los carbapenémicos, que a menudo se reservan como última opción. Muchos de estos genes de resistencia se encuentran dentro de una gran “isla” de ADN llamada PmGRI1, que puede saltar entre bacterias. Algunas versiones de esta isla llevan más de 20 genes de resistencia a la vez, convirtiendo efectivamente a Proteus en una farmacia ambulante de defensas y dejando a los médicos con pocas opciones de tratamiento.
Rasgos pegajosos que ayudan a la bacteria a persistir
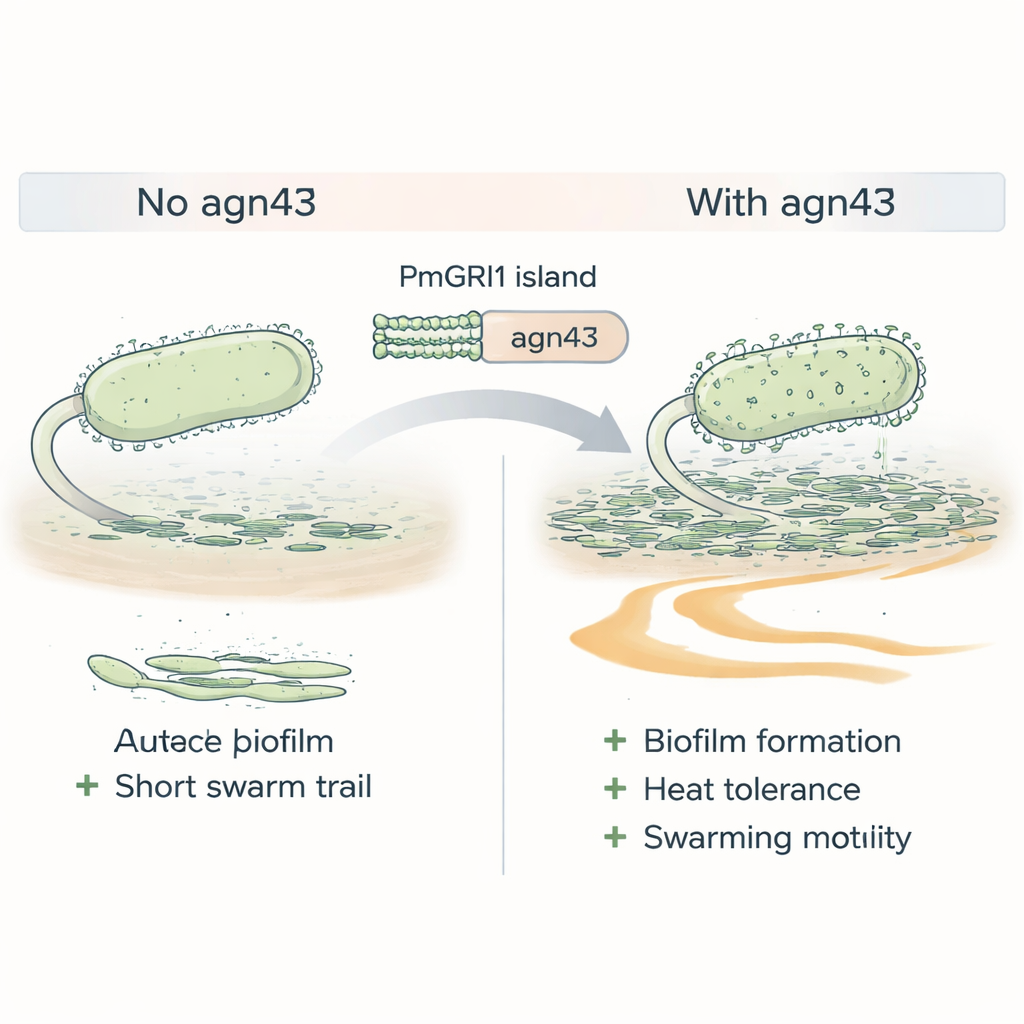
La resistencia por sí sola no garantiza el éxito; las bacterias también deben ser buenas sobreviviendo en el cuerpo y en el entorno hospitalario. Las cepas del Clúster-1 estaban enriquecidas en genes relacionados con la adhesión a células y la formación de biorrefugios—comunidades viscosas que protegen a las bacterias de los medicamentos y del sistema inmune—. Un gen destacado en la isla PmGRI1, llamado agn43, codifica una proteína de superficie que actúa como Velcro molecular, ayudando a las células a agregarse. Cuando los científicos eliminaron agn43 en una cepa del Clúster-1, el mutante formó biorrefugios más débiles, toleró peor el estrés por calor y se desplazó menos eficientemente por las superficies, rasgos que normalmente ayudan a Proteus a colonizar catéteres urinarios y propagarse dentro del tracto urinario.
Cómo y dónde se propagó esta superlínea
Combinando las diferencias genéticas con las fechas de aislamiento, los investigadores reconstruyeron una cronología para el Clúster-1. Calcularon que su ancestro común más reciente apareció alrededor de 1910, décadas antes de que los antibióticos modernos se usaran de forma generalizada. Posteriormente, la línea se dividió en dos ramas de importancia médica: una principalmente observada en China que porta un gen que inactiva carbapenémicos llamado blaKPC-2, y otra principalmente en Estados Unidos que porta un gen relacionado, blaIMP-27. Desde finales de la década de 1980, el Clúster-1 se expandió rápidamente y se detectó repetidamente moviéndose entre países y entre humanos, ganado y carne, subrayando su potencial epidémico.
Qué significa esto para los pacientes y la salud pública
Para el público en general, el mensaje es que una familia particular de Proteus mirabilis ha evolucionado hasta convertirse en un germen hospitalario muy exitoso combinando dos ventajas: una gruesa armadura de genes de resistencia a antibióticos y una «pegajosidad» extra que le ayuda a formar películas protectoras y persistir en catéteres y tejidos. Esta combinación hace que las infecciones sean más difíciles de tratar y más fáciles de propagar. El trabajo pone de manifiesto la necesidad de una vigilancia genética estrecha de esta línea tanto en hospitales como en la agricultura, un control de infecciones más estricto en torno a los catéteres y un uso prudente de los antibióticos para frenar la aparición y la circulación global de cepas multirresistentes como esta.
Cita: Zhang, T., Wei, H., Ju, Z. et al. Genomic survey uncovers the emergence of a multidrug-resistant dominant lineage in Proteus mirabilis populations. npj Antimicrob Resist 4, 17 (2026). https://doi.org/10.1038/s44259-026-00189-5
Palabras clave: resistencia a los antibióticos, infección del tracto urinario, infecciones hospitalarias, genómica bacteriana, biófilm