Clear Sky Science · es
Sinergia entre fagos y meropenem frente a aislamientos clínicos de Klebsiella pneumoniae productoras de OXA-48
Por qué los virus diminutos podrían salvar antibióticos que fallan
Los hospitales de todo el mundo luchan contra infecciones que ya no responden a nuestros antibióticos más potentes. Uno de los peores culpables es una bacteria llamada Klebsiella pneumoniae, que puede causar neumonía, infecciones del torrente sanguíneo e infecciones del tracto urinario. Este estudio explora si virus cuidadosamente seleccionados que atacan bacterias —llamados fagos— pueden asociarse con un antibiótico potente, el meropenem, para eliminar cepas altamente resistentes que actualmente amenazan la vida de los pacientes.
Un germen sigiloso de hospital en aumento
Klebsiella pneumoniae se ha convertido en un importante supergermen hospitalario porque muchas cepas han aprendido a resistir a los carbapenémicos, una familia de antibióticos reservada como última línea de defensa. Estas bacterias a menudo portan genes de resistencia en pequeños círculos de ADN llamados plásmidos, que pueden intercambiarse entre sí como si fuesen cromos coleccionables. Uno de esos plásmidos, conocido como pOXA-48, codifica una enzima que descompone los carbapenémicos, dejando fármacos como el meropenem en gran medida inútiles. A medida que estos plásmidos se propagan por clones bacterianos de alto riesgo en Europa y más allá, los tratamientos estándar se vuelven menos fiables, haciendo incluso los procedimientos médicos rutinarios más peligrosos.
Reclutar fagos como atacantes de precisión
Dado que los nuevos antibióticos tardan en llegar, los investigadores recurren a la terapia con fagos —usar virus que infectan y matan bacterias de forma específica. En este estudio, el equipo se centró en un fago lítico llamado vB_Kpn_2-P4, que puede infectar un amplio conjunto de aislados clínicos de Klebsiella recogidos en hospitales españoles. En pruebas de laboratorio, este fago pudo atacar bacterias que portaban varios mecanismos diferentes de resistencia a los carbapenémicos. Sin embargo, como suele ocurrir tanto con antibióticos como con fagos, algunas células bacterianas acabaron sobreviviendo y volviendo a crecer, lo que subraya la necesidad de estrategias combinadas en lugar de confiar en un solo arma.
Cuando el fármaco y el virus funcionan mejor juntos
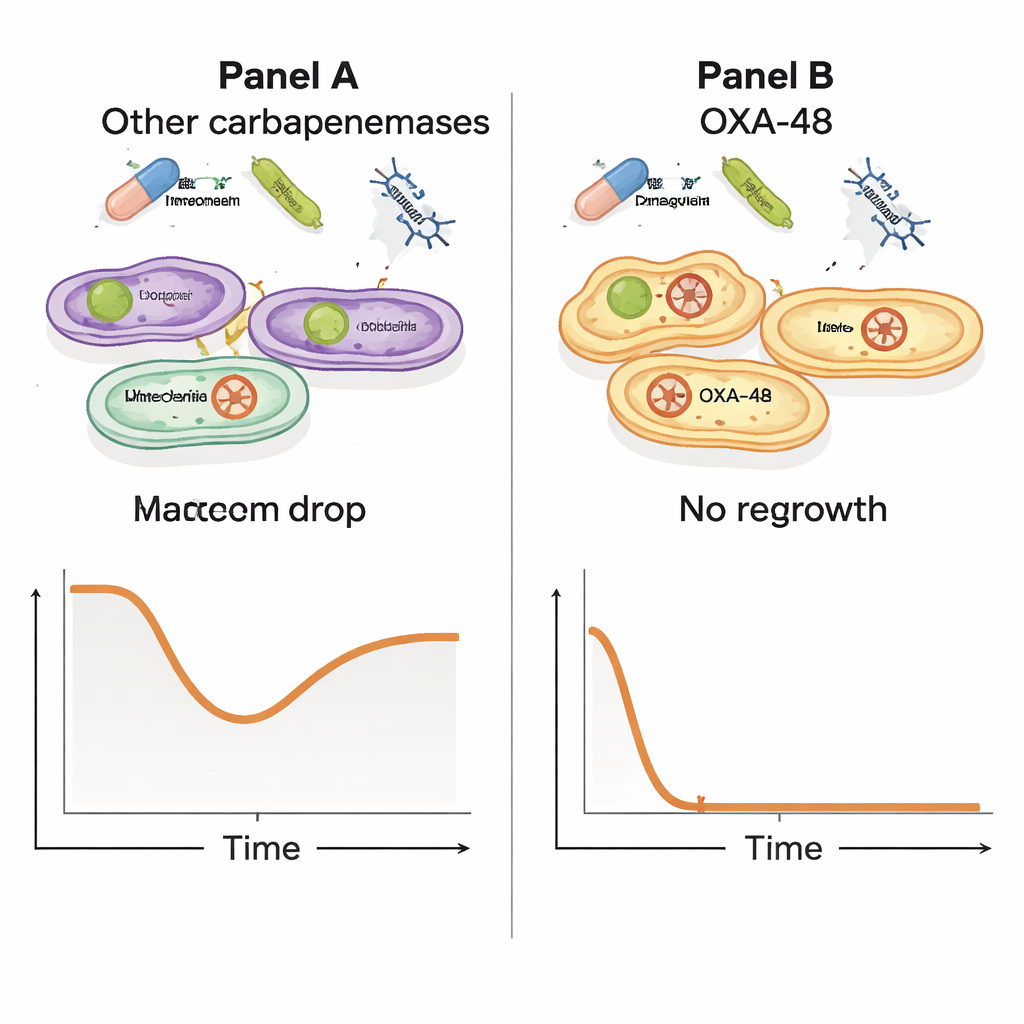
Los investigadores probaron entonces cómo se comportaban el meropenem y el fago cuando se usaban en conjunto. Hicieron crecer doce aislados resistentes y los expusieron a meropenem solo, al fago solo o a ambos a la vez, siguiendo el crecimiento durante muchas horas. Aunque todos los aislados pudieron tolerar meropenem en las condiciones de la prueba, emergió un patrón llamativo: en cepas que portaban el plásmido OXA‑48, la combinación de fago más meropenem a alta dosis provocó un desplome dramático en el número de bacterias, seguido de ausencia de re-crecimiento detectable. A niveles más bajos de meropenem, estas cepas con OXA‑48 todavía mostraron una fuerte caída en la carga bacteriana. En contraste, las cepas con otras enzimas de resistencia no mostraron este potente efecto conjunto, lo que sugiere que alguna característica especial del plásmido OXA‑48 hace que las bacterias sean especialmente vulnerables cuando enfrentan ambas amenazas a la vez.
Rastreando el ayudante genético oculto
Para entender por qué solo los productores de OXA‑48 mostraron esta sinergia, el equipo comparó los genomas de los distintos aislados bacterianos. Identificaron docenas de genes asociados con la respuesta sinérgica, casi todos agrupados en el plásmido pOXA‑48. Es importante destacar que, cuando aislaron bacterias que habían evolucionado resistencia al fago, estos supervivientes seguían portando un gen OXA‑48 intacto; no habían descartado simplemente el plásmido para escapar. Esto apunta a un panorama más sutil en el que el plásmido que confiere resistencia a los fármacos también impone costes ocultos en la biología de la bacteria —costes que se vuelven letales cuando el fago y el antibiótico atacan a la vez, inclinando la balanza en contra del patógeno.
Qué podría significar esto para tratamientos futuros
Para los no especialistas, el mensaje clave es que las mismas argucias genéticas que usan las bacterias para eludir nuestros fármacos a veces pueden volverse en su contra. En este caso, un plásmido de resistencia específico parece hacer que ciertas cepas de Klebsiella sean exquisitamente sensibles a un ataque combinado por un fago a medida y meropenem. Aunque este trabajo se realizó en condiciones de laboratorio y se necesita más investigación en modelos animales y en pacientes, sugiere que emparejar el fago adecuado con el perfil de resistencia correcto podría revivir antibióticos que parecen haber perdido su eficacia. En lugar de reemplazar a los antibióticos, los fagos podrían convertirse en aliados inteligentes que nos ayuden a superar a los supergérmenes que antes parecían invencibles.
Cita: Cantallops, I., Ferriol-González, C., Barcos-Rodríguez, T. et al. Phage-meropenem synergy against OXA-48-producing Klebsiella pneumoniae clinical isolates. npj Antimicrob Resist 4, 12 (2026). https://doi.org/10.1038/s44259-026-00186-8
Palabras clave: terapia con fagos, resistencia a antibióticos, Klebsiella pneumoniae, plásmido OXA-48, sinergia con meropenem