Clear Sky Science · es
Respuesta global a la exposición a antibióticos revela un papel crítico del metabolismo de nucleótidos en la tolerancia de alto nivel a β-lactámicos
Por qué algunas bacterias resisten a nuestros mejores antibióticos
Los antibióticos deberían eliminar las bacterias dañinas, sin embargo muchas infecciones persisten obstinadamente o reaparecen tras el tratamiento. Este artículo explora una razón poco valorada: algunas bacterias pueden acorazarse y sobrevivir temporalmente incluso a dosis muy altas de fármacos potentes como la penicilina. Al descubrir cómo estos microbios reconfiguran su química interna para capear el ataque, los investigadores señalan nuevas vías para restaurar la eficacia de antibióticos existentes.
Un truco de supervivencia sigiloso dentro de las infecciones
Al exponerse a antibióticos β-lactámicos como la penicilina, muchas bacterias Gramnegativas peligrosas no mueren simplemente. En lugar de ello, pueden deshacerse de su pared celular rígida y transformarse en cuerpos frágiles y redondeados llamados esferoplastos. En esta forma dejan de multiplicarse pero permanecen vivos y metabólicamente activos. Una vez que el fármaco desaparece, reconstruyen su pared, recuperan su forma normal de bastón y pueden reavivar la infección. Dado que esta “tolerancia” es un paso hacia la resistencia antibiótica plena y al fracaso del tratamiento, entender cómo sobreviven los esferoplastos es crucial para la medicina futura.
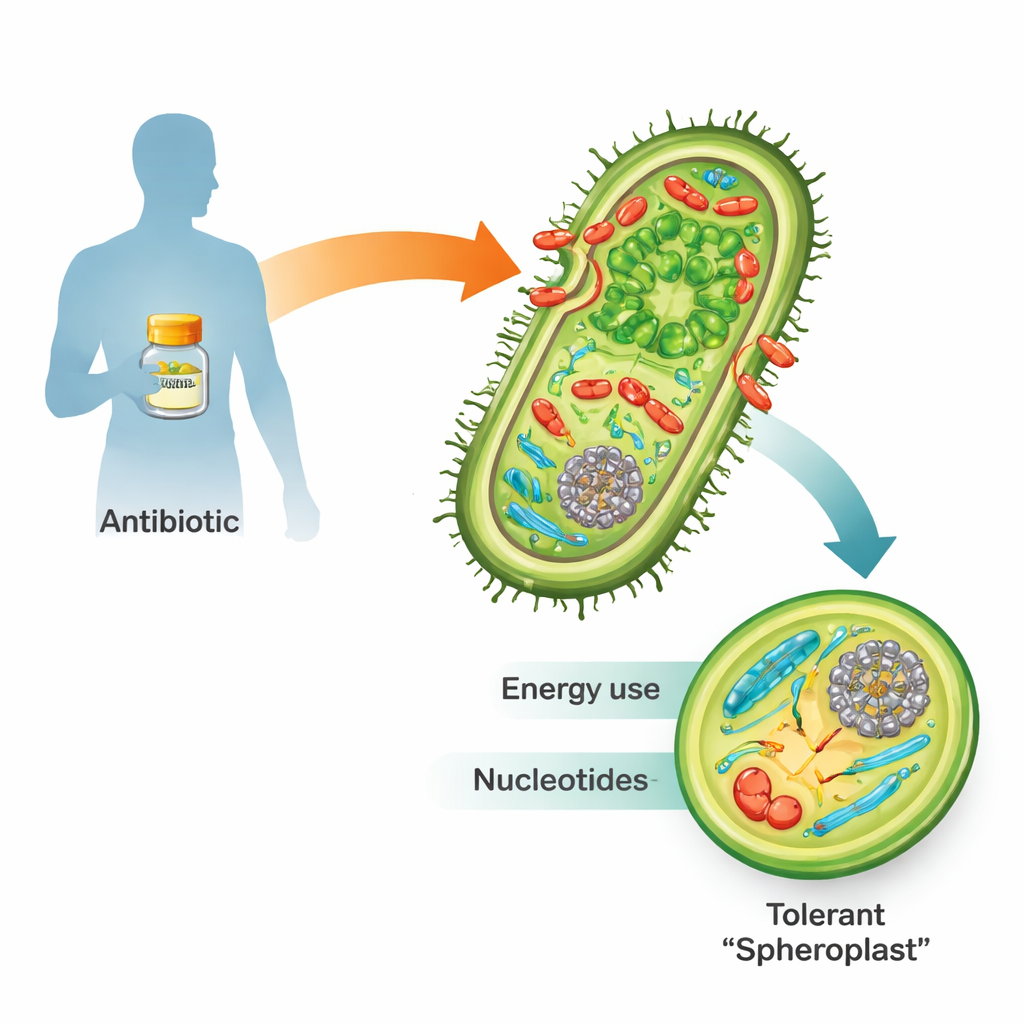
Escuchando la alerta de emergencia de la célula
El equipo utilizó Vibrio cholerae, la bacteria que causa el cólera, como modelo porque es excepcionalmente tolerante a los β-lactámicos y fácil de manipular genéticamente. Bañaron las bacterias en diez veces la dosis letal mínima de penicilina y siguieron la respuesta a lo largo del tiempo con dos herramientas potentes. La transcriptómica registró qué genes se activaban o desactivaban, mientras que la metabolómica midió cientos de pequeñas moléculas que alimentan y construyen la célula. Juntas, estas técnicas “multi-ómicas” crearon un mapa temporal de cómo una célula tolerante remodela su maquinaria interna durante un asalto farmacológico.
Redirección metabólica y un punto débil oculto
Los datos revelaron cambios extensos en rutas centrales. Los genes para construir la pared celular se encendieron con fuerza, coherente con el intento de la célula de reparar daños y prepararse para la recuperación. Los sistemas de choque térmico y respuesta al estrés también se activaron, probablemente para manejar proteínas mal plegadas u oxidadas generadas por el estrés inducido por el antibiótico. Al mismo tiempo, el metabolismo central del carbono cambió: ciertos pasos del ciclo del TCA (el principal generador de energía de la célula) se vieron potenciados, mientras que intermediarios clave de la glucólisis como glucosa-6-fosfato y fructosa-6-fosfato se agotaron drásticamente. Estos intermediarios normalmente alimentan tanto la producción de energía como la síntesis de la pared celular, lo que sugiere que un continuo y derrochador “ciclado inútil” de material de pared estaba drenando recursos.
Nucleótidos bajo presión
El cambio más llamativo afectó a los nucleótidos, los bloques constructores del ADN, ARN y muchas moléculas portadoras de energía. Los niveles de muchos nucleótidos y sus precursores se desplomaron en las células tratadas con penicilina, pese a que los genes para fabricarlos desde cero estaban fuertemente activados. Al mismo tiempo, los genes implicados en el “reciclaje” de nucleótidos se reprimieron, como si la célula intentara conservar lo poco que quedaba. Estos patrones sugerían que los esferoplastos estaban bajo un estrés severo de nucleótidos. Cuando los investigadores interfirieron deliberadamente con rutas que suministran precursores de nucleótidos —como la vía de las pentosas fosfato— o bloquearon la producción de nucleótidos con otro fármaco, trimetoprim, la combinación con β-lactámicos mató a muchas más bacterias que cualquiera de los fármacos por separado. Esta fuerte sinergia se observó no solo en Vibrio cholerae, sino también en cepas clínicas altamente tolerantes de Klebsiella pneumoniae y Escherichia coli.
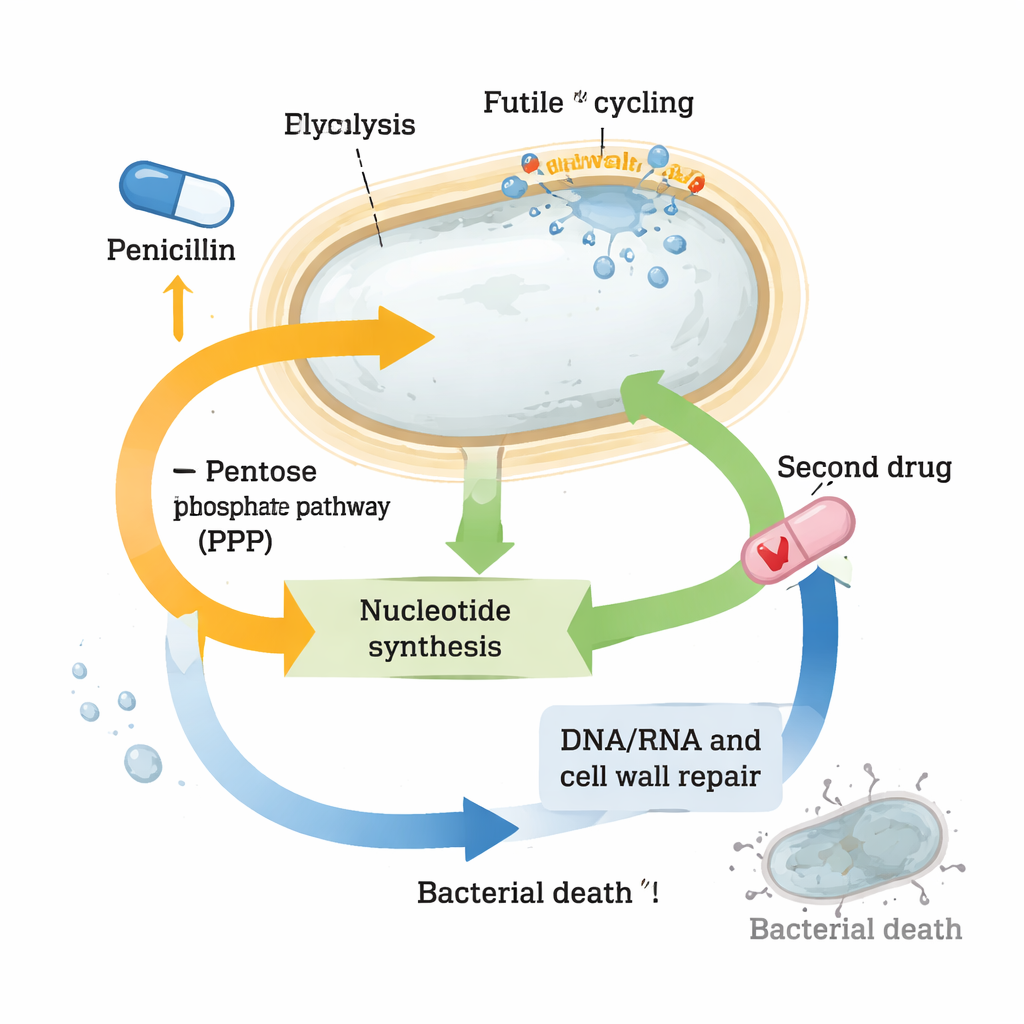
Convertir la química de supervivencia en una ventaja terapéutica
A pesar de la importante remodelación de su metabolismo, los esferoplastos tolerantes logran mantener su moneda energética, el ATP, relativamente estable y evitar daños catastróficos, lo que les ayuda a sobrevivir exposiciones largas a antibióticos. Pero el trabajo muestra que, al hacerlo, empujan sus reservas de nucleótidos hasta el límite. Ese equilibrio precario crea una vulnerabilidad: empujar un poco más el metabolismo de nucleótidos con un segundo fármaco colapsa sus defensas y restaura una muerte eficaz. Para lectores no especializados, la conclusión es que algunas bacterias sobreviven a los antibióticos no porque los fármacos dejen de alcanzar sus blancos, sino porque las células reconfiguran rápidamente su química para soportar el golpe. Al encontrar y explotar los eslabones débiles en ese cableado de supervivencia —aquí, el metabolismo de nucleótidos— los investigadores podrían convertir antibióticos antiguos en terapias combinadas potentes que superen incluso a patógenos muy tolerantes.
Cita: Keller, M.R., Kazi, M.I., Saleh, A. et al. Global response to antibiotic exposure reveals a critical role for nucleotide metabolism in high-level β-lactam tolerance. npj Antimicrob Resist 4, 11 (2026). https://doi.org/10.1038/s44259-026-00183-x
Palabras clave: tolerancia a antibióticos, antibióticos β-lactámicos, metabolismo de nucleótidos, persistencia bacteriana, combinaciones de fármacos