Clear Sky Science · es
Atenuación de la activación epicárdica y de la abundancia de miofibroblastos mediante el eje Fbln2–Nupr1b estimula la regeneración cardíaca en pez cebra
Por qué algunos corazones pueden sanarse solos
Cuando una persona sufre un infarto, el músculo dañado suele quedar cubierto por una cicatriz rígida que nunca llega a sanar por completo. El pez cebra, un pequeño pez de acuario con franjas, hace algo notable en su lugar: regenera el tejido cardíaco y finalmente elimina la mayor parte de la cicatriz. Este estudio plantea una pregunta aparentemente sencilla con grandes implicaciones médicas: ¿cómo sabe un corazón en proceso de curación cuándo debe formar tejido cicatricial y cuándo eliminarlo para permitir el crecimiento de músculo nuevo? Al descifrar este equilibrio en el pez cebra, el trabajo apunta a estrategias que podrían, algún día, ayudar a los corazones humanos lesionados a repararse a sí mismos en vez de fallar.
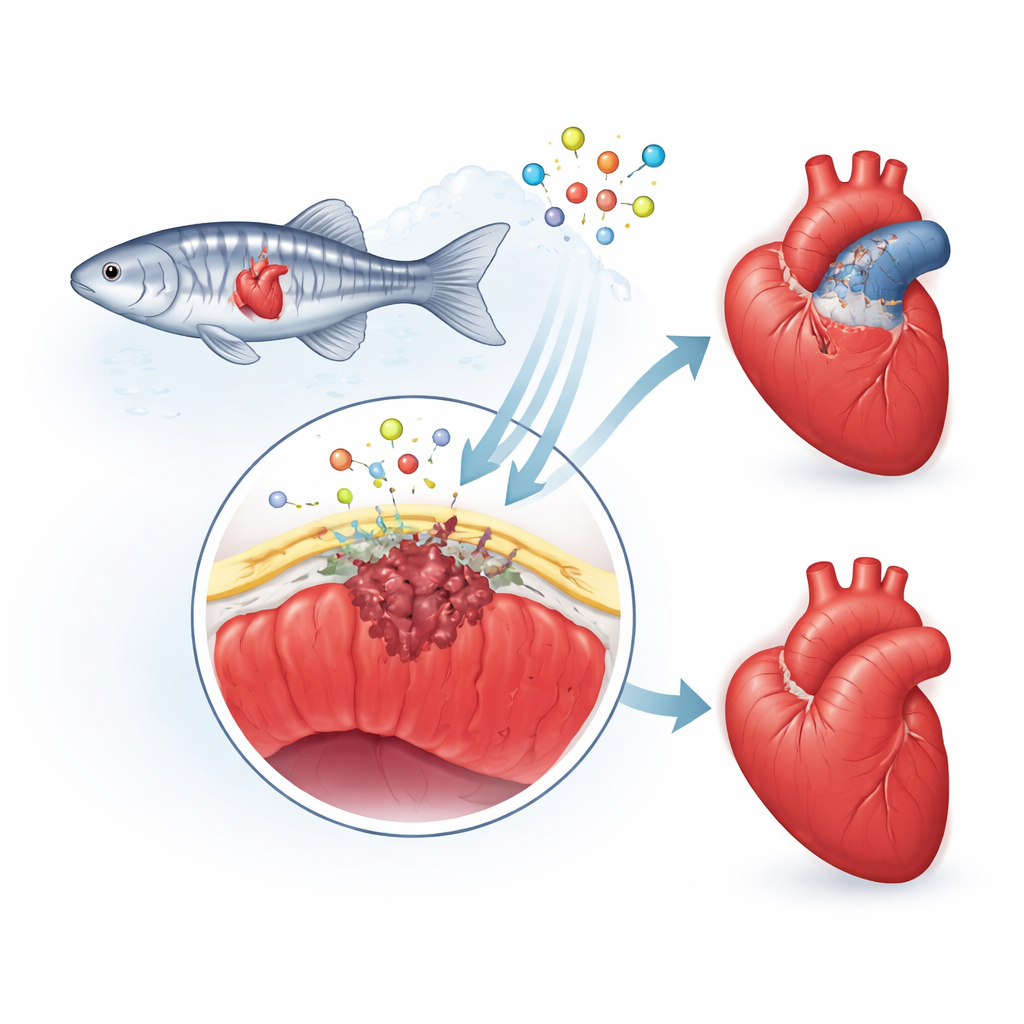
La piel protectora del corazón
Los investigadores se centran en el epicardio, una delgada «piel» que recubre el corazón. Tras una lesión, esta capa se activa, sus células cambian de identidad y algunas se internan en el área dañada. Allí se convierten en células de soporte y en formadoras de cicatriz, y liberan señales químicas que guían el crecimiento de nuevos vasos sanguíneos y del músculo cardíaco. En las personas, esta respuesta reparadora tiende a sobreactuarse, dejando una cicatriz gruesa y permanente. En el pez cebra, sin embargo, la cicatriz es temporal y se descompone de forma gradual a medida que vuelve el músculo sano. El equipo sospechó que una proteína llamada fibulina-2 (Fbln2), que reside en la matriz que rodea el corazón, ayuda a marcar el ritmo y la intensidad de esta respuesta epicárdica.
Un regulador molecular de la cicatrización
Usando edición genética en pez cebra, los científicos crearon dos tipos de animales con niveles distintos de Fbln2: una línea con Fbln2 reducida y otra con la proteína completamente eliminada. Les lesionaron los corazones con una sonda fría, imitando un infarto, y siguieron la curación durante semanas a meses. Cuando los niveles de Fbln2 disminuyeron, la división celular temprana en el músculo cardíaco y en el endotelio vascular se redujo, pero la cicatriz fibrosa que se formó fue más pequeña y más fácil de remodelar. A los tres meses, estos corazones se habían regenerado bien y retenían poca colágena, el principal material de la cicatriz. En cambio, los peces que carecían completamente de Fbln2 mostraron una inhibición más potente de una vía clave de crecimiento y cicatrización, que involucra a una familia de señales conocida como TGFβ, y tuvieron muchas menos células formadoras de cicatriz justo debajo del epicardio. Sus cicatrices tempranas también eran más pequeñas; sin embargo, con el tiempo estos corazones no lograron eliminar el colágeno y acabaron con cicatrices grandes y duraderas y una regeneración pobre.
Analizando los cambios de estado epicárdico
Para ver cómo se comportaban las células epicárdicas a resolución de célula única, el equipo empleó secuenciación de ARN unicelular poco después de la lesión. Identificaron varios «estados» celulares epicárdicos, incluidos células en reposo, células recién activadas, células estresadas que se adaptan a la baja disponibilidad de oxígeno y células que estaban proliferando activamente. En peces con niveles normales de Fbln2, las células epicárdicas progresaban con fluidez desde el estado de reposo a la activación y luego a estados maduros. En peces con Fbln2 reducido o ausente, esta progresión se estancó: las células permanecían en etapas tempranas y los grupos activados más maduros estaban insuficientemente representados, especialmente en los animales con pérdida completa. Múltiples genes que normalmente se encienden durante la activación epicárdica y en respuesta a la señalización TGFβ estaban atenuados, lo que apunta a Fbln2 como un modulador de esta vía que decide cuánto se compromete el epicardio a formar y remodelar tejido cicatricial.
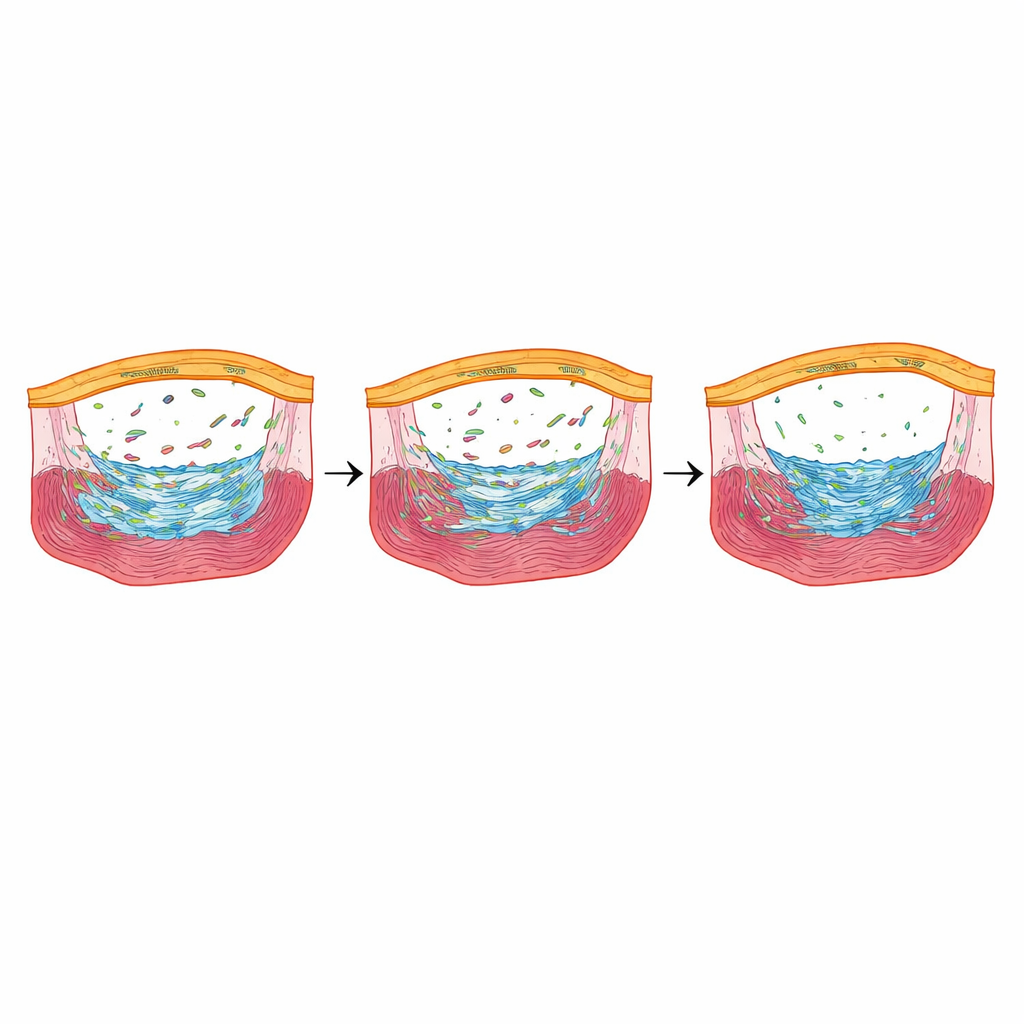
Un respondededor al estrés que ajusta la reparación
Entre los genes más marcadamente reducidos cuando Fbln2 se bajó, destacó uno: nupr1b, un regulador sensible al estrés activo en las células epicárdicas durante la fase temprana de la reparación. Cuando los investigadores eliminaron nupr1b, los peces mostraron menos células epicárdicas formadoras de cicatriz y una proliferación reducida de las células del músculo cardíaco, y mantuvieron amplios depósitos de colágena meses después de la lesión —muy parecido a los peces que carecían totalmente de Fbln2. De forma llamativa, cuando forzaron brevemente la reexpresión de nupr1b solo en las células epicárdicas de los peces con Fbln2 reducido, el número de células formadoras de cicatriz y la proliferación del músculo cardíaco se recuperaron, y aumentó la cicatrización tardía. Bloquear químicamente los receptores de TGFβ redujo los niveles de nupr1b, situando a nupr1b corriente abajo de un eje de señalización Fbln2–TGFβ.
Qué significa esto para la curación del corazón humano
En conjunto, estos hallazgos revelan un «eje epicárdico Fbln2–Nupr1b» que ayuda a los corazones de pez cebra a caminar por la cuerda floja entre muy poca y demasiada fibrosis. Atenuar ligeramente este eje modera el estallido inicial de cicatrización y facilita la eliminación eficiente de la cicatriz, mientras que apagarlo por completo descarrila la regeneración y deja atrás una cicatriz rígida. Para la medicina humana, la lección es que el objetivo no es bloquear la cicatrización por completo, sino ajustarla: mantener suficiente estructura para evitar la rotura mientras se asegura que el tejido cicatricial sea temporal y pueda ser reemplazado por músculo sano. Entender y, eventualmente, aprovechar este sistema de control del pez cebra podría orientar futuras terapias que inducen al corazón humano lesionado hacia una regeneración verdadera en lugar de una cicatrización crónica.
Cita: Kayman Kürekçi, G., Kaur Bajwa, G., Zhang, S. et al. Attenuation of epicardial activation and myofibroblast abundance via the Fbln2–Nupr1b axis stimulates cardiac regeneration in zebrafish. Nat Cardiovasc Res 5, 218–233 (2026). https://doi.org/10.1038/s44161-026-00785-8
Palabras clave: regeneración cardíaca, fibrosis, pez cebra, epicardio, señalización TGF-beta