Clear Sky Science · es
Evaluación integradora genómica y bibliográfica de la miocardiopatía arritmogénica relacionada con desmogleína 2 con validación en una cohorte italiana
Por qué este gen cardíaco importa a las familias
Muchos problemas cardíacos súbitos en personas jóvenes y por lo demás sanas no son aleatorios: están escritos, al menos en parte, en su ADN. Este artículo explora una proteína clave que actúa como “pegamento” en el corazón, denominada desmogleína‑2, y muestra cómo pequeños cambios en su gen pueden debilitar el músculo cardíaco, alterar su ritmo eléctrico y aumentar el riesgo de eventos peligrosos. Al combinar grandes bases de datos genéticas con un grupo de pacientes italianos seguidos de forma rigurosa, los investigadores ofrecen respuestas más claras para las familias que se preguntan qué significa realmente un resultado de prueba en este gen.
El pegamento mecánico del corazón
Las células del músculo cardíaco deben mantenerse fuertemente unidas mientras laten millones de veces a lo largo de la vida. La desmogleína‑2 forma parte de una estructura microscópica en forma de remache que bloquea las células vecinas entre sí para que puedan tirar como un equipo. Los autores explican cómo esta proteína se extiende desde el exterior de la célula, donde se agarra a una pareja equivalente en la célula contigua, hasta el interior, donde se engancha a un armazón de soporte. Dado que la desmogleína‑2 es el único miembro de su familia presente en las células cardíacas, cualquier daño serio en ella no puede ser compensado por un sustituto, lo que hace al corazón especialmente vulnerable.
Distinguir cambios genéticos significativos del ruido de fondo
La secuenciación moderna encuentra miles de diferencias en el gen de la desmogleína‑2 en la población, pero la mayoría no causan enfermedad. El equipo revisó sistemáticamente 115 estudios publicados y recurrió a dos grandes bases de datos públicas que en conjunto listaban más de 5.000 variantes. Usando normas ampliamente aceptadas en genética médica, reclasificaron cada cambio según la probabilidad de que sea dañino. Encontraron que las variantes realmente perjudiciales se agrupan en regiones específicas de la proteína: especialmente en los segmentos externos que necesitan calcio para formar un puente rígido entre células, en un tramo corto que debe ser cortado para que la proteína madure, y en la región interna que se une a otra proteína cardiaca clave. Muchos otros cambios permanecieron “inciertos”, pero un subconjunto mostró indicios sólidos de ser importantes y se marcó para un seguimiento más estrecho.
Lo que revela el grupo de pacientes italiano
Para ver cómo se manifiestan estos patrones genéticos en personas reales, los investigadores estudiaron a 95 individuos en Italia que portaban variantes de desmogleína‑2 y fueron evaluados en profundidad con ecografías, pruebas de ritmo cardíaco y seguimiento a largo plazo. Aproximadamente la mitad cumplía criterios estrictos de miocardiopatía arritmogénica, una condición en la que partes del músculo cardíaco son lentamente reemplazadas por cicatriz y grasa, preparando el terreno para alteraciones del ritmo peligrosas. Entre los familiares portadores de una variante, solo alrededor de cuatro de cada diez mostraron signos de enfermedad, lo que subraya que un resultado genético positivo no garantiza enfermedad pero señala la necesidad de una vigilancia cuidadosa. Quienes tenían enfermedad manifiesta presentaron una carga notable de eventos arrítmicos graves, mientras que los trasplantes y las muertes fueron menos frecuentes pero todavía se observaron.
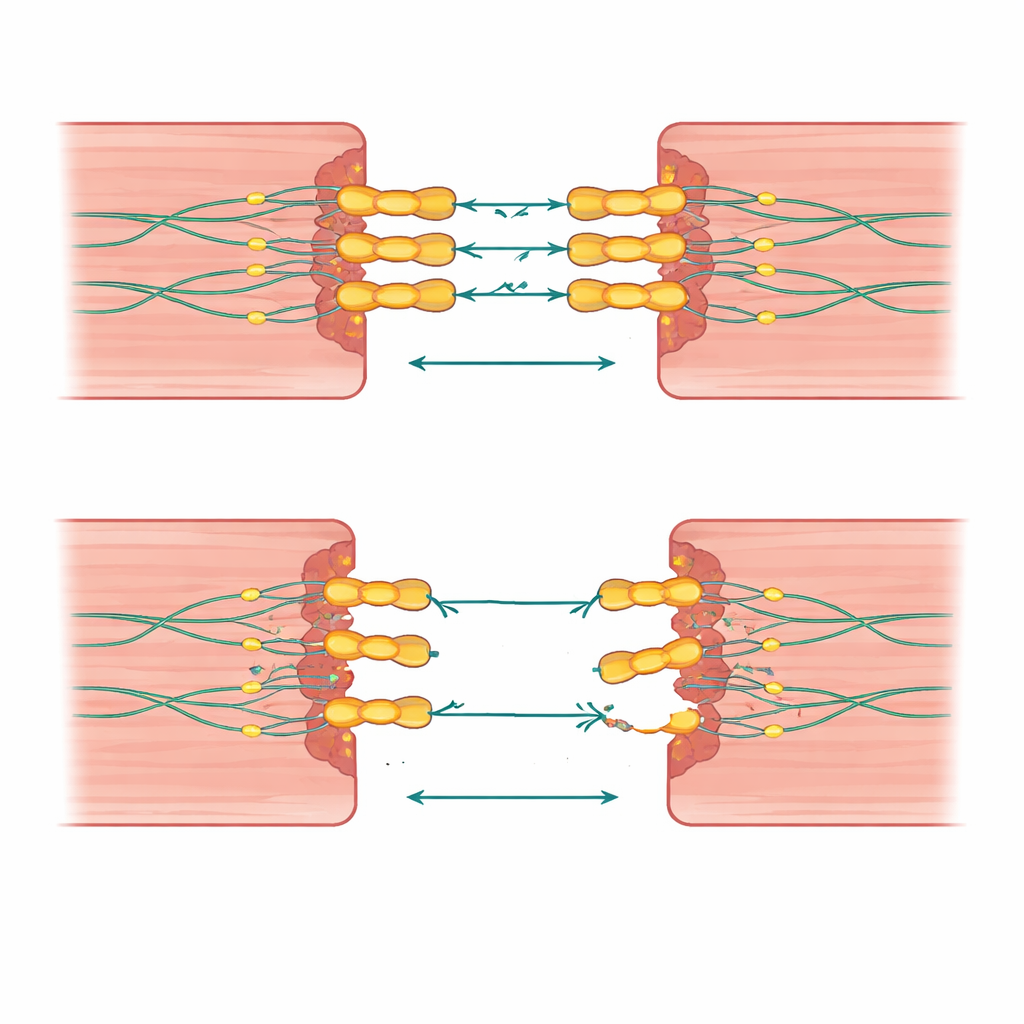
Cuando un solo golpe no es suficiente
Una percepción llamativa de este trabajo es que el número y la combinación de cambios genéticos importan. Las personas que heredaron dos copias defectuosas de desmogleína‑2, o una variante de desmogleína‑2 más un cambio en un gen vecino relacionado con el “pegamento” cardíaco, tendieron a enfermar más jóvenes y a mostrar un daño más generalizado en ambos lados del corazón. Algunas familias presentaron grandes deleciones o duplicaciones que eliminaban o duplicaban no solo a desmogleína‑2 sino también a genes adyacentes, vinculando de nuevo estas alteraciones a una enfermedad agresiva y a clusters de muertes súbitas. En contraste, muchos familiares con un solo cambio tuvieron síntomas leves o inexistentes, lo que sugiere que genes de fondo y factores de vida como el ejercicio pueden inclinar la balanza entre un riesgo silencioso y la enfermedad manifiesta.
De la forma de la proteína al riesgo para el paciente
Para relacionar el código DNA con efectos físicos, el equipo utilizó modelos proteicos 3D avanzados para ver cómo sustituciones específicas podrían aflojar el armazón de la desmogleína‑2. Los cambios que distorsionaban los bucles de unión al calcio o rompían puntos clave de anclaje se predijeron como desestabilizadores de la proteína y debilitadores de la adhesión célula a célula. Estas pistas estructurales se incorporaron al sistema de clasificación, ayudando a mover algunas variantes limítrofes hacia una consideración más probable de dañinas o, por el contrario, más probables de ser benignas. Este puente entre el modelado molecular y los datos clínicos lleva las pruebas genéticas más allá de la lectura del código hacia una comprensión más funcional.
Qué significa esto para pacientes y familias
Para las familias afectadas por la miocardiopatía arritmogénica, este estudio ofrece tanto precaución como orientación. Muestra que no toda variante de desmogleína‑2 es una sentencia a una enfermedad cardíaca severa, pero que ciertos patrones—especialmente impactos múltiples o cambios en regiones críticas de la proteína—se asocian con problemas más tempranos y graves. Los autores sostienen que las personas portadoras de estas variantes no deberían ser descartadas como “sanas hasta que se demuestre lo contrario”, sino seguidas de por vida con controles de ritmo e imagen personalizados. Su enfoque integrador—combinando genética de grandes datos, estudios familiares detallados y estructura proteica—apunta hacia estimaciones de riesgo más precisas y un asesoramiento más seguro cuando aparece un cambio en desmogleína‑2 en una prueba genética.
Cita: Pinci, S., Celeghin, R., Martini, M. et al. Integrative genomic and literature assessment of desmoglein 2-related arrhythmogenic cardiomyopathy with Italian cohort validation. Commun Med 6, 145 (2026). https://doi.org/10.1038/s43856-026-01416-w
Palabras clave: miocardiopatía arritmogénica, desmogleína-2, enfermedad cardíaca hereditaria, riesgo genético, muerte súbita cardíaca