Clear Sky Science · es
Bloqueo selectivo de la activación latente de TGF-β1 suprime la fibrosis tisular con buena seguridad
Por qué importa la cicatrización oculta
Muchas enfermedades crónicas dañan silenciosamente nuestros órganos al depositar tejido cicatricial rígido, un proceso llamado fibrosis. Esta cicatrización puede estrangular lentamente la función normal del hígado, los riñones, los pulmones e incluso alrededor de los tumores, donde también puede reducir la eficacia de las inmunoterapias modernas contra el cáncer. La proteína TGF-β1 está en el centro de este proceso de cicatrización, pero apagarla en todo el cuerpo ha demostrado ser peligroso. Este estudio describe un nuevo anticuerpo, llamado SOF10, diseñado para bloquear solo la activación dañina de TGF-β1 preservando sus funciones esenciales, y que muestra beneficios prometedores en modelos animales de enfermedad hepática, insuficiencia renal y cáncer.
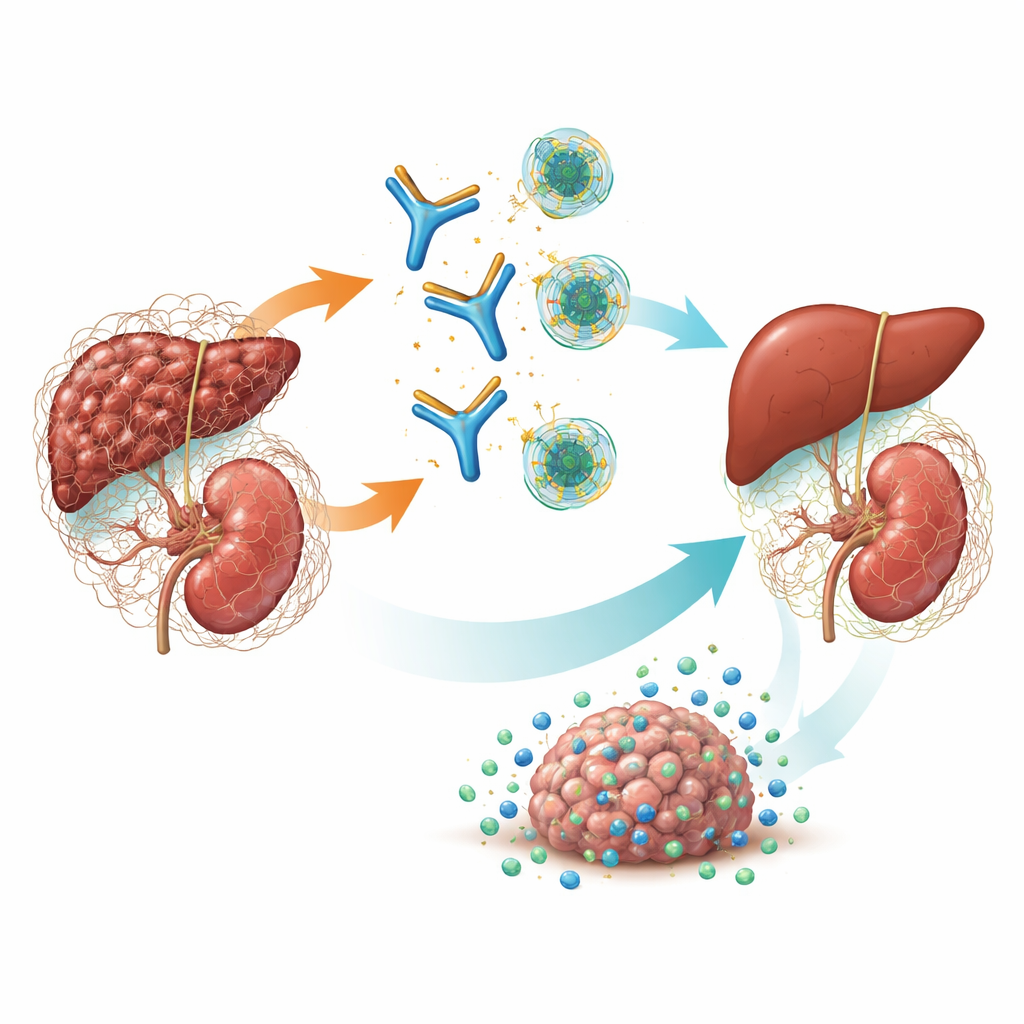
Un interruptor maestro para la cicatrización y el cáncer
TGF-β es una molécula de señalización potente que ayuda a controlar cómo crecen las células, se curan e interactúan con el sistema inmunitario. En la enfermedad crónica, una forma—TGF-β1—impulsa a los fibroblastos a construir tejido conectivo en exceso, lo que conduce al endurecimiento y fallo de los órganos. También conforma una cubierta fibrótica e inmunosupresora alrededor de los tumores que impide que las células inmunitarias y los fármacos alcancen las células cancerosas. Fármacos anteriores intentaron bloquear las tres formas de TGF-β a la vez, pero este “bloqueo pan-TGF-β” provocó efectos secundarios graves como daño de las válvulas cardíacas, hemorragias y tumores cutáneos. Estudios genéticos y modelos previos sugirieron que TGF-β1 es el principal culpable en la fibrosis renal y en muchos tumores sólidos, lo que planteó la posibilidad de que apuntar cuidadosamente solo a esta isoforma pudiera ser eficaz y más seguro.
Bloquear TGF-β1 en su forma inactiva
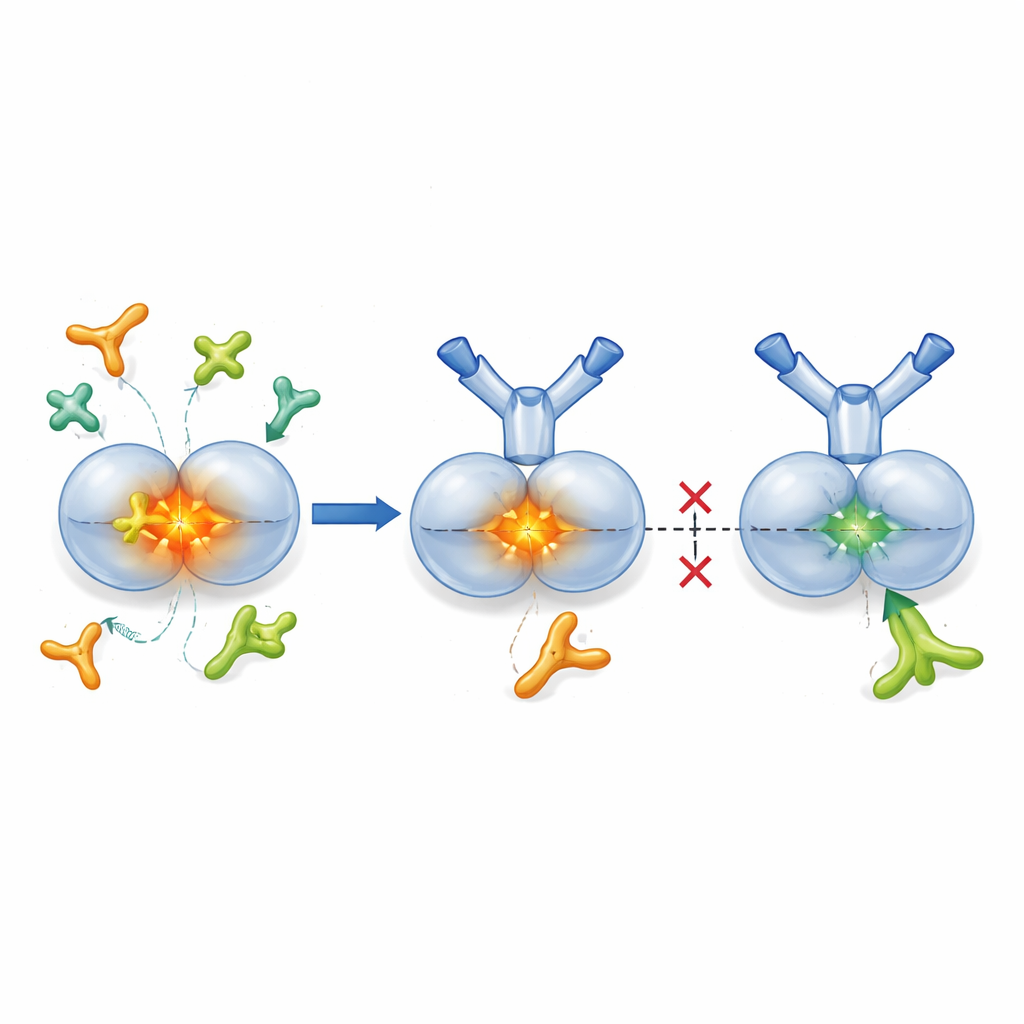
TGF-β1 se produce normalmente en un paquete “latente”, donde el núcleo activo está envuelto por una proteína compañera que lo mantiene inactivo hasta que se necesita. Enzimas llamadas proteasas y ciertas proteínas de la superficie celular conocidas como integrinas pueden abrir este paquete, liberando TGF-β1 activo en el tejido cercano. Los investigadores diseñaron SOF10, un anticuerpo humanizado que se une solo a la forma latente de TGF-β1, no a la hormona activa ni a otras isoformas. Estudios estructurales mediante cristalografía de rayos X mostraron que SOF10 se interpone en la interfaz entre las dos mitades del complejo latente, estabilizándolo como una abrazadera. En pruebas de laboratorio, esto impidió que las proteasas y una integrina (αvβ8) liberaran TGF-β1 activo, pero dejó en gran medida intacta a otra integrina (αvβ6)—importante para mantener el equilibrio inmunitario en tejidos sanos. En efecto, SOF10 silencía de forma selectiva las rutas de activación dañinas mientras preserva una vía homeostática clave.
Protección del hígado y los riñones frente al daño lento
Para comprobar si esta abrazadera selectiva sobre TGF-β1 podía limitar realmente la cicatrización, el equipo probó SOF10 en varios modelos de ratón. En un modelo rápido de dieta que induce enfermedad hepática grasa y progresa a fibrosis hepática, el tratamiento con SOF10 redujo la expresión hepática de genes sensibles a TGF-β y de genes de síntesis de colágeno, y disminuyó la hidroprolina, un marcador químico de acumulación de tejido cicatricial. En dos modelos diferentes de riñón—un modelo de obstrucción quirúrgica que induce fibrosis intersticial y un modelo genético del síndrome de Alport que desarrolla tanto cicatrización glomerular como insuficiencia renal—SOF10 redujo la actividad de genes fibróticos, disminuyó el contenido de colágeno y redujo visiblemente las áreas cicatrizadas al microscopio. En el modelo crónico de Alport, las pruebas sanguíneas mostraron una función renal mejorada, y estos beneficios fueron comparables a los de un anticuerpo de bloqueo más amplio de TGF-β, pero sin bloquear otras isoformas de TGF-β.
Liberar el sistema inmunitario dentro de los tumores
Dado que el tejido fibrótico alrededor de los tumores puede actuar tanto como una barrera física como un freno inmunitario, los investigadores preguntaron si SOF10 podía mejorar las respuestas a los fármacos inhibidores de puntos de control. En modelos murinos de cáncer de mama y de colon que normalmente responden mal a la terapia anti–PD-L1, añadir SOF10 ralentizó de forma significativa el crecimiento tumoral, mientras que SOF10 o anti–PD-L1 por separado tuvieron poco efecto. Los tumores de animales tratados con la combinación contenían más células T CD8 citotóxicas y más de las enzimas tóxicas que utilizan para destruir células cancerosas. Los fibroblastos extraídos de estos tumores mostraron menor actividad en vías de síntesis de colágeno y matriz pero mayor actividad en vías de interferón y presentación de antígeno, un cambio hacia un estroma más favorable para la respuesta inmune. Estos cambios reflejaron de cerca lo observado con el bloqueo amplio de TGF-β, lo que sugiere que apuntar solo al TGF-β1 latente puede reprogramar el microambiente tumoral de manera similar.
Señales de seguridad en animales
Puesto que intentos anteriores de bloquear TGF-β de forma amplia toparon con problemas de seguridad, el equipo realizó estudios de toxicidad de 13 semanas en ratones y monos cynomolgus, administrando dosis altas repetidas de SOF10. El fármaco se comportó como un anticuerpo típico en el torrente sanguíneo y, en un amplio rango de dosis, no hubo señales de daño en órganos principales, recuentos celulares sanguíneos ni en la función cardíaca y pulmonar. Las dosis más altas probadas—hasta 200 mg/kg cada dos semanas en ratones y 100 mg/kg en monos—se designaron como niveles sin efectos adversos observados. Este perfil de seguridad respalda la idea de que preservar TGF-β2, TGF-β3 y la activación mediada por αvβ6 reduce los riesgos observados con enfoques anteriores menos selectivos.
Qué podría significar esto para los pacientes
En conjunto, los hallazgos sugieren que bloquear TGF-β1 en su envoltura inactiva—en lugar de eliminar toda la señalización de TGF-β—puede aliviar la cicatrización en múltiples órganos, mejorar la función renal y hacer que tumores resistentes sean más vulnerables a la inmunoterapia, todo ello con una seguridad alentadora en pruebas animales. Aunque serán necesarios ensayos en humanos para confirmar estos beneficios y monitorizar efectos a largo plazo, SOF10 y estrategias similares podrían abrir una nueva vía para tratar enfermedades fibróticas crónicas y ciertos cánceres, reduciendo la cicatrización dañina mientras se preservan los roles de curación y equilibrio inmunitario que los tejidos aún requieren.
Cita: Kanamori, M., Sato, I., Koo, C.X. et al. Selective blockade of latent TGF-β1 activation suppresses tissue fibrosis with good safety. Commun Med 6, 131 (2026). https://doi.org/10.1038/s43856-026-01408-w
Palabras clave: fibrosis, TGF-beta1, anticuerpo monoclonal, enfermedad renal y hepática, inmunoterapia contra el cáncer