Clear Sky Science · es
Pembrolizumab y modificación epigenética con azacitidina remodelan el microambiente tumoral del cáncer de ovario epitelial resistente a platino: un ensayo clínico de fase 2 no aleatorizado
Por qué importa este estudio
Para muchas mujeres con cáncer de ovario avanzado, la quimioterapia estándar deja de funcionar con el tiempo, lo que deja pocas opciones eficaces. Este estudio explora una estrategia nueva: combinar un tratamiento basado en el sistema inmune con un fármaco que puede “reprogramar” las células cancerosas, con la esperanza de convertir un tumor silencioso y difícil de detectar en uno que el sistema inmune pueda reconocer y atacar. Saber si este enfoque es seguro, cuánto controla el crecimiento tumoral y qué cambios induce dentro de los tumores podría orientar tratamientos futuros para uno de los cánceres ginecológicos más letales.
Una forma de cáncer de ovario difícil de tratar
El cáncer de ovario suele diagnosticarse en estadios avanzados y muchos tumores desarrollan resistencia a un fármaco quimioterápico clave, el platino. Cuando eso ocurre, las respuestas a quimioterapias posteriores suelen ser de corta duración. Los fármacos que liberan los frenos del sistema inmune, los inhibidores de puntos de control, han transformado el tratamiento en varios otros cánceres, pero han mostrado un éxito modesto en el cáncer de ovario. Una razón es que muchos tumores ováricos son “fríos”: contienen relativamente pocas células inmunes activas, lo que dificulta la eficacia de los inhibidores de puntos de control. Los investigadores de este ensayo se preguntaron si podrían “calentar” estos tumores alterando primero cómo se activan o silencian los genes dentro de las células cancerosas.
Combinar inmunoterapia con un fármaco epigenético
El equipo probó la combinación de pembrolizumab, un inhibidor de puntos de control ampliamente utilizado, con azacitidina oral, un fármaco que modifica las marcas químicas del ADN que ayudan a controlar la actividad génica. Al cambiar esas marcas, la azacitidina puede reactivar genes silenciados y desencadenar señales parecidas a una respuesta antiviral dentro de las células tumorales. En modelos de laboratorio, este tipo de “mimetismo viral” atrae células inmunes hacia tumores previamente silenciosos. En este ensayo clínico de fase II, 34 mujeres con cáncer de ovario epitelial resistente o refractario a platino recibieron pembrolizumab junto con uno de cuatro esquemas de dosificación de azacitidina. Todas tenían enfermedad medible y ya habían pasado por la cirugía y la quimioterapia estándar.
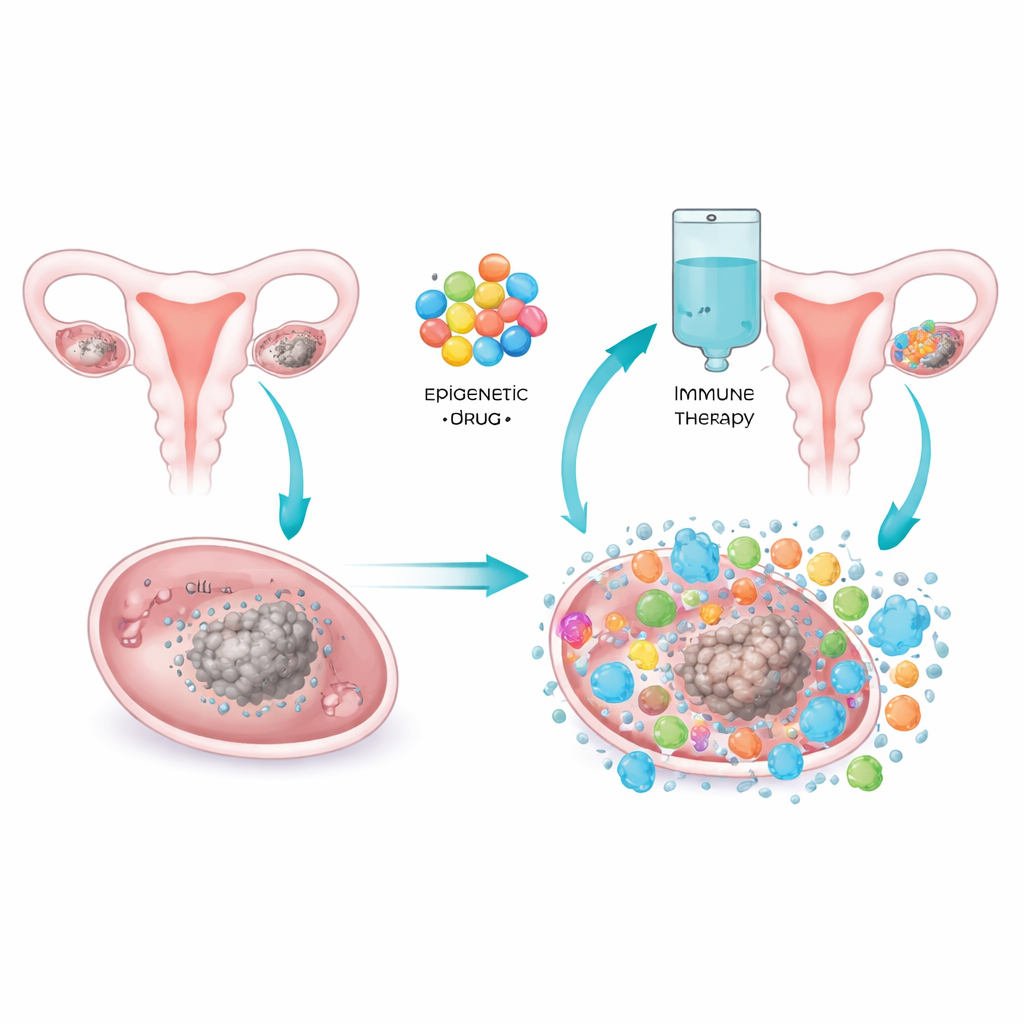
Qué ocurrió en las pacientes
La combinación se consideró moderadamente bien tolerada. Los efectos secundarios comunes incluyeron náuseas, vómitos, diarrea, fatiga, anemia y recuentos bajos de glóbulos blancos, sobre todo con dosis más altas de azacitidina. La mayoría de estos problemas se manejaron con ajustes de dosis, y no surgieron problemas de seguridad inesperados más allá de lo conocido para cada fármaco por separado. En cuanto a la reducción tumoral, solo una paciente experimentó una respuesta parcial y ninguna obtuvo respuesta completa, para una tasa de respuesta global de aproximadamente 3 %. Sin embargo, alrededor de la mitad de las mujeres presentaron reducción tumoral o enfermedad estable, lo que da una tasa de control de la enfermedad del 50 %. Un pequeño número permaneció en tratamiento por más de un año, incluida una mujer que mantuvo la remisión después de pasar a pembrolizumab en monoterapia.
Cómo se remodeló el microambiente tumoral
Para ver qué hacía la combinación dentro de los tumores, los investigadores tomaron muestras de tejido antes del tratamiento y nuevamente alrededor de seis semanas después del inicio de la terapia. Midieron los niveles de actividad de cientos de genes relacionados con la inmunidad y secuenciaron el ARN tumoral para evaluar cambios más amplios. Bajo tratamiento, los tumores mostraron mayor actividad en genes asociados a la inflamación, la señalización de interferones y la maquinaria que presenta fragmentos tumorales a las células inmunes. También se activaron vías que facilitan el movimiento y la adhesión de células inmunes hacia los tumores. Al mismo tiempo, aumentó la proporción de linfocitos T infiltrantes, especialmente del subtipo citotóxico. Estos patrones sugieren que el entorno tumoral pasó de un estado silencioso a otro más inflamado y vigilante inmunológicamente.
Pistas de las respondedores y las huellas de las células inmunes
Los investigadores examinaron también los patrones en las pacientes que mostraron signos de beneficio, ya fuera por descensos en el marcador sanguíneo CA-125 o por un control de la enfermedad más duradero. Los tumores de estas mujeres tendían a mostrar mayor actividad basal en programas génicos inflamatorios y, tras iniciar el tratamiento, exhibieron aumentos más fuertes en respuestas inmunes adaptativas—las mediadas por linfocitos T y B que reconocen objetivos específicos. Reconstruyendo los receptores reordenados de los linfocitos T a partir del ARN tumoral, el equipo observó que las poblaciones de T dentro de los tumores con frecuencia cambiaban bajo el tratamiento, con algunos clonotipos expandiéndose o reduciéndose. Esta remodelación del paisaje de los linfocitos T es otra señal de que la combinación farmacológica estaba reconfigurando activamente la batalla inmune dentro de los tumores.
Qué significa esto para las pacientes
Para las mujeres con cáncer de ovario resistente a platino, esta combinación concreta de pembrolizumab y azacitidina oral no aumentó de forma llamativa el número de tumores que se redujeron en las exploraciones en comparación con la inmunoterapia sola. Sin embargo, controló la enfermedad en alrededor de la mitad de las participantes y produjo señales moleculares claras de que los tumores se volvían más inflamados y más densamente poblados por células inmunes. Para un lector no especializado, la conclusión es que los fármacos parecen capaces de “despertar” el sistema inmune dentro de estos tumores por lo demás silenciosos, aunque eso no siempre se tradujo en reducciones tumorales importantes en este pequeño grupo muy pretratado. Los autores sostienen que refinar las dosis, mejorar la forma de administrar la azacitidina y usar marcadores moleculares para seleccionar a las pacientes con más probabilidad de responder podría convertir esta estrategia de “calentar” el tumor en un bloque de construcción importante para tratamientos futuros del cáncer de ovario.
Cita: Landon, B.V., Boland, J.L., Wahner Hendrickson, A.E. et al. Pembrolizumab and epigenetic modification with azacitidine reshapes the tumor microenvironment of platinum-resistant epithelial ovarian cancer: a phase 2 non-randomized clinical trial. Commun Med 6, 142 (2026). https://doi.org/10.1038/s43856-026-01404-0
Palabras clave: cáncer de ovario, inmunoterapia, terapia epigenética, microambiente tumoral, inhibidores de puntos de control