Clear Sky Science · es
Caracterización genómica y subagrupamiento del complejo clonal 38 de Escherichia coli revelan marcadores genéticos asociados al huésped
Por qué esto importa en la vida cotidiana
Las infecciones resistentes a los antibióticos ya no son un problema lejano limitado a los hospitales: cada vez afectan más a los alimentos, los animales, los viajes y la vida comunitaria. Este estudio se centra en un grupo específico de bacterias Escherichia coli, denominado complejo clonal 38 (CC38), que puede causar infecciones graves en la sangre y el tracto urinario y con frecuencia resiste a nuestros antibióticos más importantes. Al rastrear el origen de estas bacterias y cómo se mueven entre humanos, animales y el medio ambiente, los investigadores revelan pistas que podrían ayudar a las autoridades sanitarias a detener cepas peligrosas antes de que se propaguen ampliamente.
Una mirada más cercana a una familia bacteriana problemática
No todas las E. coli son dañinas, pero algunas líneas son reincidentes en enfermedades graves. CC38 ha emergido recientemente como uno de estos grupos problemáticos, secundario solo a una línea de alto riesgo bien conocida (ST131) en infecciones sanguíneas en Dinamarca. El equipo examinó 242 E. coli CC38 resistentes de pacientes daneses, 83 procedentes de alimentos y animales de granja, y más de 2.300 genomas relacionados recogidos en todo el mundo. Utilizaron secuenciación del genoma completo—esencialmente leer el ADN de cada bacteria—para mapear cómo se relacionan las distintas ramas de esta familia, qué genes de resistencia portan y en qué huéspedes tienden a vivir.
Siguiendo la pista desde hospitales hasta granjas y alimentos
Al comparar E. coli CC38 de pacientes daneses con las procedentes de aves de corral, ganado y alimentos, los investigadores encontraron dos grupos daneses principales. Un grupo estaba formado mayoritariamente por infecciones humanas, mientras que el otro contenía bacterias procedentes de aves, otros animales de granja y productos alimentarios. Es importante destacar que no se hallaron coincidencias de ADN casi idénticas entre aislamientos humanos y animales, lo que sugiere que no hubo brotes transmitidos por alimentos claramente identificables en Dinamarca durante el periodo del estudio. Sin embargo, modelos estadísticos que analizan segmentos de ADN accesorio indicaron que algunos subgrupos asociados a humanos probablemente tienen orígenes avícolas, lo que apunta a derrames pasados o indirectos desde pollos hacia las personas.
Un árbol genealógico global con dos grandes ramas
Al ampliar el conjunto de datos a 2.638 genomas a nivel mundial, el equipo construyó un “árbol genealógico” global para CC38. Destacaron dos ramas principales. Una estaba fuertemente vinculada a las aves de corral y presentaba niveles moderados de resistencia a fármacos junto con muchos rasgos asociados a enfermedad grave. La otra estaba dominada por subgrupos asociados a humanos que diferían en resistencia, potencial patógeno y huéspedes preferentes. Algunos subgrupos eran claramente centrados en humanos y altamente resistentes, mientras que otros mostraron patrones mixtos, apareciendo en humanos, aves, fauna silvestre, agua y animales de compañía. Este mosaico refleja la capacidad de CC38 para adaptarse a distintos entornos y especies huésped, lo que complica los esfuerzos para controlarlo.
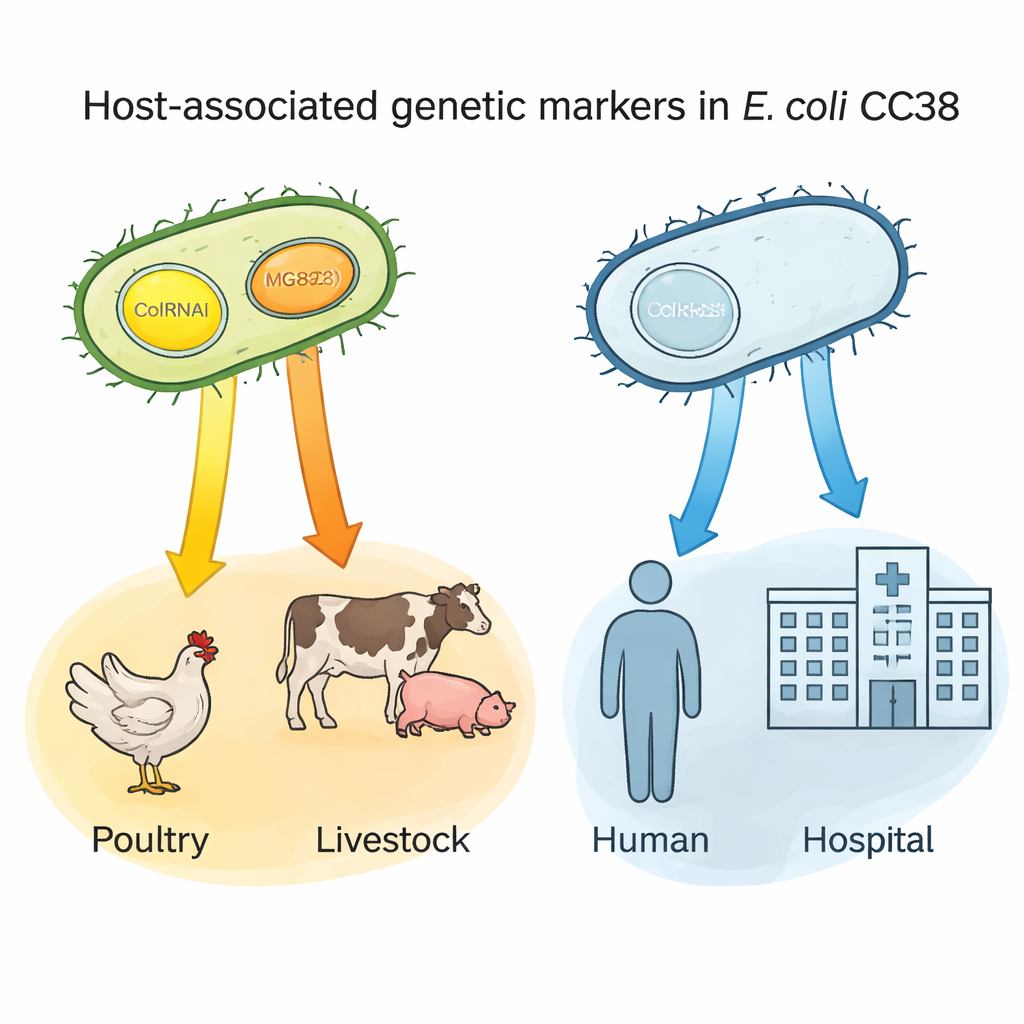
Pequeños círculos de ADN como “etiquetas” del huésped
Un descubrimiento clave implicó dos pequeños fragmentos de ADN—plásmidos llamados ColRNAI y Col(MG828)—capaces de moverse entre bacterias. Estos plásmidos eran comunes en CC38 procedente de aves y otros animales de granja, pero raros en los subgrupos centrados en humanos. Mediante análisis estadístico, los autores demostraron que portar cualquiera de los dos plásmidos predecía con fuerza un origen avícola; portar ambos a la vez era especialmente característico de linajes vinculados al ganado y a ciertas fuentes alimentarias. Como estos plásmidos también suelen portar rasgos de resistencia, pueden actuar como “etiquetas” genéticas que señalan bacterias probablemente procedentes de reservorios animales y pueden ayudar a rastrear cómo las cepas resistentes entran en la cadena alimentaria y alcanzan a las personas.
Qué implica esto para la protección de la salud
Para un público no especialista, el mensaje principal es que las E. coli dañinas y resistentes a los medicamentos no están confinadas a hospitales o pacientes: forman poblaciones interconectadas que abarcan humanos, aves de corral, ganado, fauna silvestre, alimentos y el medio ambiente. Este estudio muestra que dentro de una línea importante, CC38, algunas ramas están fuertemente ligadas a animales y otras a humanos, y que elementos móviles de ADN específicos pueden ayudar a revelar de dónde procede probablemente una cepa. Utilizar estos marcadores genéticos en la vigilancia rutinaria podría ofrecer una alerta temprana cuando bacterias resistentes asociadas a animales empiecen a aparecer en personas. A su vez, esto respalda un enfoque de “Una Sola Salud”—considerar la salud humana, animal y ambiental como partes de un mismo sistema—para diseñar estrategias más inteligentes y dirigidas para prevenir infecciones y frenar la propagación de la resistencia a los antibióticos.
Cita: Roer, L., Rasmussen, A., Hansen, F. et al. Genomic characterization and sub-clustering of Escherichia coli clonal complex 38 reveal host associated genetic markers. Commun Med 6, 126 (2026). https://doi.org/10.1038/s43856-026-01402-2
Palabras clave: resistencia a los antimicrobianos, Escherichia coli, transmisión zoonótica, aves de corral y ganado, vigilancia genómica