Clear Sky Science · es
Predicción del resultado a partir del perfil espacial de proteínas en cánceres de mama triple negativos
Por qué importa la disposición de las células cancerosas
Cuando los médicos observan un cáncer de mama agresivo al microscopio, ven un paisaje abarrotado de células tumorales, células inmunitarias y tejido de soporte. Pero hasta hace poco, la mayoría de las pruebas se han centrado en cuánto de una molécula concreta está presente, no en dónde se localiza. Este estudio muestra que la disposición física de proteínas y células dentro de los cánceres de mama triple negativos puede predecir el pronóstico de los pacientes, e introduce una nueva forma de leer esos patrones espaciales directamente a partir de imágenes de alta resolución.
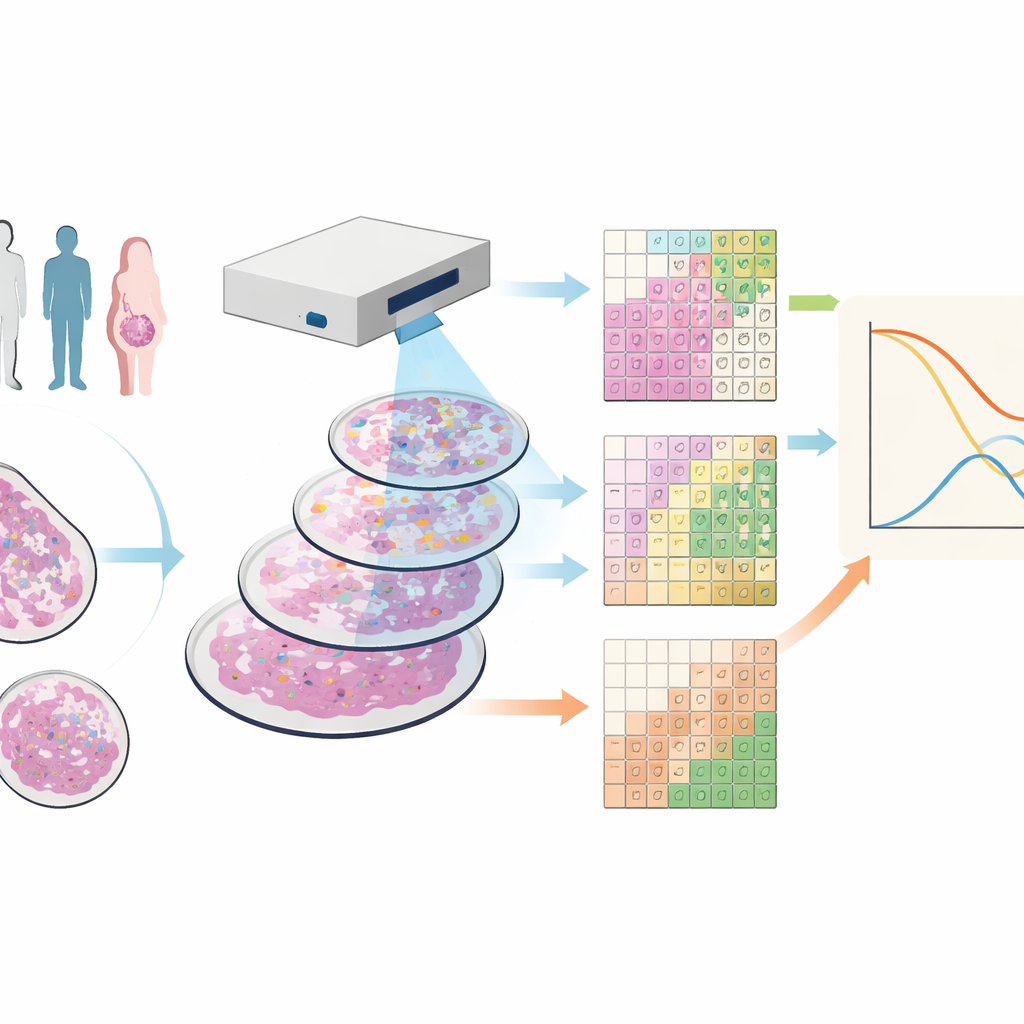
Ver el tejido canceroso en muchos colores
Los investigadores trabajaron con muestras de tejido de 88 personas con cáncer de mama triple negativo, una forma de la enfermedad que carece de dianas farmacológicas comunes y con frecuencia tiene un pronóstico desfavorable. Emplearon una técnica llamada citometría de masas por imagen, que tiñe cada muestra con docenas de anticuerpos marcados con metales. Bajo un escáner especializado, esto produce imágenes en las que cada punto del tejido tiene una huella detallada de muchas proteínas diferentes, revelando simultáneamente las células tumorales, diversas células inmunitarias, vasos sanguíneos y fibras estructurales.
Dividir la imagen en mosaicos en lugar de en células
La mayoría de las herramientas actuales intentan trazar límites alrededor de cada célula y luego clasificarlas por tipo, un proceso que puede ser propenso a errores y lento, especialmente en cortes de tejido finos donde las células solo se capturan parcialmente. El equipo creó en su lugar SparTile, un método que evita dibujar contornos celulares individuales. SparTile corta cada imagen en muchos cuadrados pequeños y solapados, o mosaicos, y utiliza técnicas matemáticas para aprender patrones recurrentes de combinaciones de proteínas dentro de esos mosaicos. Primero agrupa los mosaicos en regiones amplias —tumor, tejido de soporte (estroma) o zonas ricas en células inmunitarias— y luego divide cada región en “microambientes” más específicos, cada uno con su propia mezcla de proteínas y tipos celulares vecinos.
Barrios ocultos vinculados al resultado de los pacientes
Con esos microambientes cartografiados, los científicos midieron cuánto de cada patrón aparecía en la muestra de cada paciente y lo compararon con la supervivencia a largo plazo. Surgieron varios vínculos llamativos. Un microambiente centrado en el tumor, rico en una proteína llamada MX1 y marcadores de células inmunitarias mieloides, se asoció con un riesgo de muerte mucho mayor. Otro patrón tumoral marcado por vimentina —un indicador de que las células tumorales han pasado a un estado más móvil e invasivo— también se relacionó fuertemente con una supervivencia pobre. En contraste, las áreas dominadas por ciertos linfocitos T se vinculaban con mejores resultados, mientras que las regiones ricas en células B mostraron efectos más débiles, posiblemente porque eran raras en los pequeños núcleos de tejido analizados.
La distancia entre células tumorales e inmunitarias como señal de advertencia
Más allá de la mera presencia de vecindarios concretos, sus relaciones espaciales también importaron. El equipo midió qué tan próximas estaban las regiones tumorales y las regiones mieloides inmunes calculando una medida estadística de cuánto se solapaban sus señales proteicas en el espacio. Los pacientes cuyos tumores tenían zonas ricas en células mieloides integradas entre las células tumorales tendieron a tener un peor pronóstico que aquellos en los que las dos poblaciones estaban más separadas. Esta medida de “distancia” se mantuvo como un fuerte predictor de riesgo incluso tras ajustar por factores clínicos estándar, y su importancia se confirmó al probarla en dos conjuntos de imágenes de cáncer de mama independientes de otros grupos de investigación.
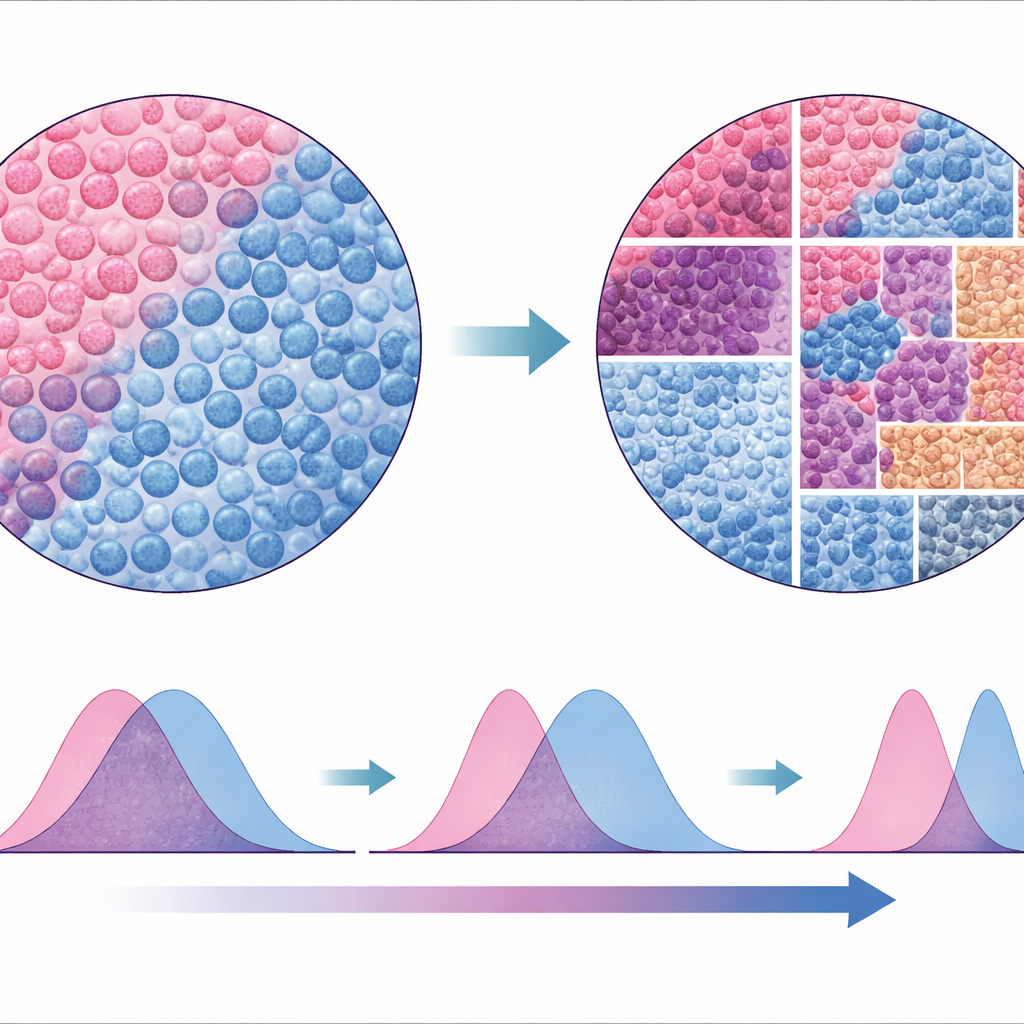
Una nueva forma de leer el paisaje tumoral
Para evaluar la solidez de su enfoque, los autores compararon SparTile con métodos tradicionales que dependen de segmentar y clasificar células individuales y luego construir vecindarios alrededor de ellas. Si bien los análisis basados en células recuperaron algunos de los mismos patrones, fueron menos consistentes entre conjuntos de datos y menos fiables a la hora de identificar ciertos microambientes de riesgo, como los que involucran MX1 y células mieloides. Como SparTile trabaja directamente sobre las imágenes crudas de proteínas, evita muchas de las suposiciones y trampas técnicas de los enfoques célula por célula, aunque todavía puede combinarse con ellos después cuando se necesiten tipos celulares detallados para diseñar experimentos o terapias.
Qué significa esto para los pacientes y la atención futura
Este trabajo demuestra que no solo importan los componentes, sino también la disposición de un tumor para predecir el devenir de un paciente con cáncer de mama triple negativo. Al convertir imágenes complejas multoproteína en patrones espaciales interpretable y medidas de distancia sencillas, SparTile ofrece una forma de identificar pacientes de alto riesgo a partir de pequeñas muestras de tejido y de descubrir disposiciones biológicas que podrían dirigirse con tratamientos futuros. Aunque se necesita más validación antes de que pueda guiar la atención de rutina, el enfoque apunta a un futuro en el que el “mapa” de un tumor sea tan importante como su lista de partes moleculares.
Cita: Foroughi pour, A., Wu, TC., Noorbakhsh, J. et al. Prediction of outcome from spatial Protein profiling of triple-negative breast cancers. Commun Med 6, 133 (2026). https://doi.org/10.1038/s43856-026-01400-4
Palabras clave: cáncer de mama triple negativo, microambiente tumoral, proteómica espacial, citometría de masas por imagen, biomarcadores pronósticos