Clear Sky Science · es
IdentifiHR predice la deficiencia de recombinación homóloga en carcinoma seroso de alto grado mediante la expresión génica
Por qué esta investigación importa para las pacientes con cáncer de ovario
Para las personas con carcinoma seroso de alto grado, una de las formas más letales de cáncer de ovario, las decisiones de tratamiento pueden ser cuestión de vida o muerte. Aproximadamente la mitad de estos tumores presentan una debilidad en la forma de reparar el ADN dañado, lo que los hace especialmente sensibles a ciertos fármacos llamados inhibidores de PARP. El reto es determinar, en cada paciente, si su tumor tiene esa vulnerabilidad. Este estudio presenta IdentifiHR, una nueva herramienta que interpreta patrones de actividad génica, en lugar de solo mutaciones en el ADN, para predecir qué tumores tienen una reparación del ADN defectuosa y podrían beneficiarse más de estos tratamientos dirigidos.
De las cicatrices del ADN a los patrones de actividad génica
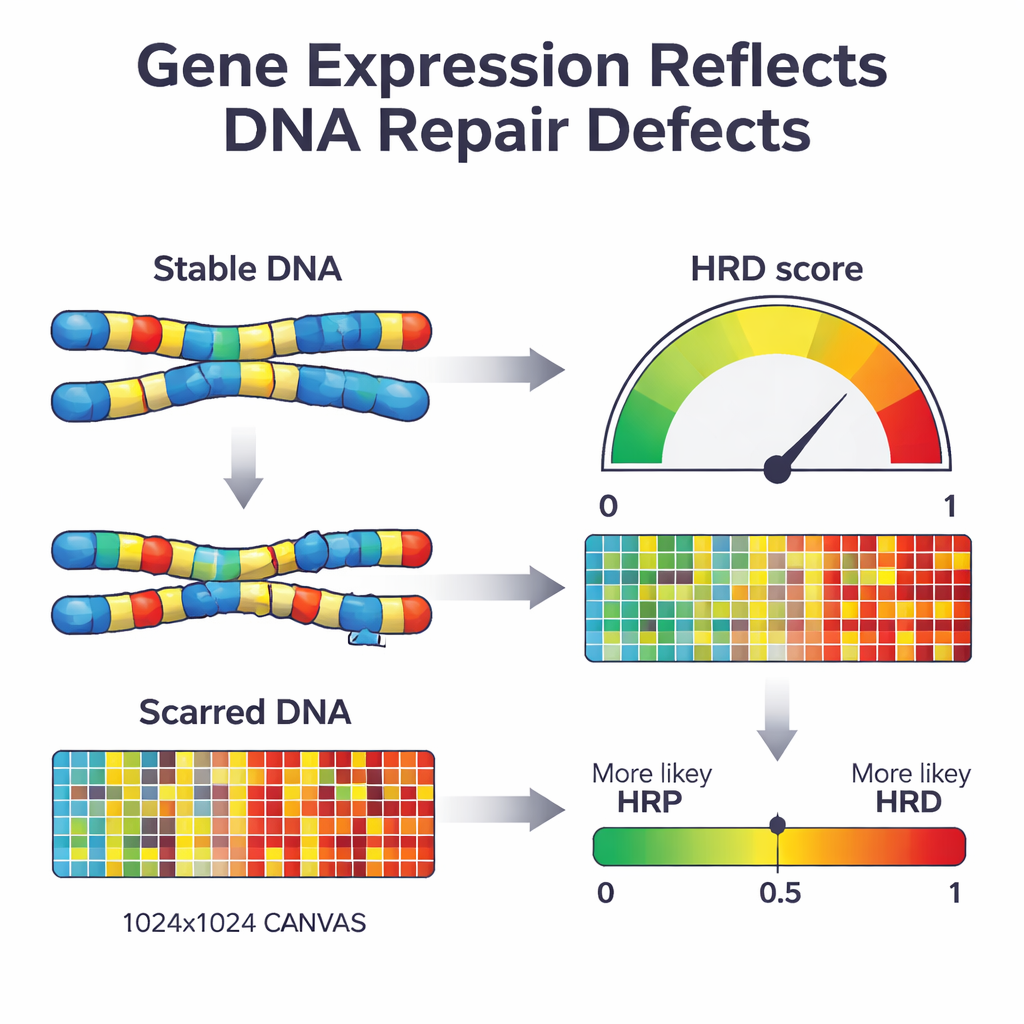
Cuando una célula pierde una vía importante de reparación llamada recombinación homóloga, comienza a parchear su ADN usando métodos más propensos al error. Con el tiempo esto deja un patrón característico de “cicatrices” en todo el genoma: regiones desaparecidas, copias extra y fragmentos cromosómicos rotos. Las pruebas clínicas actuales buscan estas cicatrices directamente en el ADN o mutaciones específicas en genes clave como BRCA1 y BRCA2. Aunque son potentes, estas pruebas requieren una secuenciación extensa del ADN y no siempre capturan el estado actual de reparación del tumor. Los autores se preguntaron si una capa diferente de la biología—el patrón de genes activados o silenciados en el tumor—podría actuar como una lectura en tiempo real de este daño y usarse para clasificar los tumores como deficientes o competentes en reparación.
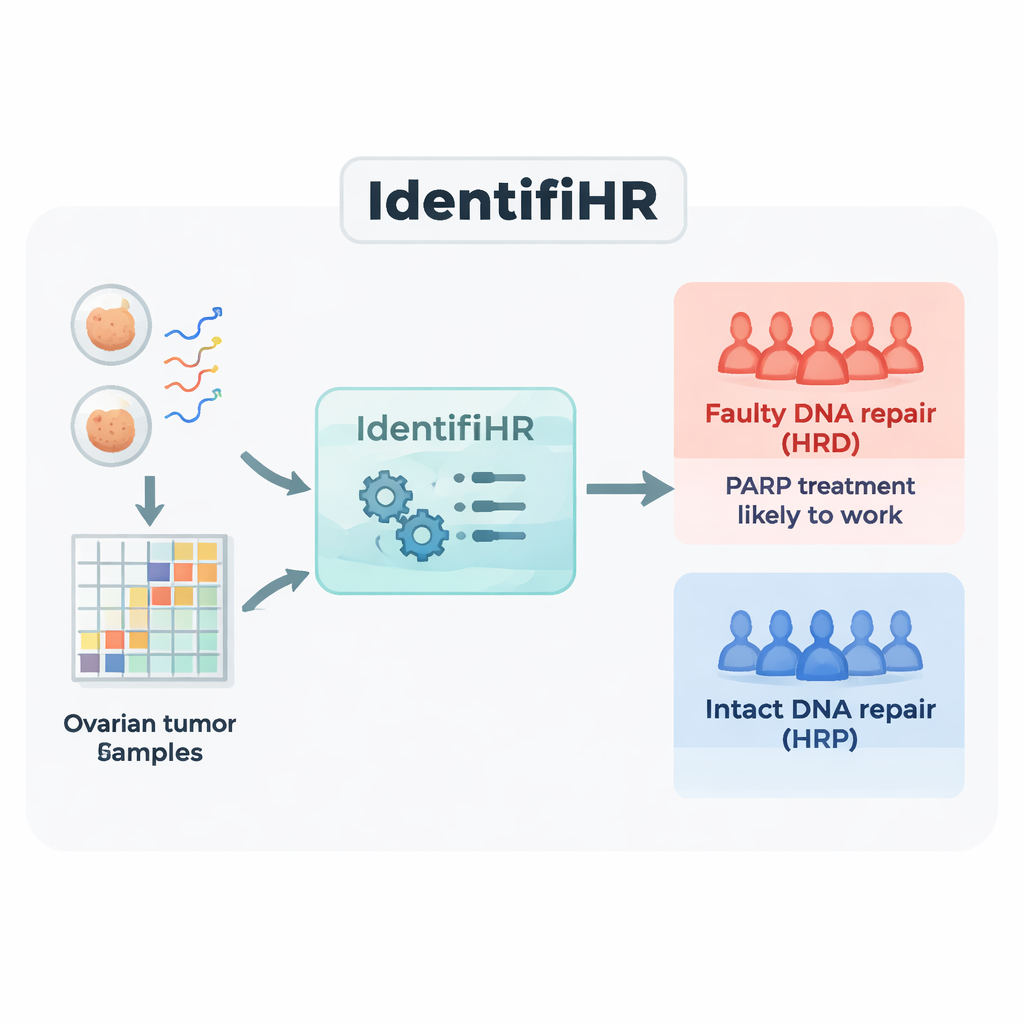
Construyendo un predictor basado en genes, IdentifiHR
El equipo partió de datos de secuenciación de ARN de 361 tumores ováricos de un gran recurso público, The Cancer Genome Atlas. La secuenciación de ARN mide qué genes están activos y en qué grado en cada muestra. Dividieron los tumores en un grupo de entrenamiento y otro de prueba, etiquetando cada caso como deficiente en reparación (HRD) o competente en reparación (HRP) usando el estándar actual basado en ADN que combina varias medidas de cicatrices genómicas. En los tumores de entrenamiento identificaron 2.604 genes cuya actividad difería de forma consistente entre cánceres HRD y HRP. Muchos de estos genes se ubicaban en regiones del genoma ya conocidas por perderse o ganarse repetidamente en tumores con defectos de reparación, lo que muestra que la señal de expresión génica refleja el daño subyacente en el ADN.
Una firma de 209 genes que rastrea el estado de reparación
A continuación, los investigadores usaron un enfoque de aprendizaje automático conocido como regresión logística penalizada para reducir esta lista de 2.604 genes al conjunto más informativo. El modelo resultante, al que llamaron IdentifiHR, se basa en la actividad de solo 209 genes para estimar la probabilidad de que un tumor sea deficiente en reparación. Curiosamente, solo uno de estos genes es un gen clásico de reparación del ADN; la mayoría son genes corrientes cuya actividad está alterada debido a cambios más amplios en la estructura cromosómica. IdentifiHR no entrega simplemente una etiqueta sí/no: produce una puntuación de probabilidad que se correlaciona de forma continua con la puntuación de daño basada en el ADN, reflejando la idea de que la deficiencia de reparación existe en un espectro más que como un estado binario.
Probando la herramienta en múltiples cohortes de pacientes
Los autores probaron rigurosamente IdentifiHR en tres conjuntos de datos independientes que no se habían usado en el entrenamiento. En el subconjunto retenido de The Cancer Genome Atlas, el modelo distinguió correctamente tumores HRD de HRP en alrededor del 85% de los casos. Rindió igual de bien—aproximadamente un 86% de precisión—en un estudio australiano separado que incluía no solo tumores primarios, sino también muestras obtenidas en autopsia, de líquido abdominal (ascitis) y de trompas de Falopio normales, el probable sitio donde comienzan muchos de estos cánceres. En cada muestra de trompa de Falopio normal, IdentifiHR predijo correctamente reparación del ADN intacta. La herramienta también funcionó en datos de células individuales “seudobulkeadas”, donde miles de células cancerosas individuales se combinaron computacionalmente para imitar una muestra a granel, alcanzando de nuevo cerca del 84% de precisión. En estas pruebas, IdentifiHR igualó o superó el rendimiento de varios métodos existentes basados en genes desarrollados originalmente para otros cánceres o para predecir puntuaciones de daño relacionadas.
Cómo esto podría cambiar la investigación y la atención clínica
Porque IdentifiHR funciona con datos de ARN, que a menudo son más baratos y fáciles de obtener que los perfiles de ADN de genoma completo, ofrece una vía práctica para que los investigadores—y potencialmente, en el futuro, los clínicos—estimen el estado de reparación del ADN cuando solo hay datos de expresión génica disponibles. El modelo se publica como un paquete R de código abierto, de modo que cualquier grupo con datos de secuenciación adecuados puede aplicarlo. Aunque todavía no reemplaza a las pruebas de referencia basadas en ADN y su capacidad para captar cambios más sutiles, como la restauración de la reparación, requiere más estudio, IdentifiHR proporciona una nueva y potente lente para identificar qué tumores ováricos son más propensos a responder a inhibidores de PARP y fármacos similares. Para las pacientes, este trabajo acerca el campo a decisiones de tratamiento más precisas y guiadas por la biología real del comportamiento de sus células cancerosas.
Cita: Weir, A.L., Lee, S.C., Li, M. et al. IdentifiHR predicts homologous recombination deficiency in high-grade serous ovarian carcinoma using gene expression. Commun Med 6, 119 (2026). https://doi.org/10.1038/s43856-026-01387-y
Palabras clave: cáncer de ovario, reparación del ADN, deficiencia de recombinación homóloga, expresión génica, aprendizaje automático