Clear Sky Science · es
Deficiencia de recombinación homóloga en cáncer de mama primario ER‑positivo y HER2‑negativo
Por qué esto importa para las pacientes con cáncer de mama
La mayoría de los cánceres de mama pertenecen a un gran grupo denominado receptores de estrógeno positivos y HER2 negativos. Estos tumores suelen tratarse con fármacos que bloquean las hormonas, a veces combinados con quimioterapia. Aun así, muchas pacientes recaen y los médicos carecen de herramientas precisas para decidir quién necesita realmente tratamientos intensivos o podría beneficiarse de nuevos fármacos dirigidos. Este estudio explora una debilidad específica en algunos tumores —llamada deficiencia de recombinación homóloga, o HRD por sus siglas en inglés— que impide a las células cancerosas reparar con eficacia el ADN roto, abriendo potencialmente la puerta a un tratamiento más personalizado.
Una debilidad oculta en solo algunos tumores
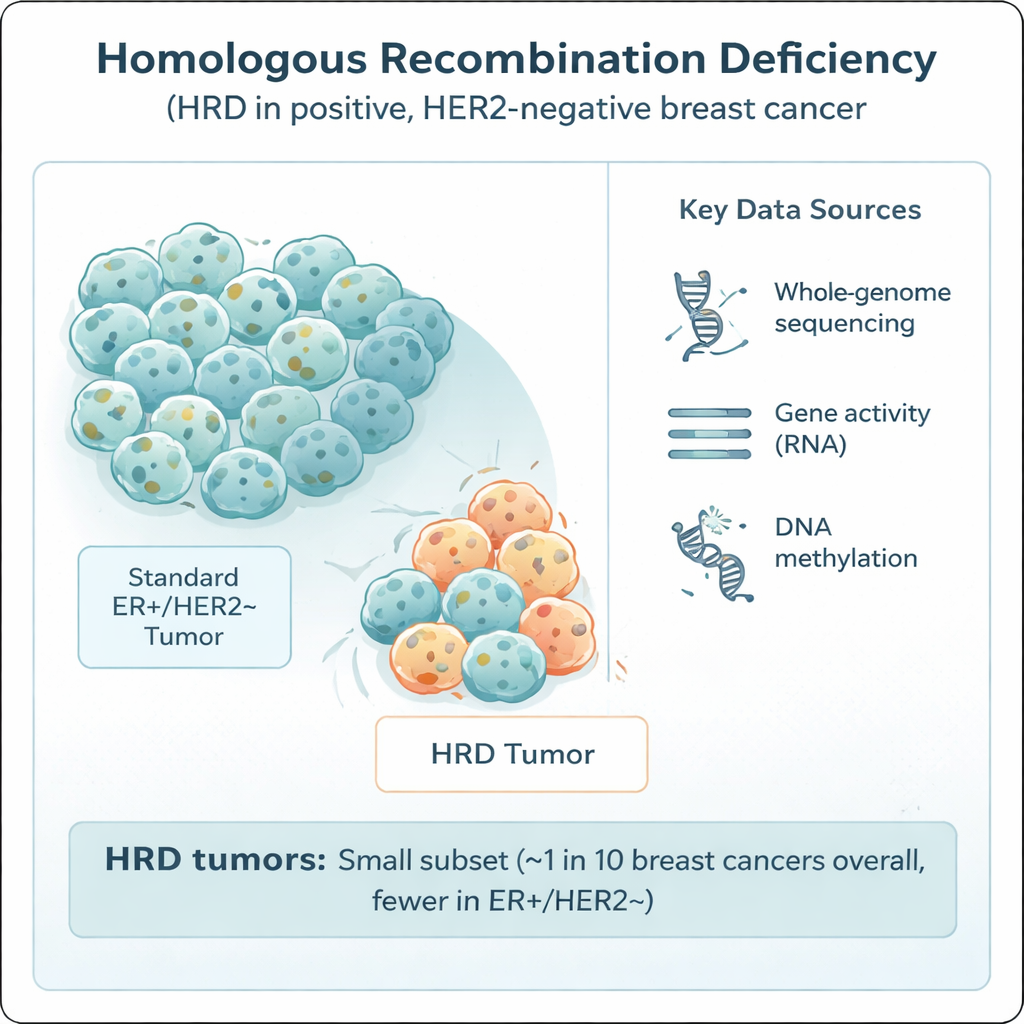
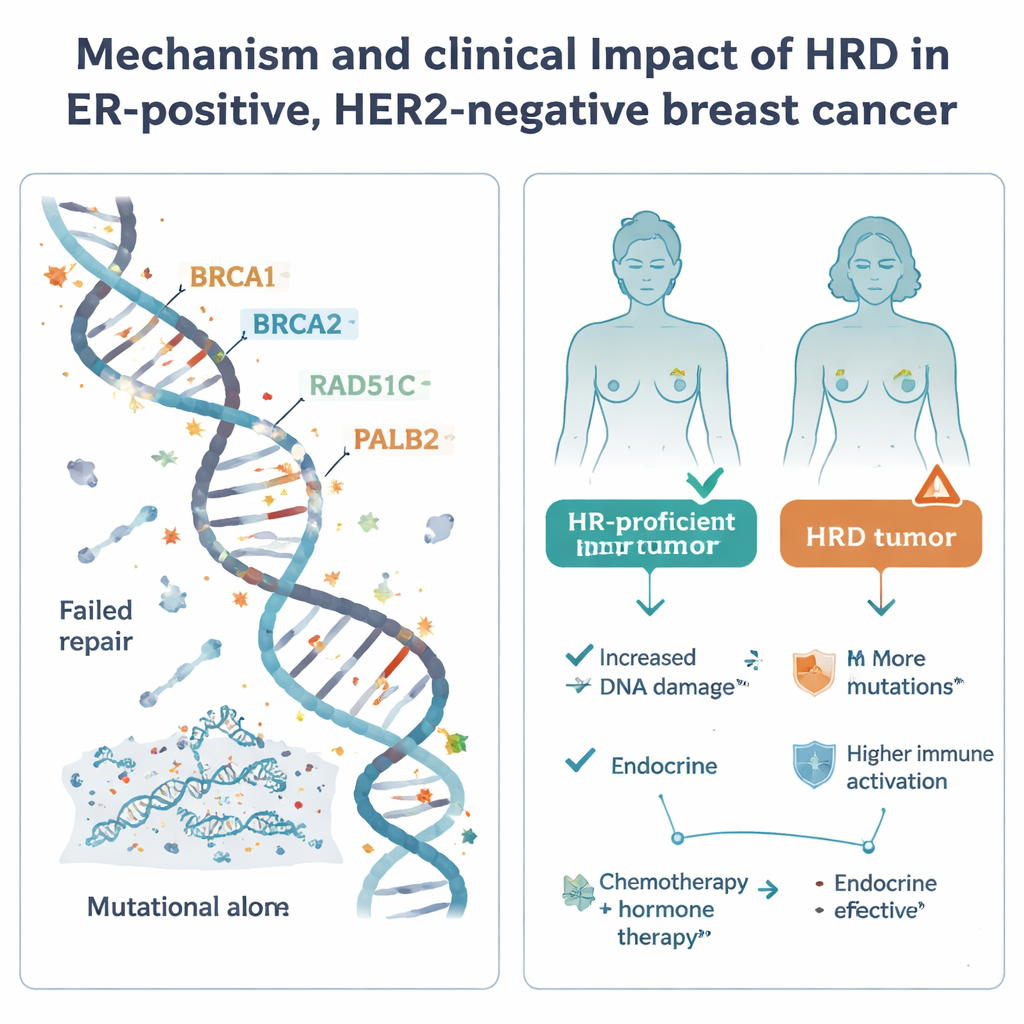
La recombinación homóloga es uno de los principales sistemas celulares para reparar roturas peligrosas del ADN. Cuando este sistema falla —a menudo por defectos en genes bien conocidos como BRCA1, BRCA2, PALB2 o RAD51C— las células acumulan mutaciones y pueden volverse especialmente sensibles a ciertos fármacos, incluidos agentes de platino y los inhibidores de PARP. La HRD es común en una forma agresiva de cáncer de mama llamada triple negativo, pero su papel en el grupo más habitual ER‑positivo y HER2‑negativo ha sido incierto. Para aclararlo, los investigadores analizaron 502 tumores de este tipo procedentes del estudio sueco SCAN‑B mediante secuenciación del genoma completo, junto con datos emparejados sobre la actividad génica, metilación del ADN, tratamientos recibidos y resultados a largo plazo.
Cómo se realizó el estudio
Todos los tumores se recogieron en el momento de la cirugía, antes de cualquier tratamiento farmacológico, lo que proporciona una instantánea clara de su biología original. El equipo utilizó una herramienta sofisticada de reconocimiento de patrones, HRDetect, para leer las “firmas mutacionales” que quedan en el ADN canceroso cuando la recombinación homóloga está rota. Los tumores se etiquetaron como HRD si superaban un umbral estricto de probabilidad. Los científicos también compararon distintas formas de detectar HRD —desde otros puntajes basados en ADN hasta una prueba de expresión génica basada en ARN— para ver con qué fiabilidad coinciden los distintos métodos. Además, examinaron características más amplias como la carga mutacional global, los patrones de ganancias y pérdidas cromosómicas, la actividad génica relacionada con la respuesta inmune y las marcas químicas en el ADN (metilación) que pueden activar o silenciar genes.
¿Qué tan común es la HRD y qué la provoca?
Los investigadores hallaron que solo el 8,4 % de los tumores ER‑positivo, HER2‑negativo en su cohorte secuenciada mostraron evidencia sólida de HRD —muy por debajo del aproximadamente 60 % observado en la enfermedad triple negativa. Combinando estos datos con información de registros nacionales y otros estudios, estimaron que alrededor de 1 de cada 20 tumores en este subgrupo clínico, y aproximadamente 1 de cada 9 cánceres de mama en poblaciones de Europa occidental/Nórdicas, presentan HRD. En los tumores HRD pudieron a menudo identificar una causa probable: cerca del 70 % tenía daño claro en BRCA1, BRCA2, RAD51C o PALB2, mediante mutaciones heredadas, mutaciones o deleciones específicas del tumor, o silenciamiento epigenético de promotores génicos. De forma llamativa, alrededor de un tercio de los casos HRD se debieron a hipermetilación de promotores —una capa química adicional que apaga genes de reparación del ADN sin alterar su secuencia. Sin embargo, aproximadamente el 30 % de los tumores HRD no mostraron un único golpe obvio, lo que sugiere rutas adicionales aún por descubrir hacia esta falla de reparación.
Cómo se ven los tumores HRD al microscopio y en la clínica
Los tumores HRD en este grupo común de cáncer de mama tendieron a mostrar señales de enfermedad más agresiva: con frecuencia tenían tasas más altas de división celular, niveles más bajos de tinción de receptores hormonales y genomas más complejos y ricos en mutaciones que los tumores con reparación funcional. Aparecieron en casi todos los grandes subtipos moleculares, pero fueron raros en la clase más indolente Luminal A y relativamente más frecuentes en un subconjunto basal‑like menor. Sin embargo, al analizar la actividad génica global y los patrones de metilación del ADN, los tumores HRD no se agruparon en un perfil único y fácilmente reconocible. En su lugar, sus patrones de expresión fueron diversos y las diferencias dentro de subtipos específicos fueron modestas. Algunos tumores HRD, especialmente en los grupos Luminal B y basal‑like, mostraron señales más altas de actividad inmune y mayor expresión de PD‑L1, lo que sugiere que podrían ser más visibles para el sistema inmunitario y potencialmente más sensibles a la inmunoterapia.
¿La HRD cambia los resultados de las pacientes?
El estudio examinó a continuación cómo se relacionaba el estado HRD con los resultados en el mundo real bajo la atención estándar. En pacientes tratadas solo con terapia hormonal tras la cirugía, los tumores HRD mostraron una tendencia hacia una supervivencia libre de recaída a distancia peor, aunque el número de casos HRD fue pequeño y el resultado no alcanzó significación estadística formal. Este patrón, junto con sus rasgos moleculares agresivos, sugiere que confiar exclusivamente en la terapia endocrina puede ser arriesgado para las pacientes cuyos tumores son HRD. En cambio, entre las pacientes que recibieron tanto quimioterapia como terapia hormonal, el estado HRD no se asoció claramente con mejores o peores resultados; todos los grupos tuvieron tasas de recaída en términos generales similares, y la quimioterapia podría estar mitigando parte del riesgo añadido en los tumores HRD.
Qué significa esto para las decisiones de tratamiento futuras
Para un lector general, el mensaje clave es que solo una minoría de los cánceres de mama ER‑positivo, HER2‑negativo poseen esta debilidad particular en la reparación del ADN, pero cuando está presente suele señalar una enfermedad más agresiva que puede no controlarse bien solo con terapia hormonal. El trabajo respalda la idea de que la secuenciación del genoma completo puede identificar con fiabilidad la HRD y aclarar sus causas subyacentes, más allá de la simple búsqueda de mutaciones hereditarias en BRCA1 o BRCA2. Aunque el estudio aún no demuestra que cambiar el tratamiento según el estado HRD mejore la supervivencia, aporta evidencias iniciales de que las pacientes con tumores HRD podrían beneficiarse de la quimioterapia y, en ensayos futuros, de inhibidores de PARP o inmunoterapias. En resumen, la prueba de HRD podría convertirse en una pieza más de un conjunto de herramientas afinadas para adaptar la intensidad del tratamiento —y las opciones dirigidas novedosas— a la biología del cáncer de mama de cada paciente.
Cita: Davies, H.R., Black, D., Kvist, A. et al. Homologous recombination deficiency in primary ER-positive and HER2-negative breast cancer. Commun Med 6, 118 (2026). https://doi.org/10.1038/s43856-026-01385-0
Palabras clave: cáncer de mama, reparación del ADN, genes BRCA, secuenciación del genoma, terapia dirigida