Clear Sky Science · es
Firma estructural de proteínas plasmáticas clasifica el estado de la enfermedad de Alzheimer
Por qué importa un análisis de sangre para la pérdida de memoria
La enfermedad de Alzheimer suele estar bien avanzada mucho antes de que los problemas de memoria sean evidentes; sin embargo, las pruebas actuales para detectarla temprano pueden ser invasivas, caras o de difícil acceso. Este estudio explora una idea diferente: si pequeños cambios en las formas tridimensionales de las proteínas que circulan en la sangre pueden revelar en qué punto se encuentra una persona en el trayecto desde un envejecimiento sano a un olvido leve y, finalmente, a la enfermedad de Alzheimer. Si tiene éxito, un análisis de sangre así podría facilitar el cribado, permitir tratamientos más tempranos y ayudar a los investigadores a seguir quién se beneficia de nuevas terapias.
Observando la forma de las proteínas, no solo su cantidad
La mayoría de los análisis de sangre miden cuánto de una molécula determinada está presente. Aquí, los científicos se centraron en cambio en la forma de las proteínas. Dentro de nuestras células, un sistema de control de calidad mantiene las proteínas correctamente plegadas; cuando este sistema falla con la edad, las proteínas mal plegadas pueden acumularse y dañar las células cerebrales. El equipo se preguntó si este deterioro en la “gestión doméstica” de las proteínas deja una huella estructural en las proteínas sanguíneas. De 520 voluntarios que estaban cognitivamente sanos, tenían deterioro cognitivo leve (DCL) o padecían Alzheimer, tomaron sangre y usaron una técnica química llamada perfilado covalente de proteínas para marcar las partes expuestas de las proteínas. Cuanto más expuesto está un sitio, más fácilmente se marca, proporcionando una lectura numérica de la forma de la proteína que es en gran medida independiente de la cantidad de proteína presente.
Encontrando huellas estructurales en la sangre
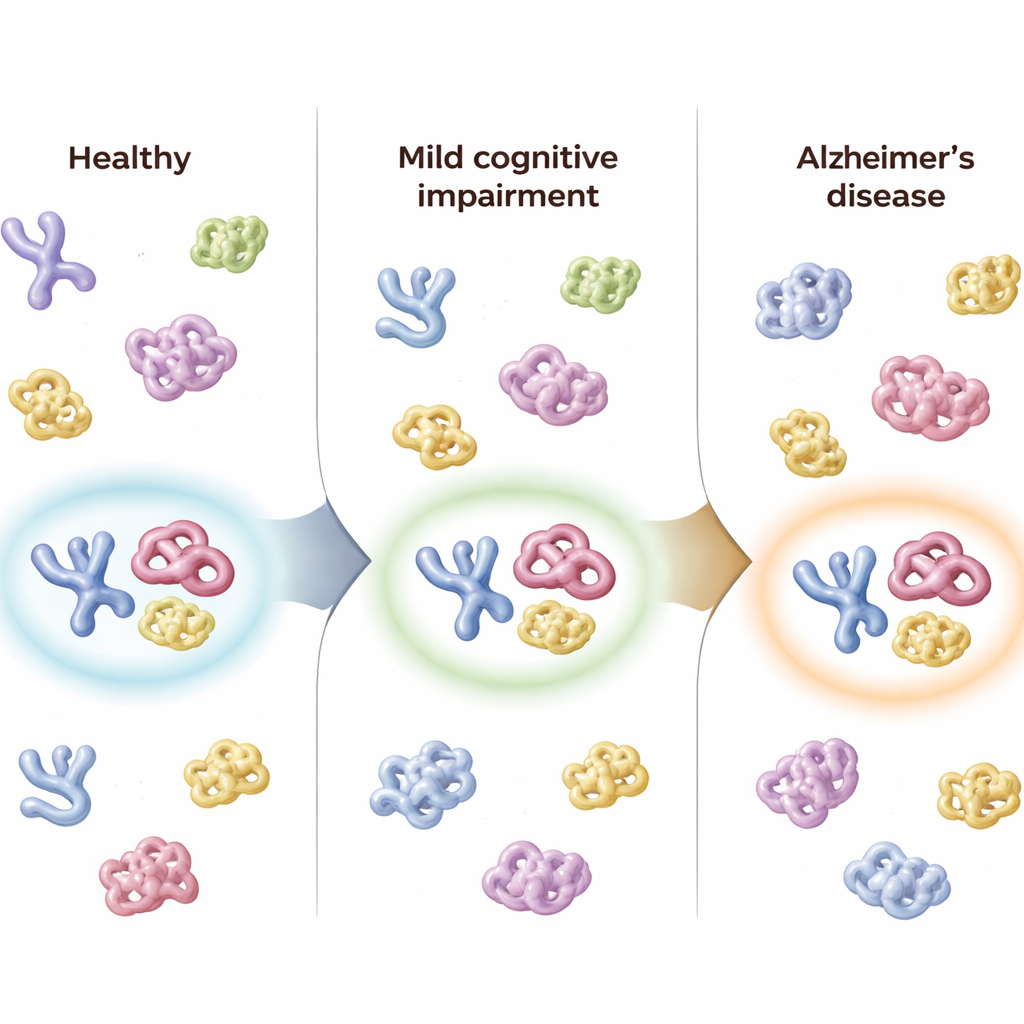
En casi 900 fragmentos proteicos marcados, los investigadores observaron una tendencia sutil pero consistente: a medida que las personas pasaban de sanas a DCL y a Alzheimer, ciertas superficies proteicas se volvían menos expuestas y más variables entre individuos. Este patrón encaja con la idea de que el control del plegamiento de proteínas empeora a medida que avanza la enfermedad. El equipo también examinó cómo un importante factor de riesgo genético para el Alzheimer, la variante APOE ε4, influía en la forma de las proteínas. Encontraron que las personas que portaban dos copias de ε4 mostraban cambios estructurales distintivos en varias proteínas que interactúan con la proteína APOE, lo que sugiere que este gen de riesgo altera no solo qué proteínas están presentes, sino cómo están plegadas y organizadas.
Vinculando las proteínas sanguíneas con el ánimo y el comportamiento
El Alzheimer afecta mucho más que la memoria; síntomas como agitación, depresión y alucinaciones son comunes y con frecuencia difieren entre hombres y mujeres. Los investigadores combinaron las valoraciones clínicas de 12 tipos de síntomas neuropsiquiátricos con sus medidas de forma proteica. En ambos sexos, los síntomas más graves tendían a ir de la mano con proteínas que se volvían estructuralmente más “cerradas”. Algunas proteínas, incluida la clusterina y varias otras vinculadas a la acumulación de amiloide, siguieron la gravedad de los síntomas de forma similar en hombres y mujeres, mientras que otras mostraron patrones específicos por sexo. Estos hallazgos sugieren que la estructura de las proteínas en sangre puede reflejar no solo la presencia de la enfermedad, sino también cómo se manifiesta en el comportamiento y el estado de ánimo.
Un panel de tres proteínas para clasificar la etapa de la enfermedad
Para convertir estas mediciones complejas en algo clínicamente útil, el equipo introdujo los datos estructurales en 18 enfoques distintos de aprendizaje automático. El modelo con mejor rendimiento, basado en aprendizaje profundo, se apoyó en solo tres fragmentos proteicos procedentes de C1QA, clusterina (también llamada CLUS) y apolipoproteína B (ApoB). Usando únicamente las lecturas estructurales de estos tres fragmentos, el modelo clasificó correctamente a las personas como sanas, con DCL o con Alzheimer en aproximadamente el 83 % de las ocasiones en un conjunto de prueba independiente. Al plantear preguntas más sencillas de dos vías —por ejemplo, distinguir sano de DCL, o DCL de Alzheimer—, el rendimiento del panel fue aún mayor, con medidas de precisión comparables o superiores a muchas aproximaciones actuales basadas en cantidades de proteína más que en su estructura.
Seguimiento de personas a lo largo del tiempo
Los investigadores también contaron con muestras de seguimiento de 50 participantes tomadas hasta unos ocho meses después. En las personas cuyo diagnóstico empeoró—por ejemplo, de sano a DCL, o de DCL a Alzheimer—, la puntuación combinada del panel de tres proteínas cambió en la misma dirección, reflejando la progresión de la enfermedad. En contraste, los individuos cuyo estado clínico se mantuvo igual mostraron poco cambio en sus puntuaciones del panel. La puntuación global de “confianza en Alzheimer” del panel se correlacionó estrechamente con pruebas cognitivas estándar, con medidas de funcionamiento diario, con la pérdida de volumen cerebral observada en resonancia magnética y con marcadores establecidos en líquido cefalorraquídeo de amiloide y tau, lo que sugiere que la señal estructural basada en sangre refleja los cambios cerebrales subyacentes.
Qué podría significar esto para los pacientes
En conjunto, el trabajo muestra que pequeños cambios coordinados en las formas de solo unas pocas proteínas abundantes en sangre pueden señalar de manera fiable si una persona está cognitivamente sana, tiene deterioro leve o padece la enfermedad de Alzheimer. Dado que la prueba utiliza sangre en lugar de líquido cefalorraquídeo o imágenes cerebrales, podría, en principio, escalarse para cribados de rutina o para seleccionar y monitorizar participantes en ensayos clínicos. Los autores advierten que se necesitan estudios más amplios y a más largo plazo, y que la química implicada sigue siendo especializada. No obstante, sus resultados señalan a la estructura de las proteínas—no solo a sus niveles—como una nueva y prometedora fuente de información para detectar y seguir la enfermedad de Alzheimer de forma más temprana y precisa.
Cita: Son, A., Kim, H., Diedrich, J.K. et al. Structural signature of plasma proteins classifies the status of Alzheimer’s disease. Nat Aging 6, 597–611 (2026). https://doi.org/10.1038/s43587-026-01078-2
Palabras clave: Biomarcadores de la enfermedad de Alzheimer, análisis de sangre para la demencia, cambios en el plegamiento de proteínas, diagnóstico mediante aprendizaje automático, clusterina y C1QA