Clear Sky Science · es
La resistencia al tratamiento con quimioterapia basada en platino en cáncer de pulmón y ovario está impulsada por un secretoma senescente dependiente de TGFβ y susceptible de ser dirigido
Cuando el tratamiento contra el cáncer resulta contraproducente
La quimioterapia basada en platino es uno de los pilares del tratamiento del cáncer moderno, especialmente en los cánceres de pulmón y de ovario. Su objetivo es dañar el ADN tumoral tan gravemente que las células cancerosas no puedan dividirse. Sin embargo, muchos pacientes ven cómo sus tumores se reducen al principio para después reaparecer, más resistentes que antes. Este estudio plantea una pregunta sencilla pero inquietante: ¿pueden los mismos fármacos que salvan vidas también ayudar a las células cancerosas supervivientes a recuperarse? La respuesta, según los autores, reside en un grupo especial de células dañadas y con rasgos de envejecimiento y en los potentes mensajes químicos que emiten.
La doble vida de las células cancerosas envejecidas
La quimioterapia no trata por igual a todas las células tumorales. Algunas son eliminadas de inmediato, pero otras entran en un estado llamado senescencia celular: detenidas permanentemente en su capacidad de dividirse, pero todavía vivas. Estas células senescentes aumentan de tamaño y comienzan a secretar un cóctel de proteínas y señales conocido como fenotipo secretor asociado a la senescencia, o SASP. Usando células humanas de cáncer de pulmón y ovario en el laboratorio, así como modelos en ratón, los investigadores demostraron que los fármacos con platino como el cisplatino y el carboplatino generan células senescentes especialmente potentes. Cuando células cancerosas recién cultivadas se expusieron al líquido procedente de estos cultivos senescentes, crecieron más rápido, migraron con mayor facilidad y formaron agregados y esferas más grandes y agresivas que las células de control.
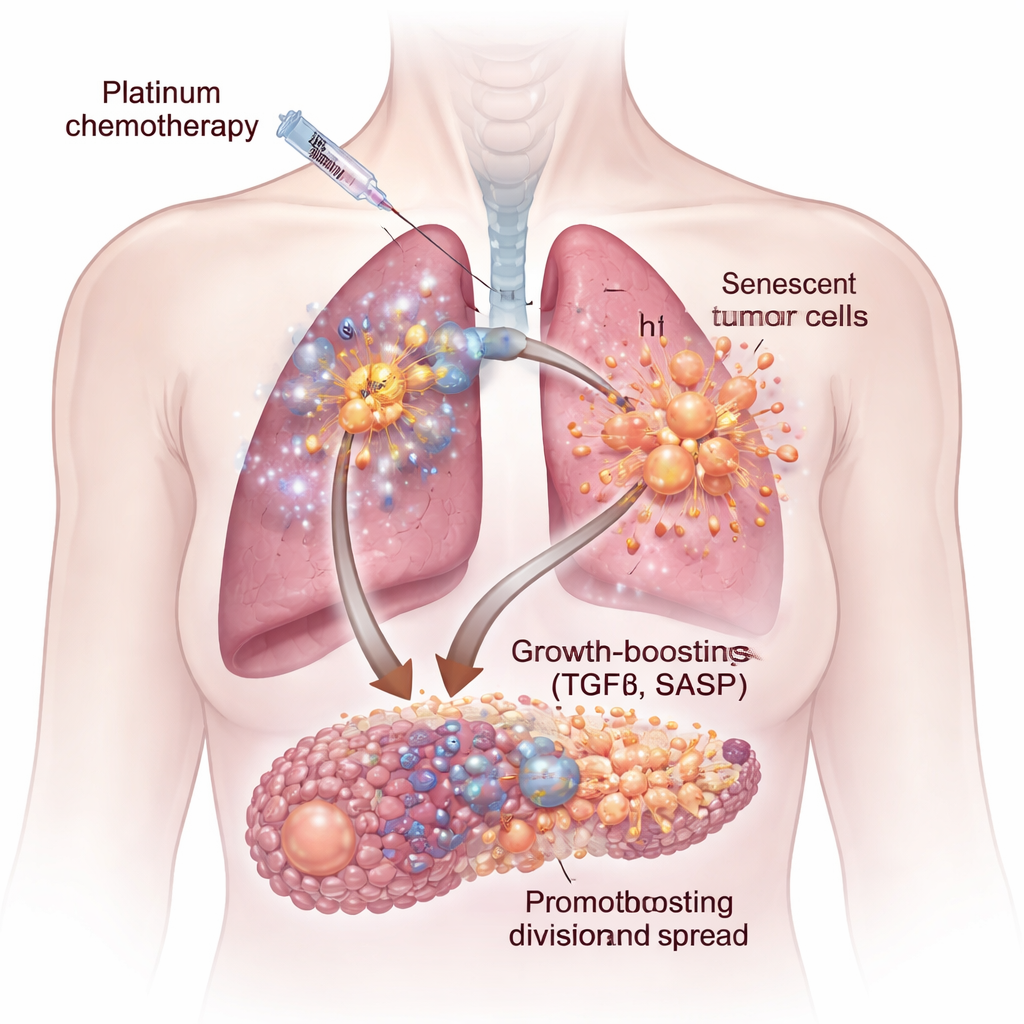
Una señal oculta de crecimiento: TGFβ
No todas las quimioterapias desencadenaron las mismas secreciones perjudiciales. Al comparar los fármacos con platino con otros dos agentes comunes, docetaxel y palbociclib, solo las células tratadas con platino produjeron un SASP que aumentaba de forma marcada el crecimiento tumoral. Combinando estudios de expresión génica, mediciones proteicas y un microarreglo de microambientes de alto rendimiento, identificaron a un culpable clave: la molécula de señalización factor de crecimiento transformante beta, o TGFβ. Las células senescentes inducidas por cisplatino estaban enriquecidas en múltiples formas de TGFβ y en vías relacionadas. Añadir TGFβ purificado a células cancerosas imitó el impulso de crecimiento observado con el fluido de células senescentes, lo que destaca a esta familia de citocinas como un motor central del secretoma pro-tumoral.
Cómo la señal reprograma las células cancerosas
El estudio rastreó luego cómo estas señales ricas en TGFβ cambian el comportamiento de las células tumorales vecinas. En la superficie de las células receptoras, TGFβ se une a un receptor llamado TGFBR1. Esto, a su vez, activa una cadena interna de proteínas —particularmente las vías AKT y mTOR— que se sabe que controlan el crecimiento celular, el metabolismo y la supervivencia. Tanto en células de cáncer de pulmón humanas como de ratón, la exposición a las secreciones derivadas del cisplatino aumentó rápidamente las formas activadas (fosforiladas) de AKT y de su blanco aguas abajo p70S6K, y potenció la expresión de genes del ciclo celular. Bloquear TGFBR1 con un fármaco llamado galunisertib, o inhibir directamente mTOR, cerró en gran medida este aumento de señalización y redujo la proliferación adicional, la formación de colonias y el crecimiento invasivo de esferas desencadenados por el secretoma senescente.
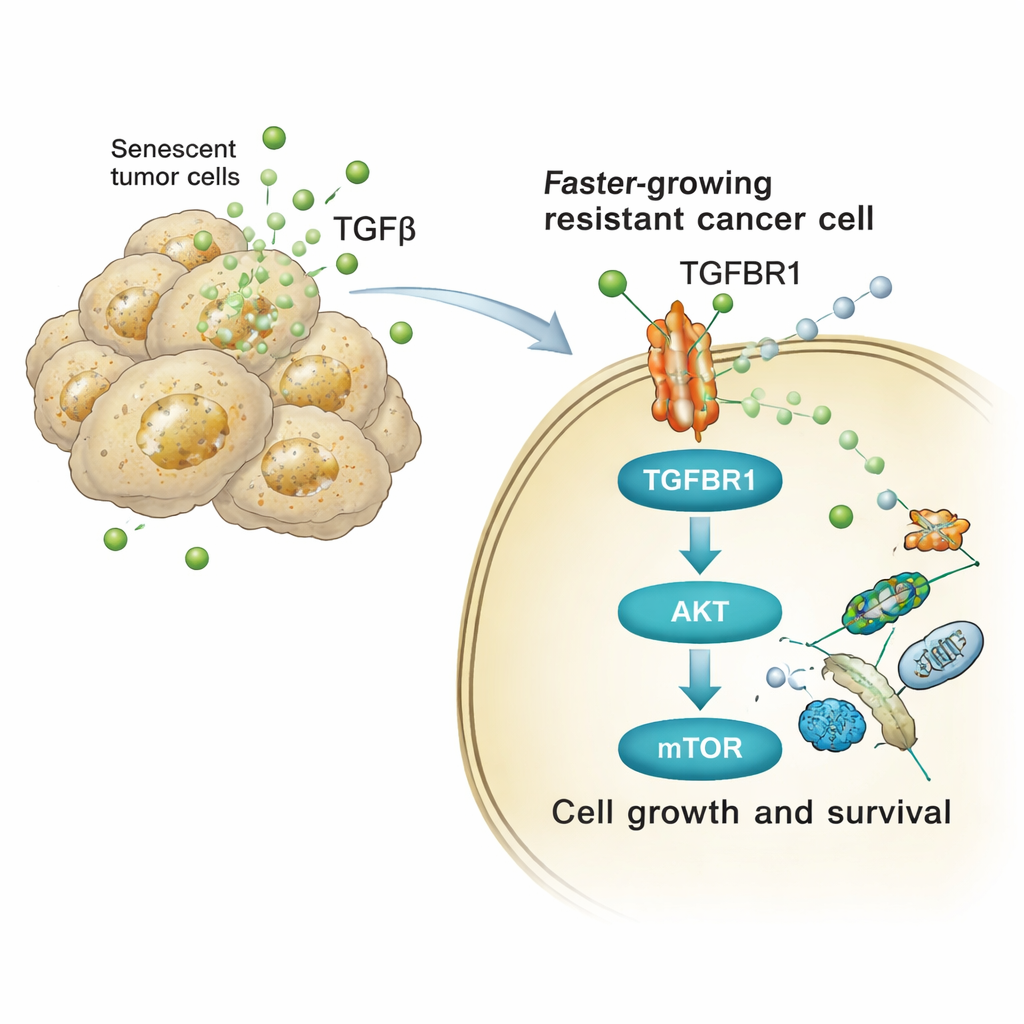
De los ratones a los pacientes: un punto débil compartido
Estos mecanismos no se limitaron a placas de cultivo. En ratones con tumores pulmonares, mezclar células cancerosas senescentes y no senescentes dio lugar a tumores de crecimiento más rápido y a una supervivencia menor, mientras que eliminar las células senescentes o bloquear TGFBR1 atenuó este efecto. Cuando se administró cisplatino estándar a ratones con cánceres de pulmón genéticamente modificados, los tumores acumularon marcadores de senescencia junto con alta actividad de AKT/mTOR en células cercanas que seguían dividiéndose. Combinar cisplatino con la inhibición de TGFBR1 o con fármacos senolíticos (que eliminan selectivamente las células senescentes) redujo la carga tumoral y prolongó la supervivencia en comparación con la quimioterapia sola. De forma crucial, los análisis de muestras humanas de cáncer de pulmón y de carcinoma seroso de alto grado de ovario tomadas tras la terapia basada en platino revelaron patrones similares: aumento de marcadores de senescencia y mayor señalización AKT/mTOR en el microambiente tumoral, especialmente en regiones ricas en células senescentes.
Convertir una desventaja en una ventaja
Para el lector general, la conclusión es que la quimioterapia con platino puede dejar tras de sí una población de células dañadas pero peligrosas, unas “células zombis”. Estas células tumorales senescentes ya no se dividen, pero secretan señales ricas en TGFβ que reactivan a las células cancerosas vecinas, ayudando a que los tumores vuelvan a crecer y a resistir tratamientos posteriores. La noticia alentadora es que esta debilidad puede ser explotada terapéuticamente. En modelos preclínicos de cáncer de pulmón y ovario, añadir fármacos que bloquean el receptor TGFBR1 o que eliminan selectivamente las células senescentes hizo que la quimioterapia con platino fuera más efectiva y mejoró la supervivencia sin toxicidad adicional evidente. El trabajo apunta hacia futuros ensayos clínicos que combinen el tratamiento estándar con platino con estrategias senolíticas o anti-TGFβ, con el objetivo de conservar los beneficios de la quimioterapia al tiempo que se desactivan sus efectos colaterales ocultos impulsados por la senescencia.
Cita: González-Gualda, E., Reinius, M.A.V., Macias, D. et al. Treatment resistance to platinum-based chemotherapy in lung and ovarian cancer is driven by a targetable TGFβ senescent secretome. Nat Aging 6, 368–392 (2026). https://doi.org/10.1038/s43587-025-01054-2
Palabras clave: resistencia a la quimioterapia, senescencia celular, señalización TGFβ, cáncer de pulmón, cáncer de ovario