Clear Sky Science · es
El daño del ADN en macrófagos impulsa la autorreactividad inmunitaria mediante la presentación de antígenos nucleares
Cuando el desgaste celular vuelve al sistema inmunitario contra nosotros
El envejecimiento conlleva un mayor riesgo de enfermedades autoinmunes, en las que el sistema inmunitario comienza a atacar el propio cuerpo que debe proteger. Este estudio explora un culpable sorprendente: el daño cotidiano del ADN dentro de células inmunitarias llamadas macrófagos. Al rastrear cómo este daño cambia lo que los macrófagos muestran a otras células inmunitarias, los investigadores descubren un posible eslabón perdido entre el envejecimiento y el desarrollo de enfermedades como el lupus.
Los guardianes del cuerpo que se salen del guion
Los macrófagos son defensores de primera línea que engullen microbios y desechos y luego exhiben fragmentos proteicos a las células T, ayudando al sistema inmunitario a decidir qué atacar. El equipo diseñó ratones cuyos macrófagos presentaban un defecto en una proteína clave de reparación del ADN, ERCC1-XPF, de modo que estas células acumulaban daño persistente en el ADN. A medida que estos ratones envejecían, desarrollaron rasgos de autoinmunidad: focos inflamatorios en los riñones, depósitos de complejos inmunes y proteínas del complemento, bazo agrandado y niveles elevados de anticuerpos antinucleares similares a los observados en animales naturalmente viejos. Un perfil inmunitario detallado mostró una expansión de células plasmáticas, células T activadas y células asesinas naturales, todos signos de un sistema inmunitario crónicamente estimulado.
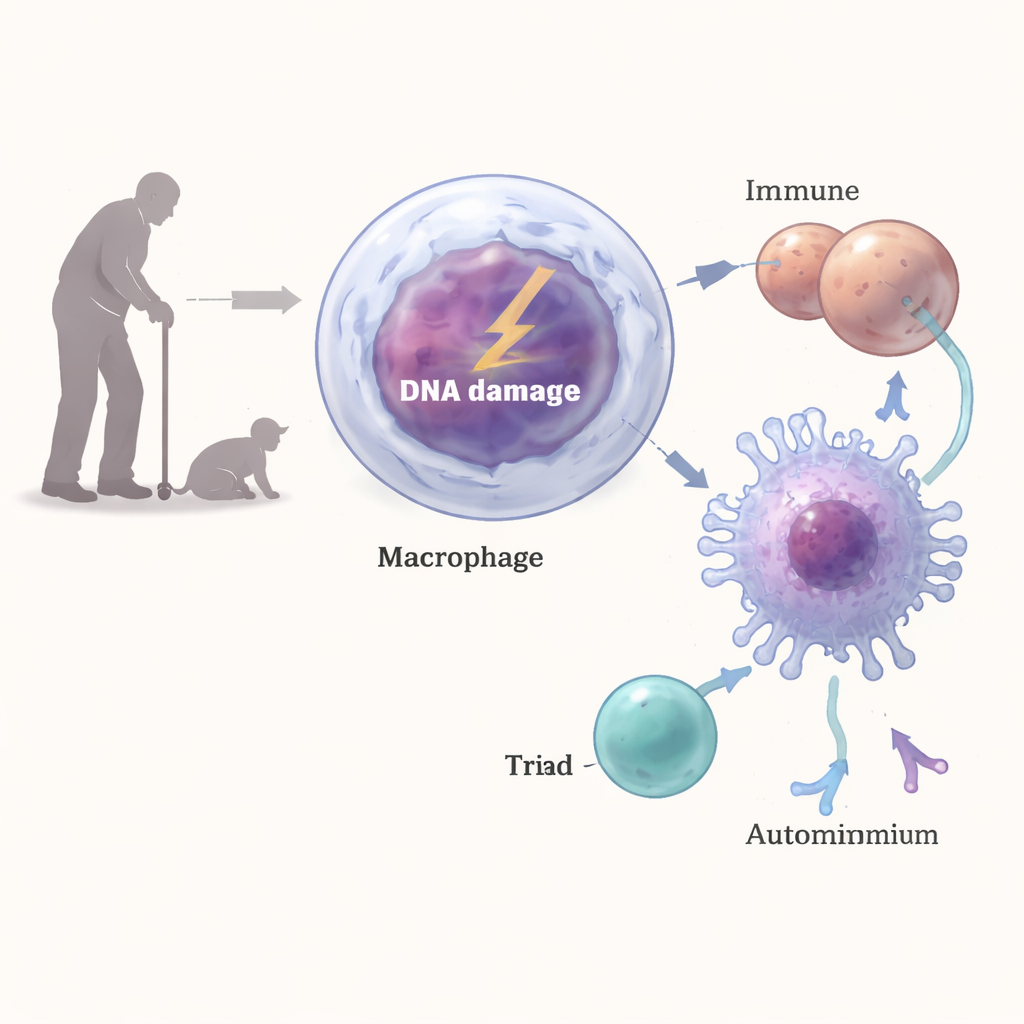
Del ADN roto a las células T que atacan lo propio
¿Cómo podría el daño en el ADN de los macrófagos desencadenar una respuesta tan intensa, similar a la autoinmune? Los investigadores hallaron que las roturas de ADN activaban una vía clásica de respuesta al daño en estas células, que implicaba enzimas como ATM, ATR y DNA-PK. Esta señalización elevó la expresión en superficie de MHC clase II, las vitrinas moleculares utilizadas para presentar fragmentos proteicos a las células T CD4. Cuando los macrófagos con daño en el ADN se mezclaban con células T, provocaban una activación más fuerte de las T y una mayor producción de interferón gamma que los macrófagos normales. Bloquear MHC-II o interferir con la respuesta al daño del ADN revirtió gran parte de este efecto, y en animales vivos, anticuerpos que bloqueaban MHC-II o la depleción de células T CD4 redujeron la inflamación renal y los niveles de autoanticuerpos.
Proteínas propias del núcleo expuestas en primer plano
Para ver exactamente qué mostraban los macrófagos dañados a las células T, el equipo aisló los péptidos unidos a MHC-II y los analizó mediante espectrometría de masas. En comparación con células normales o estimuladas con lipopolisacárido, los macrófagos con daño en el ADN presentaron un repertorio de péptidos notablemente diferente. En lugar de provenir mayoritariamente de proteínas de membrana y extracelulares, sus moléculas MHC-II estaban enriquecidas en fragmentos derivados de proteínas nucleares y ribosomales, incluidas histonas y otros componentes estrechamente asociados al ADN. Cuando algunos de estos péptidos nucleares se sintetizaron y utilizaron para restimular células inmunitarias de los ratones modificados, desencadenaron fuertes respuestas de células T, lo que sugiere que estos fragmentos de origen propio eran, de hecho, inmunogénicos.
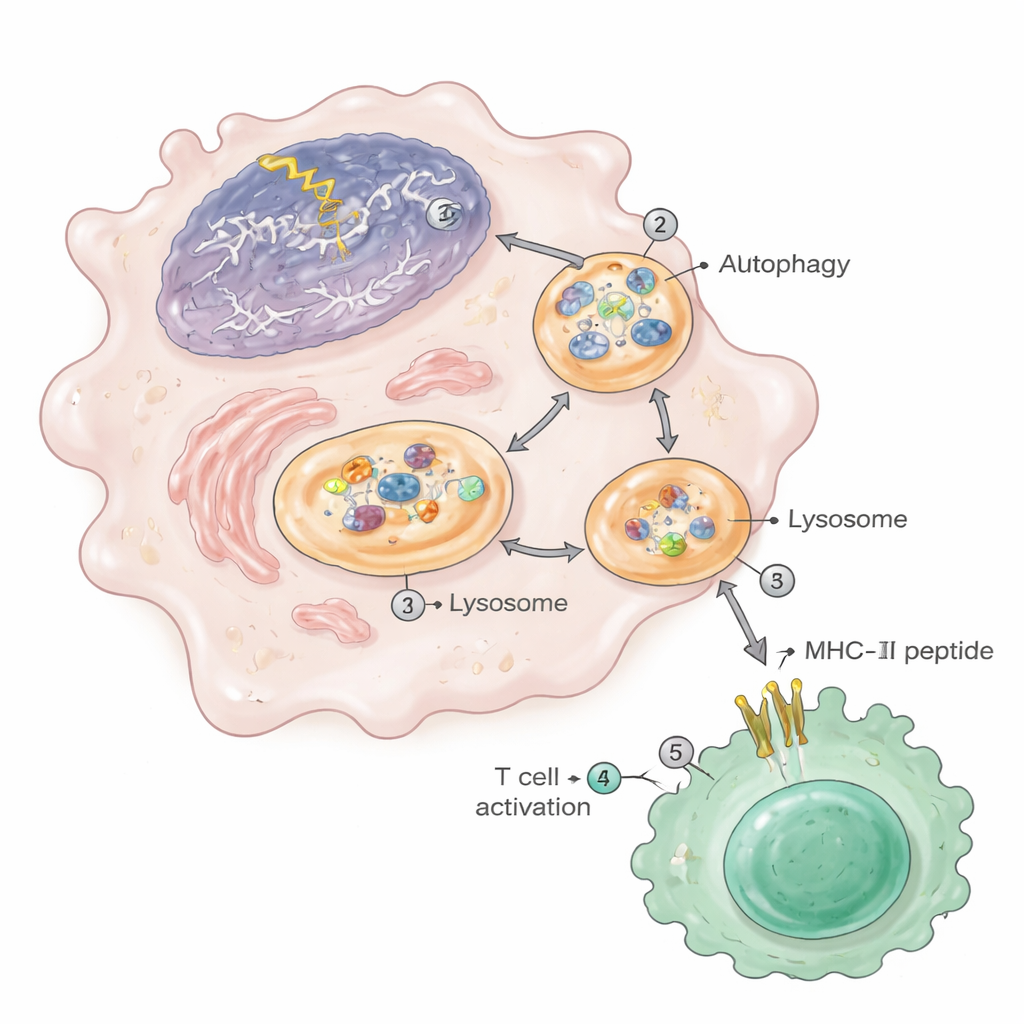
Autofagia: la vía de limpieza que alimenta la autoinmunidad
El tránsito del material nuclear hacia la vitrina MHC-II dependió en gran medida de la autofagia, el sistema interno de reciclaje celular. Ante el daño en el ADN, la autofagia se intensificó y transportó fragmentos de cromatina—del propio núcleo celular—hacia autofagosomas que luego se fusionaban con los lisosomas, donde las proteínas se degradan en péptidos. Estos lisosomas en macrófagos dañados contenían niveles elevados de proteínas nucleares y ribosomales. Cuando los investigadores bloquearon la autofagia con fármacos o eliminaron genéticamente un gen esencial de autofagia (Atg5) en las mismas células mieloides, los animales presentaron menos lesiones renales, menos células T activadas y células plasmáticas, y una reducción drástica de los péptidos nucleares que aparecían en MHC-II. Fragmentos similares de cromatina y un aumento de la presentación antigénica se observaron en macrófagos de ratones propensos al lupus, en líneas celulares humanas de monocitos expuestas a fármacos que dañan el ADN y en macrófagos de ratones muy viejos.
Por qué esto importa para el envejecimiento y la enfermedad autoinmune
En conjunto, los hallazgos sugieren una idea sencilla pero potente: a medida que envejecemos, el daño en el ADN se acumula en los macrófagos, que a su vez utilizan la autofagia para eliminar los restos nucleares. Al hacerlo, fragmentan inadvertidamente el material nuclear en péptidos que se cargan en MHC-II y se muestran a las células T como si fueran ajenos. Con el tiempo, esta exposición crónica a autoantígenos nucleares puede entrenar al sistema inmunitario para reaccionar contra el propio cuerpo, promoviendo la autoinmunidad. Al identificar esta vía—del daño en el ADN a la autofagia y la presentación de antígenos nucleares—el estudio destaca nuevas estrategias para mitigar la autoinmunidad relacionada con la edad, como mejorar la reparación del ADN, ajustar finamente la autofagia o bloquear selectivamente la presentación de péptidos nucleares propios sin apagar las defensas vitales del sistema inmunitario.
Cita: Niotis, G., Arvanitaki, E.S., Theodorakis, E. et al. DNA damage in macrophages drives immune autoreactivity via nuclear antigen presentation. Nat Aging 6, 393–413 (2026). https://doi.org/10.1038/s43587-025-01053-3
Palabras clave: envejecimiento y autoinmunidad, daño en el ADN, macrófagos, autofagia, anticuerpos antinucleares