Clear Sky Science · es
Análisis exploratorios de resultados clínicos del estudio BIIB080 fase 1b en la enfermedad de Alzheimer leve
Por qué esta investigación importa para las familias
La enfermedad de Alzheimer deteriora lentamente la memoria, la independencia y la identidad; los fármacos actuales ofrecen solo un alivio modesto. La mayoría de los tratamientos nuevos se han centrado en eliminar un culpable: la proteína amiloide, con un impacto limitado sobre el otro sello distintivo clave de la enfermedad: los ovillos enredados de una proteína llamada tau dentro de las células cerebrales. Este estudio exploró si un fármaco experimental, BIIB080, que pretende reducir la producción de tau en su origen genético podría frenar con seguridad la pérdida de memoria y el deterioro en la vida diaria en personas con Alzheimer temprano.
Una nueva forma de reducir una proteína dañina
En lugar de atacar la tau una vez que ya ha formado ovillos, BIIB080 actúa un paso antes. Es un oligonucleótido antisentido, una corta hebra de material genético sintético diseñada para unirse al mensajero que las células usan para fabricar tau. Al adherirse a ese mensajero, BIIB080 instruye a las células para que lo destruyan, reduciendo la cantidad total de tau que produce el cerebro, incluidas las formas que se consideran especialmente tóxicas. La esperanza es que, con menos tau nueva, los ovillos existentes puedan disminuir y propagarse más lentamente, atenuando el daño a los circuitos cerebrales que subyace a los problemas de memoria y pensamiento en la enfermedad de Alzheimer.
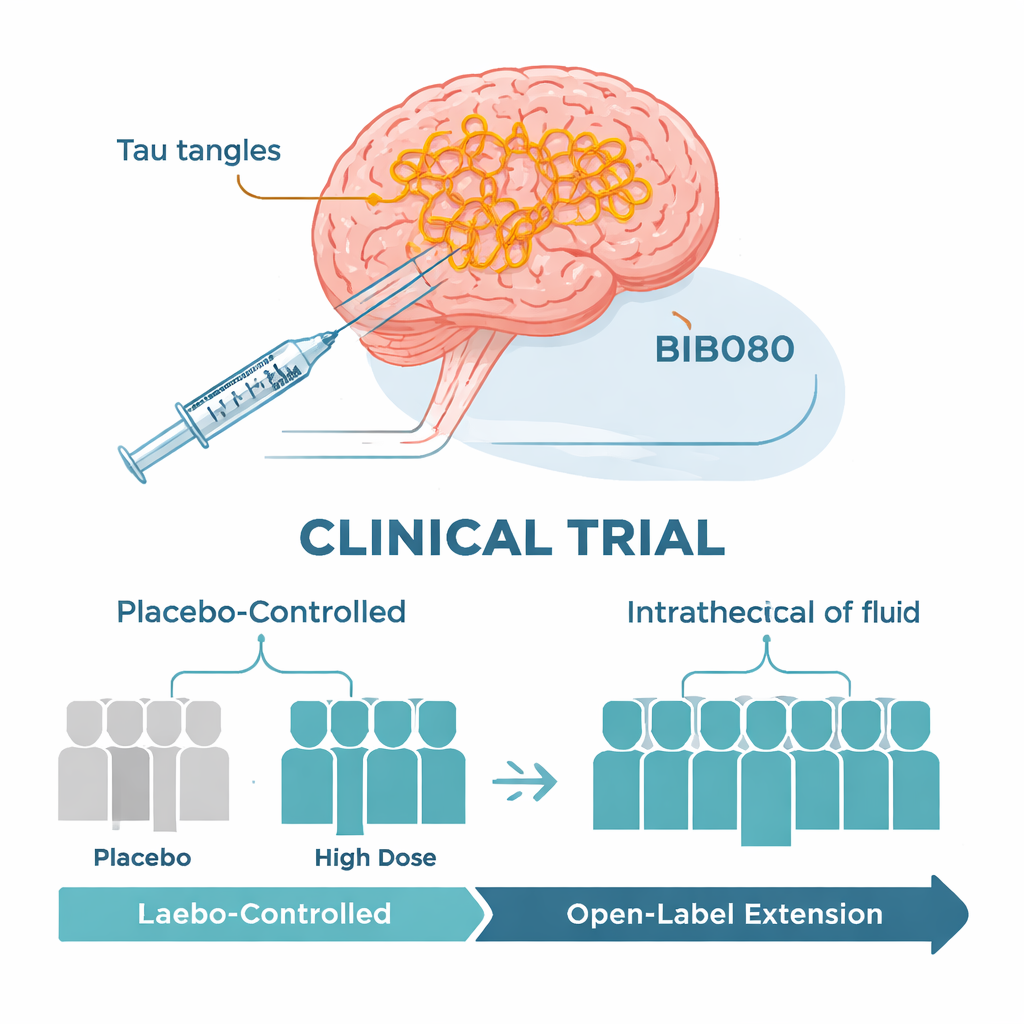
Cómo se diseñó el ensayo temprano
Los investigadores llevaron a cabo un ensayo clínico internacional fase 1b principalmente diseñado para evaluar la seguridad. Se inscribieron poco más de 100 personas de 50 a 74 años con Alzheimer leve, confirmado mediante pruebas de líquido cefalorraquídeo. En la primera parte del estudio, los participantes fueron asignados al azar para recibir BIIB080 o un placebo mediante inyecciones periódicas en el líquido que rodea la médula espinal durante tres meses, seguidas de varios meses de seguimiento. Diferentes grupos recibieron dosis crecientes de forma gradual. A continuación se realizó una extensión a largo plazo en la que todos recibieron lo que el equipo consideró una dosis alta de BIIB080 durante casi un año. Como en esta segunda fase no hubo grupo con placebo, los científicos compararon a los pacientes tratados con pacientes bien emparejados extraídos de otros estudios amplios sobre Alzheimer.
Señales de un deterioro más lento en el pensamiento y la vida diaria
Aunque el estudio fue pequeño y no se diseñó para demostrar eficacia, surgieron varios patrones. Las personas que recibieron las dosis más altas de BIIB080 mostraron, en promedio, menos empeoramiento en pruebas estándar de función cognitiva (como el Mini-Mental State Examination), memoria y capacidad para manejar tareas cotidianas que los que recibieron placebo durante los primeros meses. En la extensión a largo plazo, 16 participantes que continuaron con dosis altas a lo largo del estudio se compararon con “controles externos” cuidadosamente emparejados procedentes de otro ensayo centrado en la tau y de una importante base de datos de investigación del Alzheimer. En múltiples medidas —clasificación global de demencia, puntuaciones cognitivas y cuestionarios funcionales—, el grupo tratado con BIIB080 tendió a declinar más lentamente que estos grupos de comparación durante aproximadamente dos años desde el inicio del tratamiento.
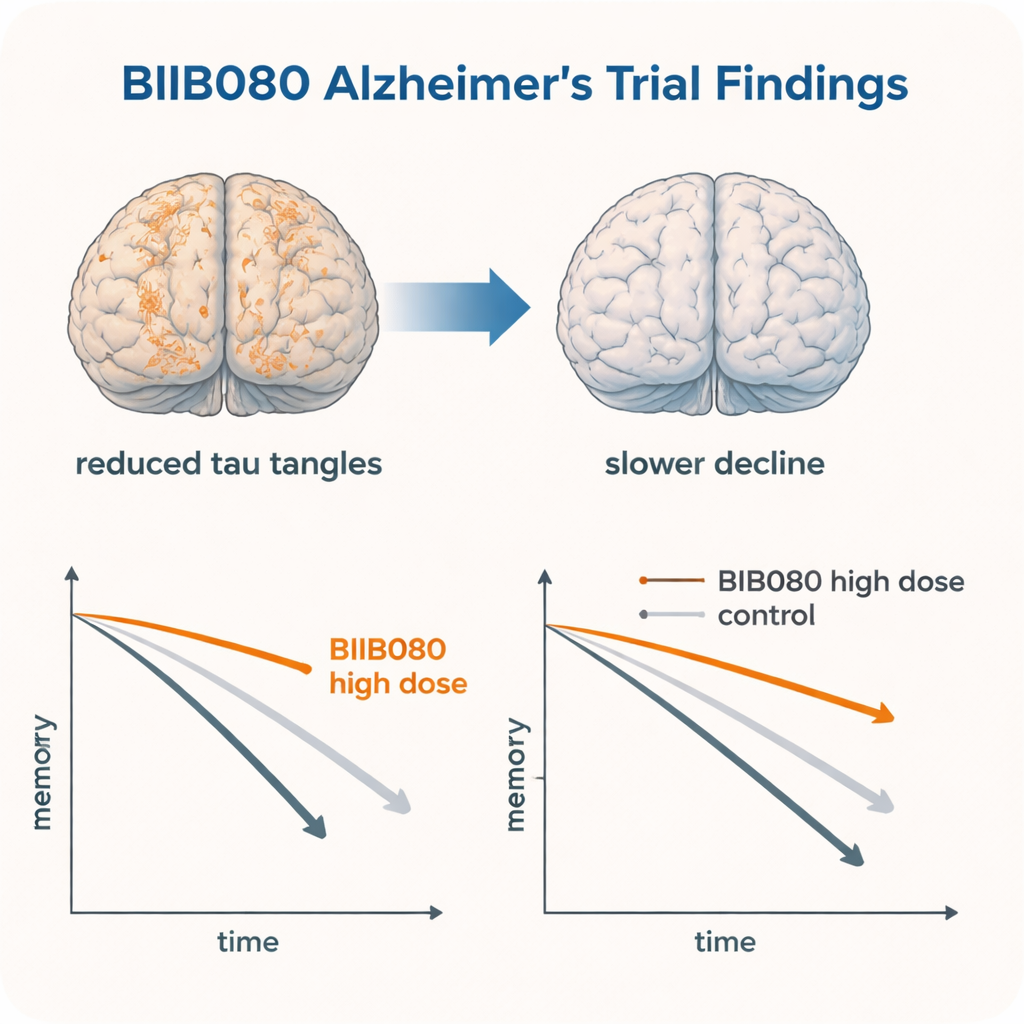
Cambios dentro del cerebro que coinciden con las tendencias clínicas
Informes anteriores del mismo ensayo ya habían mostrado que BIIB080 redujo de forma notable los niveles de tau en el líquido cefalorraquídeo y, de manera llamativa, disminuyó la cantidad de ovillos de tau observados en exploraciones cerebrales especializadas en muchas regiones. Los hallazgos clínicos exploratorios de este estudio se corresponden con esos cambios biológicos: donde los ovillos de tau disminuyeron, la función cognitiva y la capacidad para la vida diaria parecieron deteriorarse más despacio. En modelos animales que sobreproducen tau, fármacos antisentido similares no solo redujeron los depósitos de tau, sino que también atenuaron las convulsiones, la pérdida de neuronas y los problemas de conducta. En conjunto, estos hilos de evidencia sugieren que reducir la tau en su origen podría realmente modificar el curso del Alzheimer, no solo enmascarar síntomas.
Seguridad, salvedades y siguientes pasos
La mayoría de los efectos adversos de BIIB080 en este ensayo fueron leves a moderados y estuvieron relacionados con las propias inyecciones espinales, como dolor de cabeza, dolor de espalda o mareo temporal. Algunos participantes desarrollaron problemas más serios, incluido un empeoramiento de los síntomas de demencia, y suspendieron el tratamiento, por lo que sigue siendo esencial una monitorización cuidadosa. Es importante subrayar que el estudio fue pequeño, usó varios grupos de dosis con características iniciales desiguales y se basó en la comparación con datos externos una vez que todos recibieron el fármaco activo. Por tanto, los autores insisten en que las tendencias alentadoras todavía podrían deberse al azar o a sesgos sutiles.
Qué podría significar para tratamientos futuros
Para las personas que afrontan la enfermedad de Alzheimer, estos hallazgos aún no ofrecen una nueva terapia aprobada, pero señalan un camino prometedor. BIIB080 parece reducir con seguridad los ovillos de tau en el cerebro humano y se asocia con un declive clínico más lento en este estudio inicial, especialmente a dosis más altas. Dado que el ensayo fue exploratorio, se necesitan estudios mayores y más rigurosos para confirmar si el fármaco realmente frena la pérdida de memoria y preserva la independencia. Dicha investigación ya está en marcha en un ensayo de fase 2 llamado CELIA, que seguirá a más pacientes durante más tiempo. Si los resultados futuros se mantienen, las terapias que reduzcan la producción de tau podrían sumarse o complementar los fármacos dirigidos a la amiloide, ofreciendo un enfoque más completo para alterar el curso del Alzheimer.
Cita: Shulman, M., Wu, S., Ziogas, N. et al. Exploratory analyses of clinical outcomes from the BIIB080 phase 1b study in mild Alzheimer’s disease. Nat Aging 6, 445–453 (2026). https://doi.org/10.1038/s43587-025-01031-9
Palabras clave: Enfermedad de Alzheimer, proteína tau, terapia antisense, ensayo clínico, neurodegeneración