Clear Sky Science · es
Las senotoxinas atacan la senescencia mediante especificidad de unión a lípidos, desequilibrio iónico y remodelación del lipidoma
Por qué matar células “zombi” podría afinar el tratamiento del cáncer
A medida que envejecemos —o tras someternos a tratamientos agresivos como la quimioterapia— algunas células dejan de dividirse pero se niegan a morir. Estas células “zombi”, conocidas como células senescentes, pueden segregar moléculas inflamatorias que dañan tejidos y pueden ayudar a que los tumores reaparezcan. Este estudio explora una vía sorprendente para eliminar selectivamente esas células problemáticas usando una proteína derivada de veneno, lo que podría hacer que los tratamientos contra el cáncer sean a la vez más eficaces y más seguros.
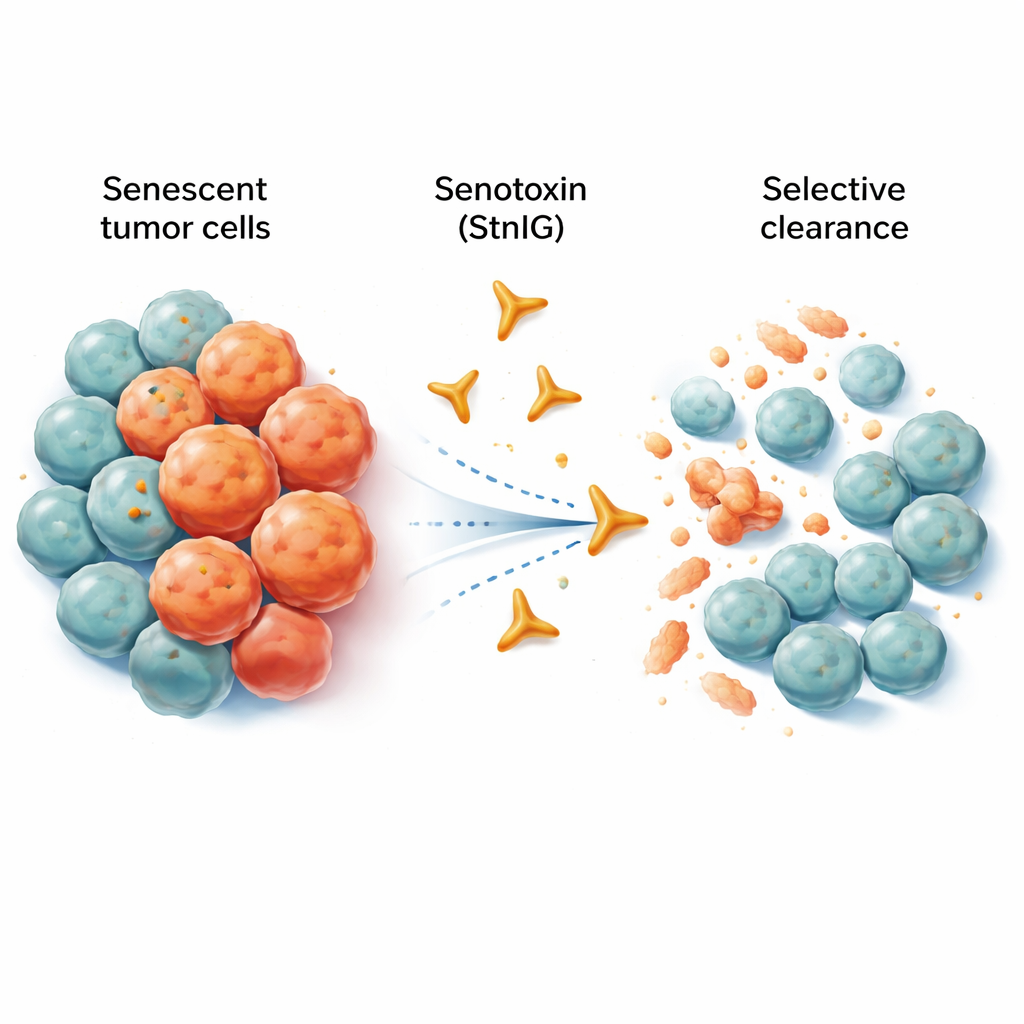
Células viejas que no se van
Las células senescentes son como trabajadores jubilados que siguen ocupando su puesto y alteran la oficina. Ya no se multiplican, pero liberan un cóctel de señales inflamatorias que pueden debilitar el tejido circundante, promover el envejecimiento e incluso favorecer el crecimiento y la diseminación tumoral. La quimioterapia, aunque mata muchas células cancerosas, a menudo deja tras de sí una población de células senescentes dentro y alrededor del tumor. Estas células persistentes pueden alimentar la inflamación crónica, los efectos secundarios y, finalmente, la recaída. Los fármacos experimentales existentes llamados senolíticos intentan eliminar las células senescentes, pero muchos de ellos dañan también células sanas, actúan solo en un rango de dosis muy estrecho o son difíciles de absorber por el organismo.
Convertir el veneno de anémona de mar en una herramienta de precisión
Los investigadores recurrieron a los especialistas naturales en matar células: los venenos animales. Se centraron en una proteína formadora de poros llamada sticholysina I (StnI), encontrada en una anémona marina caribeña. Esta proteína puede perforar pequeñas aberturas en las membranas celulares. El equipo descubrió que StnI, y una versión afinada que diseñaron llamada StnIG, son notablemente mejores matando células cancerosas senescentes que a sus vecinas no senescentes. En varios tipos de células humanas cancerosas (melanoma, hígado, pulmón y tumores de origen nervioso) inducidas a senescencia por fármacos quimioterapéuticos, StnI y sobre todo StnIG eliminaron las células envejecidas a dosis mucho más bajas de las necesarias para afectar a células en proliferación activa. StnIG fue más selectiva que un senolítico experimental líder, navitoclax, lo que sugiere que las toxinas cuidadosamente diseñadas pueden superar los enfoques actuales.
Cómo las membranas alteradas se convierten en un talón de Aquiles
Las células senescentes no solo cambian internamente; su membrana exterior —la piel grasa que rodea cada célula— también se remodela. En las células sanas, ciertos lípidos se sitúan principalmente en el lado interno de la membrana, ocultos desde el exterior. En las células senescentes ese equilibrio se rompe y esos lípidos quedan expuestos. Mediante análisis químicos detallados y simulaciones por ordenador, el equipo demostró que StnIG reconoce y se adhiere a este paisaje lipídico alterado. Su estructura es especialmente apta para engancharse a lípidos concretos que las células senescentes muestran en su superficie. Una vez adherida, StnIG forma poros que permiten que átomos cargados, o iones, fluyan dentro y fuera de forma muy desequilibrada.
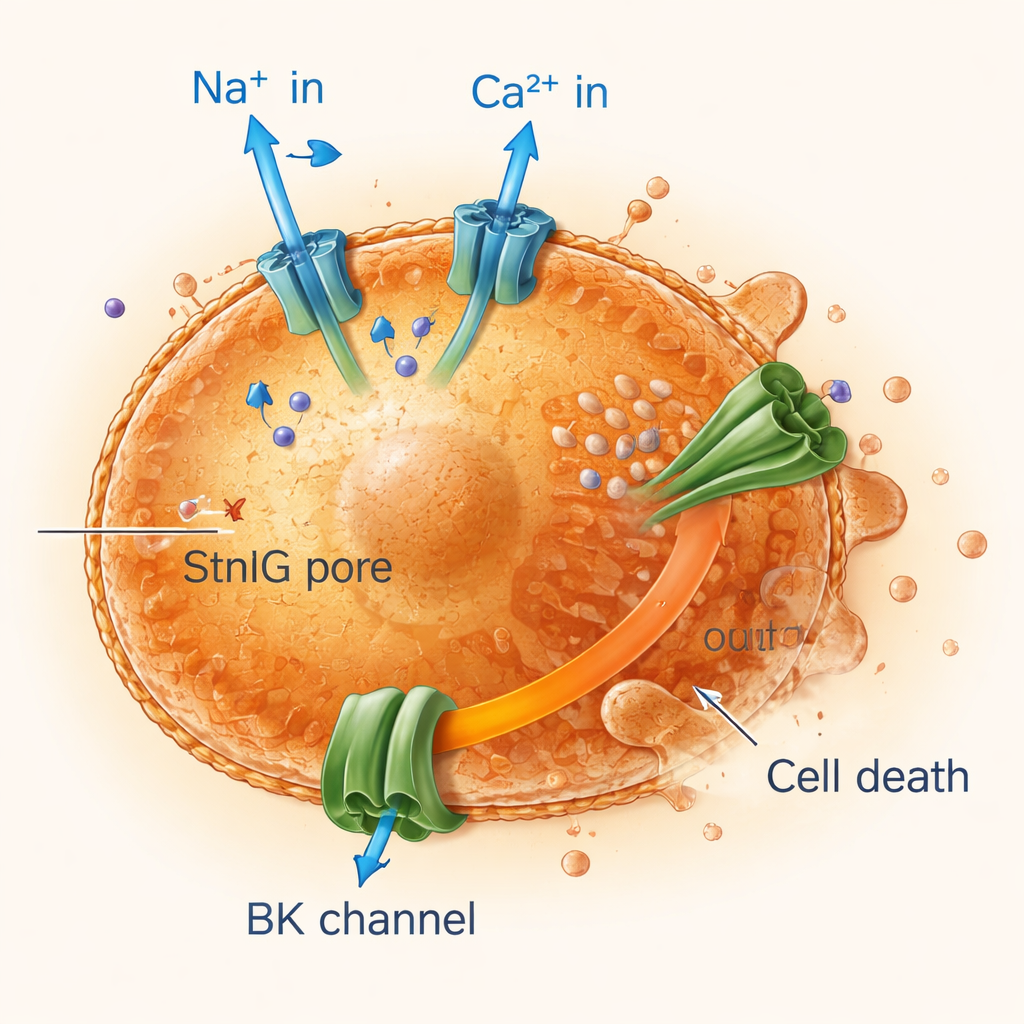
Poner en corto circuito a las células envejecidas mediante desequilibrio iónico
Al monitorizar la electricidad y el movimiento iónico a través de las membranas celulares, los investigadores observaron que los poros de StnIG permiten que sodio y calcio entren rápidamente en las células senescentes mientras el potasio se fuga de forma continua. El aumento de calcio activa grandes canales de potasio, amplificando la pérdida de potasio, que es crucial para mantener el volumen y la supervivencia celular. Las células senescentes, ya menos flexibles y más frágiles que las sanas, no pueden soportar esta perturbación iónica sostenida. Sus mitocondrias —las centrales energéticas de la célula— pierden su carga eléctrica, la producción de energía cae y las células experimentan formas programadas de muerte, incluida la apoptosis y una muerte inflamatoria y violenta llamada piroptosis. Bloquear la entrada de calcio o los canales de potasio protegió a las células senescentes, confirmando que este desequilibrio iónico es central en la acción de la toxina.
De los cultivos celulares a los animales vivos
El equipo probó luego si esta estrategia funciona en organismos vivos. En embriones de pez cebra portadores de células humanas de melanoma senescentes, dosis bajas de StnIG redujeron el número de estas células con la misma eficacia que navitoclax, sin toxicidad aparente. En modelos murinos de melanoma y cáncer de hígado, la quimioterapia con un fármaco del ciclo celular (palbociclib) ralentizó el crecimiento tumoral al inducir la senescencia en muchas células cancerosas. Cuando los investigadores añadieron StnIG de forma intermitente, los tumores se encogieron o entraron en remisión con más eficacia que con la quimioterapia sola, y de forma comparable a la combinación quimioterapia–navitoclax. Importante: los ratones tratados con StnIG presentaron efectos secundarios limitados y sin daños evidentes en órganos principales, aunque el potasio sanguíneo aumentó en animales con tumores senescentes, probablemente reflejando la liberación masiva de potasio al destruirse las células tumorales.
Qué significa esto para la futura atención del cáncer
Este trabajo presenta las “senotoxinas”: proteínas inspiradas en venenos y diseñadas que explotan las particularidades de membrana y manejo iónico de las células senescentes. Al dirigirse a lípidos alterados y forzar desequilibrios iónicos fatales, StnIG puede eliminar selectivamente células senescentes dañinas mientras respeta la mayor parte del tejido sano. Empleadas junto con la quimioterapia, tales senotoxinas podrían algún día ayudar a barrer las células zombi que alimentan la recaída y la inflamación crónica, haciendo los tratamientos contra el cáncer más duraderos y potencialmente aliviando algunos efectos secundarios a largo plazo.
Cita: Moral-Sanz, J., Fernández-Carrasco, I., Ramponi, V. et al. Senotoxins target senescence via lipid binding specificity, ion imbalance and lipidome remodeling. Nat Aging 6, 349–367 (2026). https://doi.org/10.1038/s43587-025-01030-w
Palabras clave: senescencia celular, senolíticos, tratamiento del cáncer, fármacos derivados de veneno, canales iónicos