Clear Sky Science · es
La edición de bases en PIK3CD adaptada a CAR mejora la potencia antitumoral de las células T
Reprogramando las células que combaten el cáncer
La terapia con células T con receptor de antígeno quimérico (CAR) ha transformado el tratamiento de algunos cánceres hematológicos, pero muchos pacientes siguen recaendo o no responden. Un problema clave es que estas células inmunitarias diseñadas pueden agotarse o no persistir en el organismo el tiempo suficiente. Este estudio plantea una pregunta simple pero potente: en lugar de rediseñar por completo los CAR, ¿y si pudiéramos «reajustar» sutilmente el cableado interno de las células T para que mantengan su potencia durante más tiempo y lo hagan con seguridad?
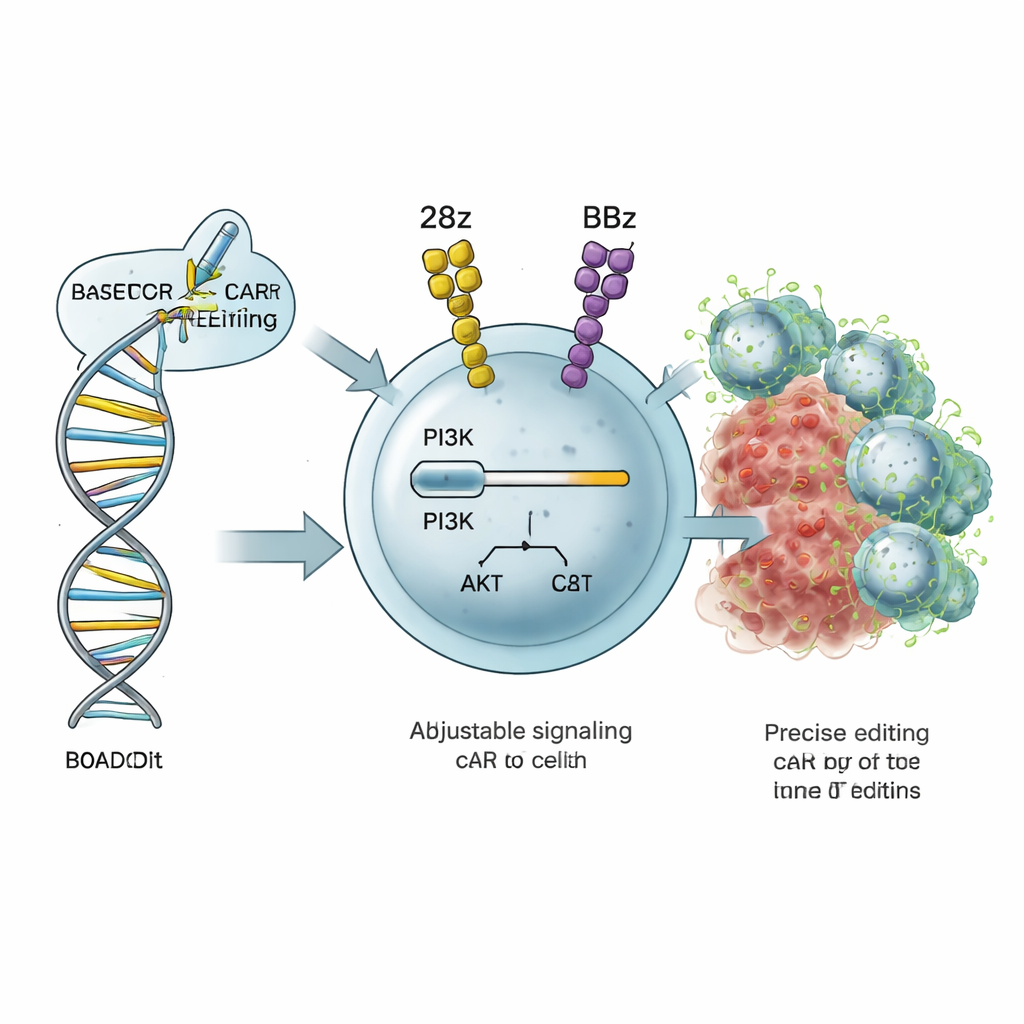
Apuntando al control de volumen de la célula T
Las células T asesinas del cáncer dependen de circuitos de señalización internos que les indican con qué intensidad activarse, con qué rapidez dividirse y si convertirse en combatientes de corta vida o en células de memoria de larga duración. Un circuito importante es la vía PI3K–AKT, en la que una proteína llamada PI3Kδ —codificada por el gen PIK3CD— actúa como un control de volumen para la activación y el metabolismo. Los autores desarrollaron una estrategia que llaman ROADSTAR, que utiliza la edición de bases, una forma de ingeniería genómica CRISPR de alta precisión, para cambiar letras individuales en PIK3CD. En lugar de apagar o encender por completo la vía, ROADSTAR busca pequeñas mutaciones que aumenten o reduzcan la señalización de forma suave, adaptándola a la arquitectura concreta del CAR presente en la célula T.
Descubriendo mutaciones útiles
El equipo construyó una biblioteca de 34 cambios de una sola letra en la región reguladora de PIK3CD e introdujo estas variantes en células T humanas que ya portaban uno de dos diseños de CAR comunes: 28z (basado en la molécula CD28) y BBz (basado en 4‑1BB). Estos CAR difieren en cómo estimulan a las células T: 28z tiende a inducir un ataque fuerte y rápido pero también agotamiento, mientras que BBz favorece mejor supervivencia y memoria aunque puede ser menos agresivo. Las células CAR T editadas se sometieron a una «prueba de estrés» exponiéndolas repetidamente a células leucémicas. Mediante secuenciación profunda, los investigadores rastrearon qué mutaciones permitían a las CAR T superar a sus pares no editadas durante varias semanas.
Dos mutaciones destacaron claramente. En las células BBz CAR T, un cambio llamado E81K aumentó ligeramente la actividad de PI3Kδ, incrementando las señales vía PI3K–AKT. En las CAR T 28z, un cambio distinto, L32P, atenuó la actividad de PI3Kδ. El modelado estructural sugirió que ambas ediciones alteran sutilmente la interacción de PI3Kδ con su socio regulador, ajustando la intensidad de la señalización en lugar de cambiarla totalmente. Es importante que la mutación beneficiosa para un diseño de CAR no fue la misma que para el otro, lo que subraya que cada arquitectura de CAR demanda su propio ajuste interno óptimo.
Células CAR T más fuertes, en mejor forma y de mayor duración
Cuando las ediciones prometedoras se probaron de forma individual, E81K hizo que las BBz CAR T se activaran más al detectar células tumorales, proliferaran mejor y fueran notablemente más eficaces matando objetivos cancerosos, incluidos aquellos con niveles bajos de antígeno. Estas células evolucionaron hacia un fenotipo de memoria efectora que combinaba una potente capacidad citotóxica con la capacidad de persistir. En modelos de ratón de leucemia y de neuroblastoma metastásico, las BBz CAR T editadas con E81K controlaron los tumores de forma más completa y durante mucho más tiempo que las BBz no editadas, incluso superando múltiples rondas de reexposición tumoral. Análisis detallados de ARN unicelular y de metabolismo mostraron que las células E81K tenían una función mitocondrial mejorada, mayor capacidad respiratoria y glicolítica de reserva y menos signos de agotamiento: esencialmente eran más enérgicas y resistentes.
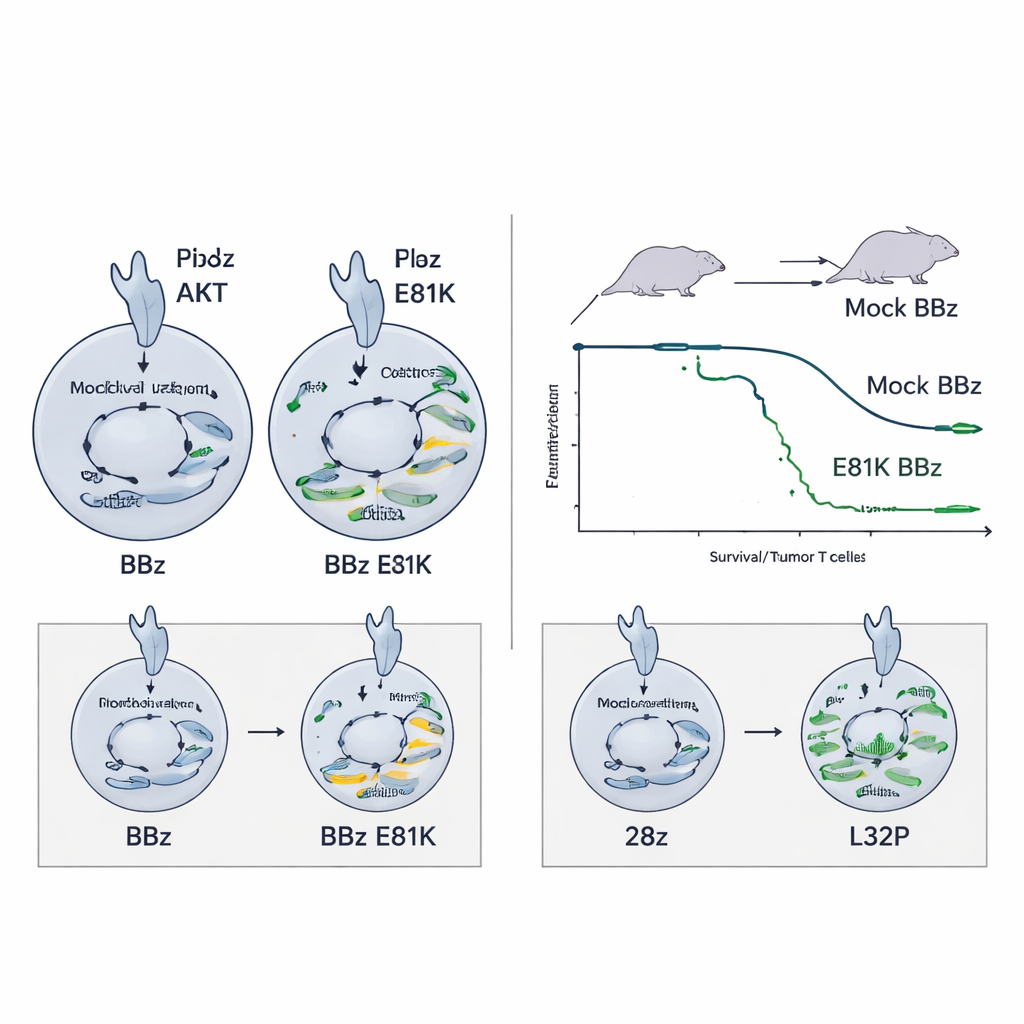
Evitar el agotamiento en CAR muy activos
El mismo impulso de E81K no ayudó —e incluso pudo perjudicar— a las CAR T 28z, que ya señalizan con fuerza. En ese contexto, la actividad extra de PI3K aumentó marcadores de agotamiento sin mejorar la función. Aquí, la mutación L32P resultó más adecuada: al reducir modestamente la señalización PI3K–AKT, las 28z CAR T editadas con L32P mostraron una activación basal menor pero conservaron una alta capacidad citotóxica y proliferaron más con el tiempo. También mantuvieron un estado menos diferenciado, similar a la memoria, incluyendo una reserva de memoria tipo célula madre que se piensa sostiene respuestas a largo plazo. En un modelo exigente de neuroblastoma, las 28z CAR T modificadas con L32P mejoraron la supervivencia en comparación con sus pares no editadas.
Seguridad y promesa futura
Una preocupación central al alterar de forma permanente la señalización inmune es el riesgo de crecimiento descontrolado o cánceres secundarios. Por ello, los autores realizaron comprobaciones de seguridad exhaustivas. Las BBz CAR T editadas con E81K no crecieron de manera anormal en cultivo, no causaron daño orgánico ni crisis inflamatorias en ratones y no mostraron signos de linfoma o invasión tisular meses después de la infusión. Las bases de datos clínicas tampoco muestran una enriquecimiento de estas mutaciones específicas de PIK3CD en las leucemias de células T. En conjunto, el trabajo demuestra que ediciones genómicas de una sola letra, cuidadosamente elegidas, pueden actuar como diales de precisión para el comportamiento de las células T: aumentar la potencia antitumoral y la persistencia respetando la biología única de cada CAR. Este enfoque ROADSTAR podría ayudar a diseñar la próxima generación de terapias CAR T, más efectivas y fiables frente a las neoplasias hematológicas y, potencialmente, frente a tumores sólidos.
Cita: Bucher, P., Brückner, N., Kortendieck, J. et al. CAR-adapted PIK3CD base editing enhances T cell anti-tumor potency. Nat Cancer 7, 368–383 (2026). https://doi.org/10.1038/s43018-025-01099-7
Palabras clave: Células CAR T, Señalización PI3K, Edición de bases, Inmunoterapia contra el cáncer, Metabolismo de las células T