Clear Sky Science · es
Glioma difuso de línea media con alteración H3.3K27M de novo en organoides del tronco encefálico humano para desentrañar la función de las células CAR T anti-GD2
Por qué importa este estudio sobre cáncer cerebral infantil
El glioma difuso de línea media es uno de los cánceres cerebrales infantiles más letales; afecta a niños muy pequeños en el tronco encefálico y deja a las familias con casi ninguna opción terapéutica eficaz. Como los tumores se sitúan profundamente en el cerebro y rara vez se operan, los investigadores disponen de poco tejido para estudiar y de pocas maneras seguras de probar nuevas terapias. Este estudio construye un “mini‑tronco encefálico en un plato” realista y lo utiliza para observar cómo se comporta, durante semanas, una prometedora inmunoterapia —las células CAR T anti‑GD2— y por qué en ocasiones fracasa.
Construir un mini tronco encefálico en el laboratorio
El equipo partió de células madre humanas y las guió, paso a paso, para que crecieran en organoides cerebrales tridimensionales que se parecen a la región del tronco encefálico llamada protuberancia (pons), donde suelen originarse estos tumores. Mediante la sincronización precisa de señales de crecimiento, produjeron organoides ricos en los mismos tipos de células gliales ―células de soporte— que normalmente habitan esa zona. Análisis genéticos detallados mostraron que los tipos celulares y su maduración siguieron patrones vistos en el desarrollo cerebral humano temprano, especialmente las líneas gliales típicas de la protuberancia y la médula adyacente. Esto significa que los organoides pueden servir como un trasfondo realista para estudiar cómo comienza y progresa este cáncer.
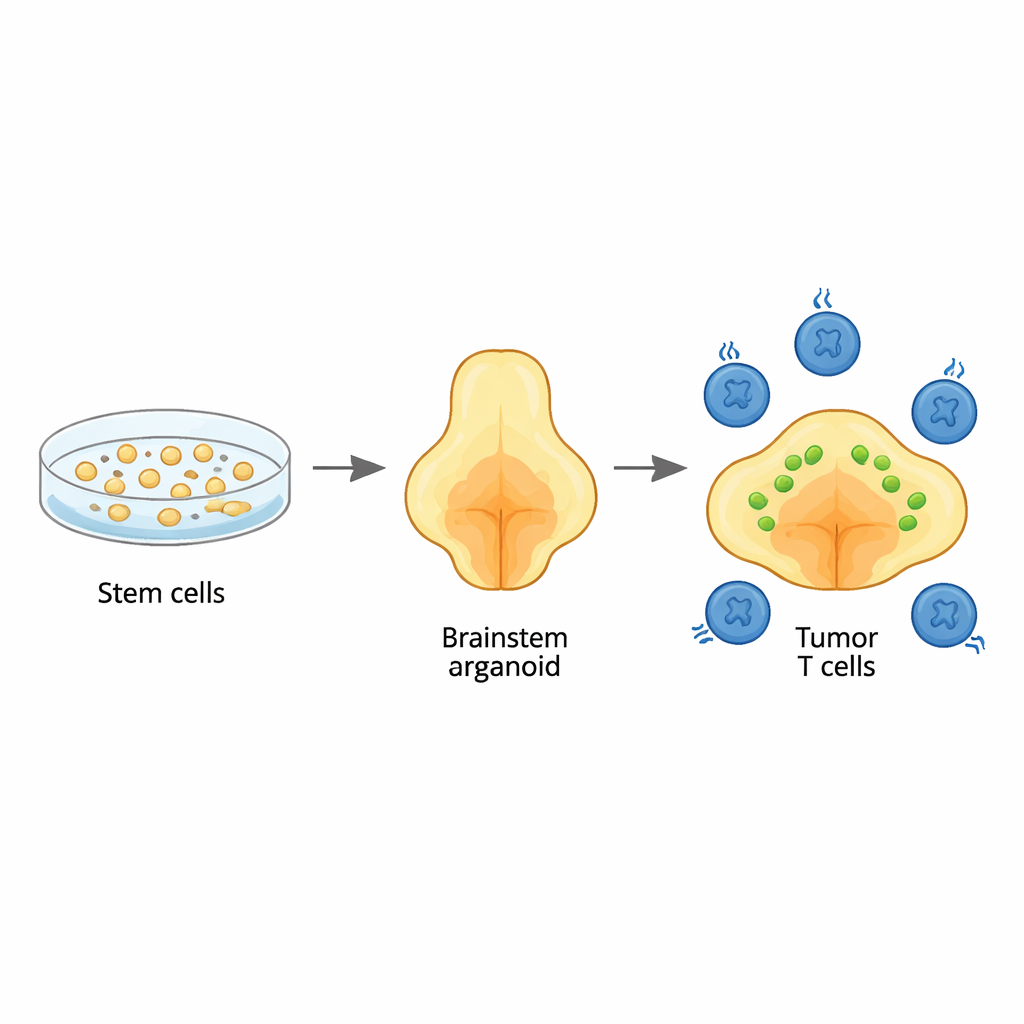
Recrear el tumor infantil dentro del organoide
Para imitar el glioma difuso de línea media, los investigadores introdujeron tres cambios genéticos clave en organoides jóvenes: una mutación distintiva en una proteína histona (H3.3K27M), pérdida del supresor tumoral TP53 y una alteración activadora en el receptor de crecimiento PDGFRA. Cuando se introdujeron en una etapa de desarrollo muy temprana, estas alteraciones convirtieron a células selectas de tipo glial en cancerosas. Los tumores resultantes se diseminaron de forma difusa por los organoides, tal como ocurre en los troncos encefálicos de los niños, y mostraron las mismas firmas amplias de ADN y ARN que se observan en los tumores de pacientes. La secuenciación unicelular reveló una mezcla de estados celulares cancerosos, incluyendo células gliales inmaduras específicas de la protuberancia que coinciden con las encontradas en tumores pediátricos reales, lo que subraya que el modelo recrea fielmente la enfermedad humana.
Observar cómo las inmunoterapias combaten—y se agotan—con el tiempo
Con este modelo de tumor en un tronco encefálico en el plato, el equipo añadió células CAR T anti‑GD2 —linfocitos T de pacientes modificados para reconocer una molécula llamada GD2 en las células tumorales— y siguió tanto el tamaño del tumor como el comportamiento de las T durante hasta un mes. Algunos organoides mostraron una reducción tumoral marcada, otros solo un control parcial, reflejando los resultados variados observados en ensayos clínicos. La secuenciación unicelular de más de 20.000 células CAR T expuestas a los tumores reveló una sorprendente diversidad de estados de las T. Algunas células eran altamente citotóxicas, otras estaban activadas pero no completamente letales, y un grupo distinto mostraba señales de agotamiento, con genes matadores de cáncer atenuados y alta expresión de frenos inhibitorios. Las células agotadas se parecían mucho a las T fatigadas observadas en infecciones crónicas y tumores humanos, lo que indica que el sistema de organoides captura la fatiga T clínicamente relevante impulsada por el contacto continuado con el cáncer.
Encontrar células T potentes pero de corta duración
Al profundizar, los investigadores identificaron un subgrupo de células CAR T marcado por una proteína de superficie llamada NCAM1 que eran asesinas especialmente potentes a corto plazo. Cuando esas células NCAM1‑positivas se aislaron y utilizaron por separado, controlaron los tumores con mayor fuerza al principio que sus contrapartes NCAM1‑negativas. Sin embargo, también se agotaron y disminuyeron más rápido, lo que condujo a un control más débil con el tiempo. Este intercambio entre potencia inmediata y persistencia ayuda a explicar por qué las terapias CAR T pueden producir respuestas espectaculares pero temporales, y sugiere que preseleccionar o remodelar subconjuntos de T podría optimizar la durabilidad del tratamiento.
Cómo las células inmunes del cerebro pueden debilitar la terapia
En el cerebro real, los tumores están rodeados no solo por neuronas y glía, sino también por microglía, las células inmunitarias residentes del cerebro. Para capturar este nivel de complejidad, los científicos añadieron microglía derivada de células madre a sus organoides. Estas células maduraron, adoptaron formas y patrones de expresión génica específicos de la microglía encontrada en glioma difuso de línea media y produjeron moléculas asociadas a un entorno inmunosupresor. Cuando se añadieron células CAR T a organoides con tumor que contenían microglía, las T se desplazaron aún más hacia estados agotados y de baja eficacia, y el control tumoral empeoró. Al mismo tiempo, factores inflamatorios vinculados a efectos secundarios del tratamiento, como IL‑6, aumentaron, lo que sugiere que el modelo también puede ayudar a estudiar las toxicidades relacionadas con las CAR T.
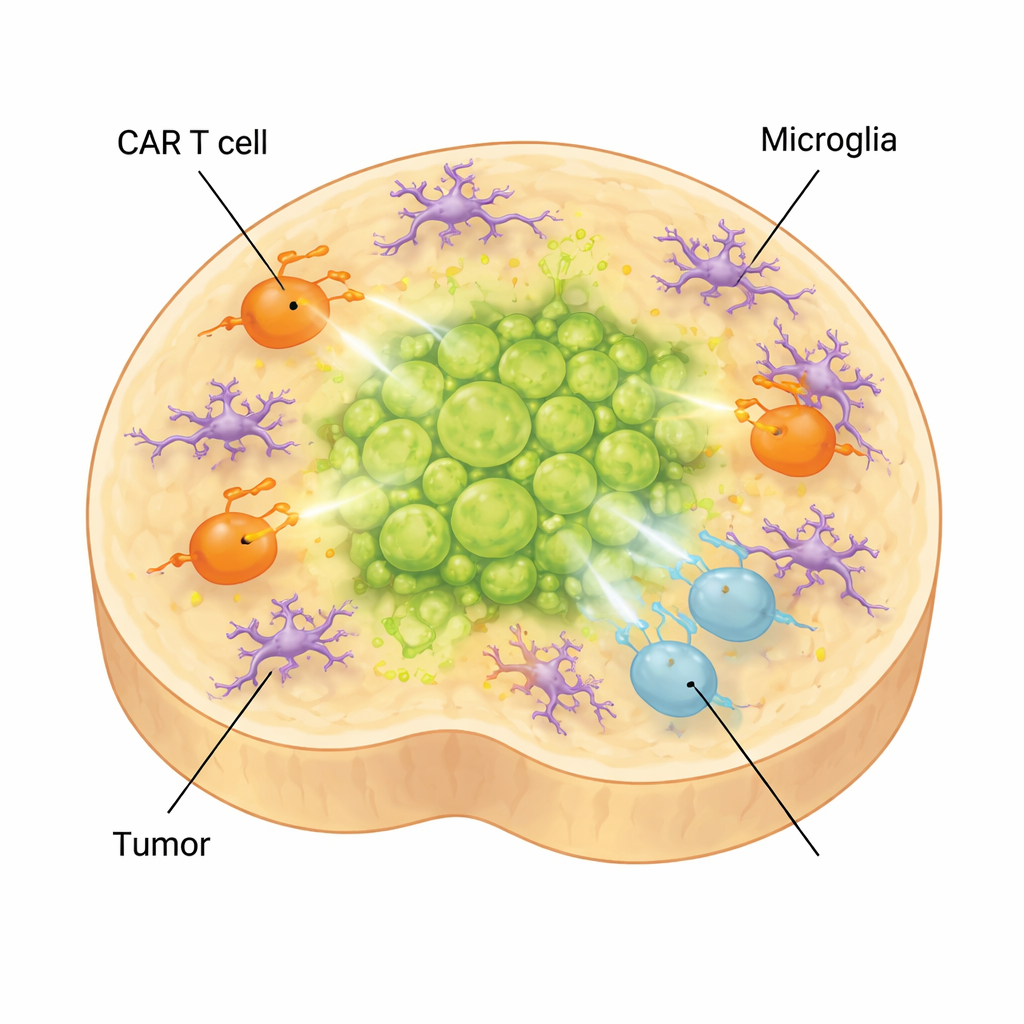
Qué significa esto para los niños con este cáncer
Para las familias afectadas por el glioma difuso de línea media, este trabajo aún no ofrece una cura nueva, pero proporciona un campo de pruebas potente para llegar a ella más rápido. Al recrear el entorno del tronco encefálico del niño y el tumor en un plato, los científicos pueden ahora observar, en tiempo real, cómo interactúan durante semanas distintos tipos de células tumorales, subtipos de células CAR T y la microglía. Esto les permite identificar qué células T diseñadas son más eficaces, cuándo y cómo se agotan, y de qué manera las células inmunes residentes del cerebro socavan sus esfuerzos. En última instancia, dichos modelos de organoides podrían personalizarse para pacientes individuales y utilizarse para afinar inmunoterapias antes de administrarlas, mejorando las probabilidades de que futuras terapias con células CAR T sean tanto más seguras como más efectivas para los niños.
Cita: Bessler, N., Wezenaar, A.K.L., Ariese, H.C.R. et al. De novo H3.3K27M-altered diffuse midline glioma in human brainstem organoids to dissect GD2 CAR T cell function. Nat Cancer 7, 316–333 (2026). https://doi.org/10.1038/s43018-025-01084-0
Palabras clave: glioma difuso de línea media, organoides cerebrales, células CAR T, cáncer cerebral pediátrico, microglía