Clear Sky Science · es
Informe de reutilizabilidad: Evaluación del rendimiento de un modelo fundacional de meta-aprendizaje para predecir la actividad antibacteriana de productos naturales
Buscar nuevos antibióticos, más rápido
La resistencia a los antibióticos está aumentando, pero descubrir fármacos nuevos es un proceso dolorosamente lento y a menudo depende del ensayo y error en el laboratorio. Este estudio explora si un tipo de inteligencia artificial potente, entrenada originalmente con colecciones masivas de datos farmacológicos, puede adaptarse rápidamente para predecir qué compuestos naturales derivados de plantas podrían combatir bacterias, usando solo pequeñas cantidades de nuevos datos experimentales. Si tiene éxito, este tipo de herramienta podría ayudar a los científicos a concentrar el tiempo de laboratorio escaso en los candidatos más prometedores y acelerar la búsqueda de la próxima generación de antibióticos.
Por qué importan los compuestos vegetales
Muchos de nuestros mejores antibióticos comenzaron su vida como productos naturales procedentes de plantas y microbios. Estas moléculas pueden detener el crecimiento bacteriano, pero encontrar nuevas en la naturaleza es algo así como buscar una aguja en un pajar. Los investigadores deben probar muchos compuestos frente a numerosas cepas bacterianas, y cada ensayo tiene un coste. Peor aún, los grandes conjuntos de datos cuidadosamente etiquetados —que los métodos modernos de aprendizaje profundo necesitan para rendir bien— son escasos en este ámbito. Eso convierte el descubrimiento de antibióticos en un terreno ideal para probar “modelos fundacionales”: sistemas de IA grandes y de propósito general que pueden ajustarse para tareas específicas con tan solo unos pocos ejemplos nuevos.
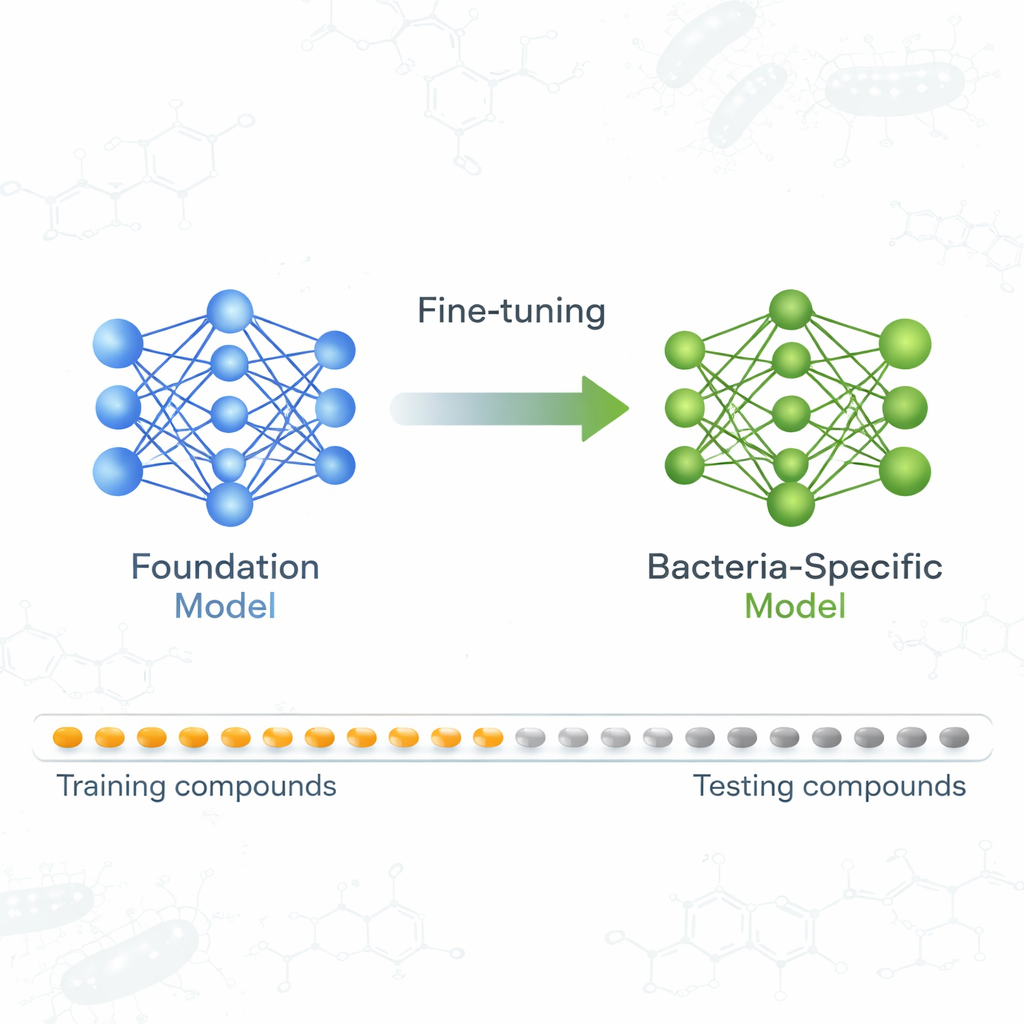
Un modelo fundacional aprende sobre agentes bactericidas
El equipo se centró en un modelo fundacional llamado ActFound, entrenado originalmente para predecir con qué intensidad diferentes químicos afectan a objetivos biológicos, usando conjuntos de datos vastos procedentes de recursos como las bases ChEMBL y BindingDB. En lugar de predecir un solo número para cada compuesto, ActFound aprende comparando pares de compuestos dentro del mismo experimento y estimando cuál es más activo. Este aprendizaje “pareado”, combinado con una estrategia de entrenamiento conocida como meta-aprendizaje, está diseñado para ayudar al modelo a adaptarse rápidamente a nuevas tareas de predicción cuando solo hay un pequeño número de ejemplos etiquetados disponibles—exactamente la situación en muchas pantallas de antibióticos.
Probar el modelo con datos reales de plantas
Para comprobar cuán reutilizable es ActFound, los autores lo ajustaron finamente con un conjunto de datos curado de productos naturales derivados de plantas probados por su capacidad para inhibir el crecimiento de diversas bacterias. Cada cepa bacteriana se trató como su propia tarea, y el modelo se adaptó usando solo entre 8 y 128 compuestos por cepa, o porcentajes fijos de los datos disponibles. También compararon ActFound con modelos más simples de meta-aprendizaje y de transferencia que no emplean comparaciones pareadas. En estas pruebas, ActFound no alcanzó la precisión que había mostrado en trabajos anteriores sobre otros tipos de datos farmacológicos. Sin embargo, cuando había muy pocos datos disponibles—aproximadamente solo unos pocos compuestos por cepa—ActFound y su variante de transferencia generalmente igualaron o superaron a los métodos alternativos.
Cuando la similitud ayuda — y cuando perjudica
ActFound parte de la suposición de que moléculas similares se comportan de manera similar, lo cual funciona bien cuando los conjuntos de datos se construyen alrededor de grupos de químicos relacionados. El conjunto de productos naturales, sin embargo, era químicamente diverso y con frecuencia carecía de “familias” de compuestos estrechamente relacionadas. Esta diversidad, si bien valiosa científicamente, socavó la estrategia de aprendizaje pareado: cuando los compuestos dentro de un experimento son muy diferentes entre sí, al modelo le resulta difícil aprender comparaciones estables. Los autores también hallaron que un diagnóstico sencillo, propuesto en el artículo original de ActFound para predecir de antemano el rendimiento del modelo en una nueva tarea, no se mantuvo con estos datos de productos naturales, lo que subraya una limitación importante al trasladarse a nuevos espacios químicos.
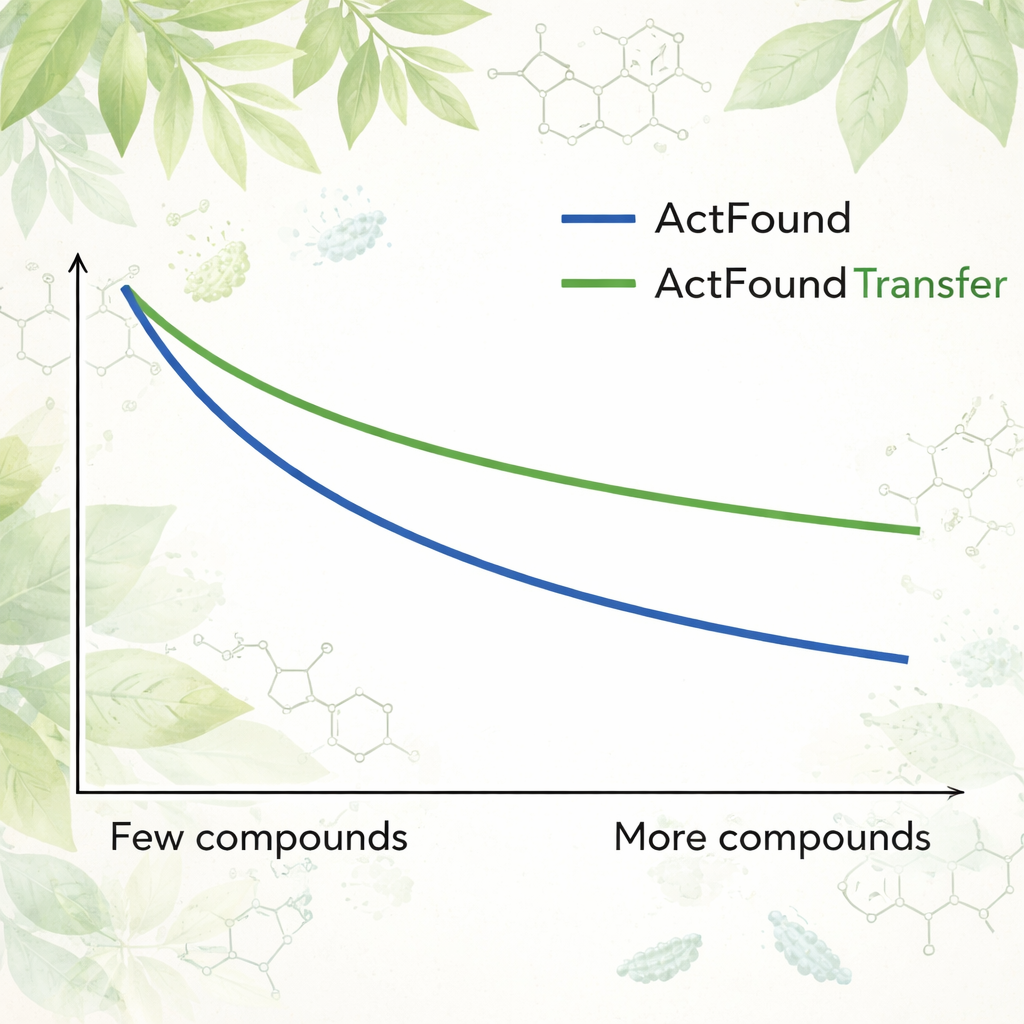
Qué significa esto para el futuro del descubrimiento de fármacos
Para el público general, la conclusión es que los modelos fundacionales como ActFound son herramientas prometedoras para el descubrimiento de fármacos cuando los datos son escasos, pero no son soluciones mágicas. En este estudio, ActFound y su versión de transferencia con frecuencia igualaron o superaron a los métodos competidores cuando solo había disponibles unos pocos compuestos vegetales para el entrenamiento, aunque tuvieron dificultades con este conjunto altamente diverso de productos naturales. El trabajo sugiere que estos modelos de IA son más útiles cuando los datos incluyen muchos compuestos químicamente similares —como en estudios focalizados de relaciones estructura–actividad—, pero siguen siendo menos fiables para predecir el comportamiento de tipos de moléculas completamente nuevos. En otras palabras, la IA puede ayudar a acotar la búsqueda, pero la parte más difícil de explorar territorios químicos realmente nuevos sigue estando por delante.
Cita: Butt, C.M., Walker, A.S. Reusability Report: Evaluating the performance of a meta-learning foundation model on predicting the antibacterial activity of natural products. Nat Mach Intell 8, 270–275 (2026). https://doi.org/10.1038/s42256-026-01187-y
Palabras clave: descubrimiento de antibióticos, productos naturales, aprendizaje profundo, meta-aprendizaje, cribado de fármacos