Clear Sky Science · es
Los ácidos grasos promueven la respiración desacoplada a través de los transportadores ATP/ADP en adipocitos blancos
Por qué las células grasas pueden ayudar a quemar energía
La mayoría de la gente piensa en la grasa corporal como un almacén silencioso de calorías. Este estudio revela un aspecto sorprendentemente activo de los adipocitos blancos: bajo las condiciones adecuadas, pueden desperdiciar combustible y generar calor. Al descubrir una nueva vía por la que las células grasas permiten que la energía "se escape", el trabajo apunta a estrategias novedosas para ayudar al cuerpo a quemar más calorías y, potencialmente, combatir la obesidad.
Cuando la grasa almacenada se convierte de nuevo en combustible
En la vida cotidiana, los adipocitos blancos pasan gran parte del tiempo almacenando energía en forma de triglicéridos: grandes gotículas de grasa. Durante el ejercicio, el ayuno o la exposición al frío, señales de estrés desencadenan que estas células descompongan los triglicéridos en un proceso llamado lipólisis, liberando ácidos grasos y glicerol. Los investigadores confirmaron que cuando esta descomposición se estimula en adipocitos blancos cultivados en el laboratorio, las células aumentan bruscamente su consumo de oxígeno, una señal de que sus centrales energéticas, las mitocondrias, están trabajando más. Bloquear el primer paso de la lipólisis detuvo tanto la liberación de ácidos grasos como el aumento del consumo de oxígeno, lo que demuestra que el proceso depende de los propios ácidos grasos.
Ácidos grasos libres como interruptores de la quema de energía
Los ácidos grasos que salen de la célula adiposa no abandonan todo el tejido; algunos permanecen en su interior. El equipo mostró que estos ácidos grasos libres residuales son clave para aumentar la actividad mitocondrial. Cuando una proteína en el medio de cultivo celular se usó para absorber los ácidos grasos, las células liberaron más grasa en conjunto pero su consumo de oxígeno cayó, lo que indica que los niveles internos altos de ácidos grasos —no solo la lipólisis en general— impulsan la respiración adicional. Por el contrario, bloquear la reesterificación de triglicéridos, una vía que normalmente vuelve a empaquetar los ácidos grasos, elevó el consumo de oxígeno y redujo aún más la diferencia de potencial a través de la membrana mitocondrial. En conjunto, estos hallazgos sugieren que los ácidos grasos libres empujan a las mitocondrias a un modo permeable que desperdicia energía.
Un nuevo actor en la respiración termogénica
En la grasa parda clásica productora de calor, una proteína llamada UCP1 perfora la barrera mitocondrial para que la energía de los alimentos se libere como calor en lugar de almacenarse como combustible celular útil. Los adipocitos blancos tienen poco o nada de UCP1, por lo que los autores buscaron otra vía. Se centraron en el transportador ATP/ADP, una proteína que normalmente intercambia la moneda energética de la célula a través de la membrana mitocondrial. Usando tanto un inhibidor químico específico como herramientas genéticas para reducir este transportador, demostraron que es necesario para la fuga inducida por ácidos grasos: bloquear el transportador preservó la diferencia de potencial mitocondrial e impidió el aumento del consumo de oxígeno durante la lipólisis, aunque la lipólisis en sí transcurriera con normalidad. Esto apunta a que los ácidos grasos libres actúan junto con el transportador para crear una fuga controlada de protones a través de la membrana mitocondrial, activando la respiración desacoplada.
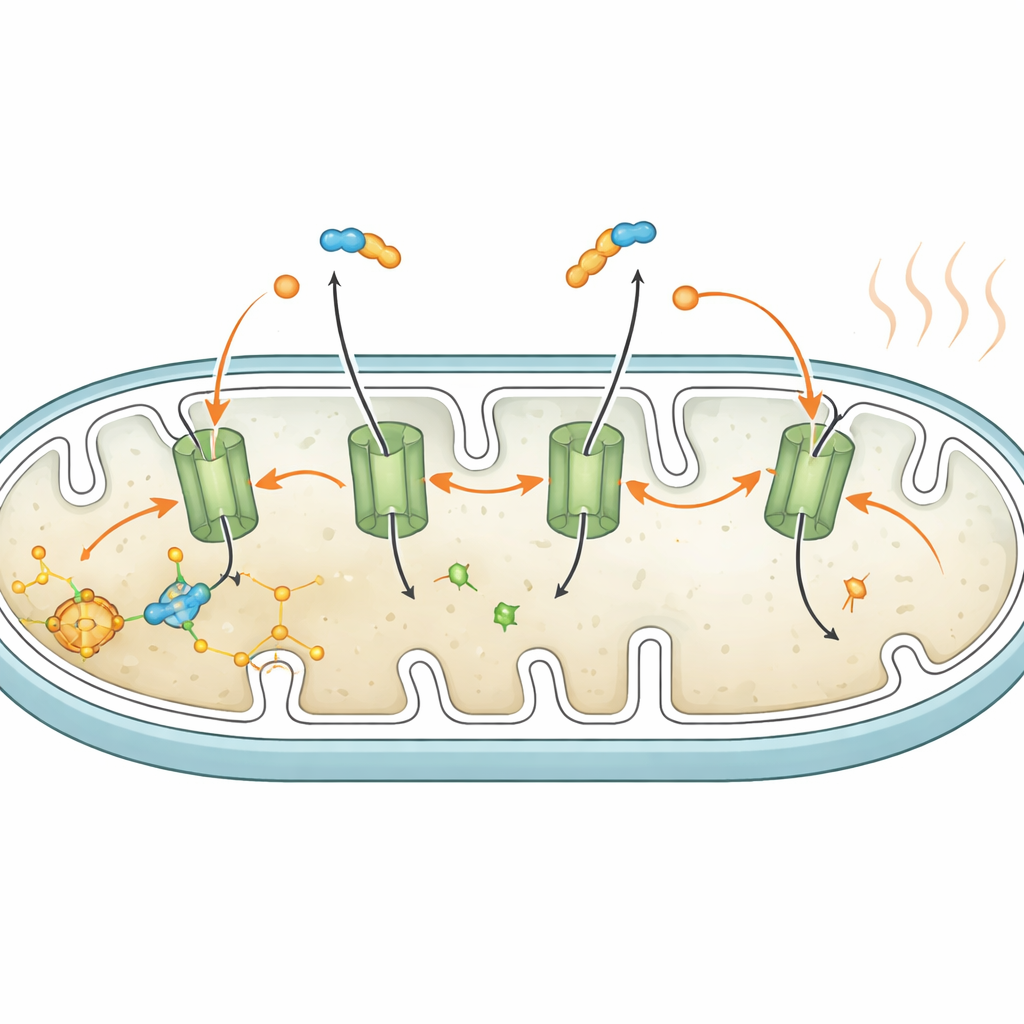
De los cultivos celulares a los animales vivos
Para evaluar si esta fuga de energía importa en animales completos, los investigadores usaron ratones en los que una proteína de señalización llamada STAT3 había sido eliminada específicamente de las células grasas. Estos animales realizan la lipólisis con normalidad pero presentan una respiración dependiente de ácidos grasos reducida en su tejido adiposo blanco. En las condiciones habituales del laboratorio, donde la grasa parda está activa y gestiona la mayor parte de la defensa contra el frío, estos ratones se mantuvieron cálidos como sus compañeros de camada normales. Sin embargo, cuando los animales se volvieron obesos y se mantuvieron a una temperatura en la que la grasa parda está en gran parte inactiva, los ratones sin STAT3 en su tejido graso se volvieron sensibles al frío y mostraron un aumento más débil del consumo global de oxígeno durante la exposición al frío o tras la inducción farmacológica de la lipólisis. Es importante señalar que cambios similares no se observaron cuando STAT3 se eliminó sólo en la grasa parda, lo que señala un papel específico para la grasa blanca.
La grasa blanca como calentador oculto
El estudio concluye que en los adipocitos blancos, los ácidos grasos libres generados durante la lipólisis activa pueden unirse al transportador ATP/ADP en las mitocondrias y desencadenar una fuga de energía que produce calor en lugar de combustible celular útil. En animales obesos mantenidos en ambiente cálido, esta respiración desacoplada en la grasa blanca contribuye de forma significativa a mantener la temperatura corporal y el gasto energético total, especialmente cuando la grasa parda y el escalofrío muscular están limitados. Dado que la grasa blanca es abundante en adultos, particularmente en la obesidad, potenciar suavemente esta fuga podría ofrecer una nueva manera de aumentar la quema de calorías en el día a día y apoyar terapias para la pérdida de peso, siempre que pueda hacerse con seguridad y sin dañar otros tejidos.
Cita: Ahmadian, M., Aksu, A.M., Dhillon, P. et al. Fatty acids promote uncoupled respiration via ATP/ADP carriers in white adipocytes. Nat Metab 8, 572–586 (2026). https://doi.org/10.1038/s42255-026-01467-2
Palabras clave: tejido adiposo blanco, ácidos grasos, desacoplamiento mitocondrial, termogénesis, obesidad