Clear Sky Science · es
PFKM gobierna los cambios metabólicos durante la diferenciación del músculo esquelético
Por qué las células musculares necesitan un uso inteligente del azúcar
Cuando hacemos ejercicio o simplemente nos levantamos de una silla, nuestros músculos esqueléticos entran en acción, quemando azúcares para impulsar cada contracción. Pero las células madre musculares jóvenes y las fibras musculares completamente formadas no gestionan la glucosa de la misma manera. Este estudio revela un sistema de conmutación integrado—centrado en una única enzima llamada PFKM—que decide si la glucosa se quema para obtener energía inmediata o se desvía para proteger y reconstruir las células. Comprender este interruptor podría abrir nuevas vías para tratar la debilidad muscular, el envejecimiento muscular y enfermedades metabólicas hereditarias.
Un semáforo para el combustible celular
La glucosa que entra en una célula puede seguir varias rutas. Una vía principal, la glucólisis, convierte rápidamente el azúcar en energía y en bloques de construcción para las fibras musculares en crecimiento. Otra ruta, la vía de las pentosas fosfato, genera moléculas que protegen a las células contra el estrés oxidativo y respaldan la síntesis de ADN y lípidos. Los investigadores se centraron en PFKM, una isoforma de la enzima fosfofructoquinasa‑1 que ocupa un punto clave en la glucólisis. Midiendo cientos de metabolitos durante minutos a horas tras activar una señal de crecimiento llamada Wnt, encontraron que las células acumulaban rápidamente intermediarios tempranos de la glucólisis mientras caía el producto de PFKM, y aumentaban los metabolitos de la vía de las pentosas fosfato. Esto sugiere que las células estaban modulando activamente PFKM para desviar la glucosa hacia química protectora en lugar de pura producción de energía. 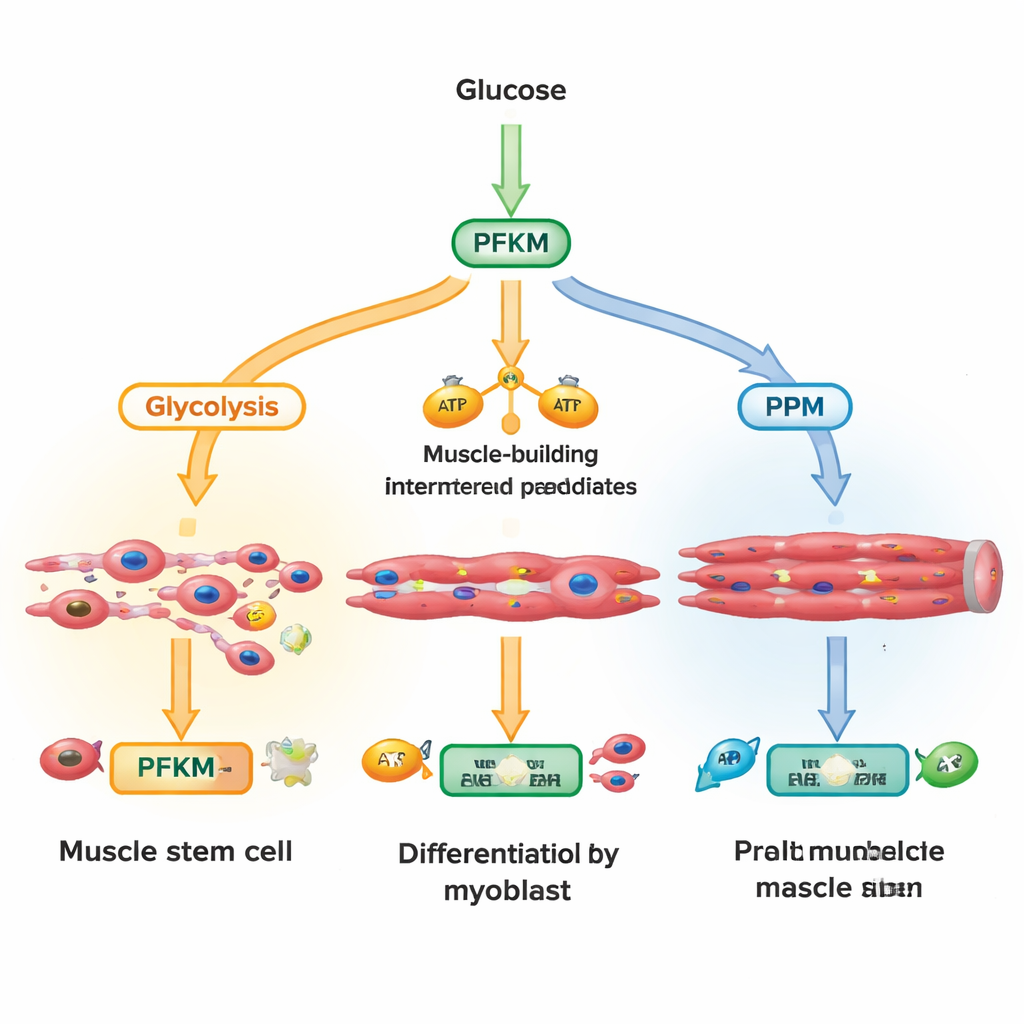
Etiquetar y eliminar la enzima guardiana
Para entender cómo se controla PFKM, el equipo rastreó dónde se localiza la proteína dentro de las células. En reposo, PFKM se distribuía por todo el citoplasma. En pocos minutos tras la estimulación por Wnt, se agrupó en puntos brillantes que se solapaban con lisosomas, los compartimentos celulares encargados de destruir proteínas. Dos isoformas hermanas, PFKL y PFKP, no se movieron ni cambiaron de niveles, lo que reveló que solo la variante muscular PFKM era el blanco. Pruebas bioquímicas mostraron que bloquear la función lisosomal impedía la pérdida de PFKM, mientras que inhibir el proteasoma—el otro gran sistema de eliminación de proteínas—no tenía efecto. El análisis de secuencias identificó un breve motivo único en PFKM denominado “degrón de metil‑arginina”. La enzima PRMT1 añadió una marca de metilación específica en una arginina dentro de ese motivo, y esta etiqueta permitió a la maquinaria de microautofagia, incluido el proteína VPS4, incorporar PFKM en los lisosomas para su degradación. Inactivar PRMT1 o VPS4 estabilizó PFKM y bloqueó su eliminación.
De la célula madre a la fibra muscular funcional
Utilizando grandes conjuntos de datos de una sola célula humanos, los autores cartografiaron los niveles de PFKM en muchos tipos celulares musculares. Las células madre musculares, que permanecen en estado latente hasta que se necesitan para la reparación, tenían muy poca PFKM pero expresaban numerosos genes de la vía de las pentosas fosfato y componentes lisosomales. A medida que las células se comprometían a convertirse en músculo y se fusionaban en fibras multinucleadas, los transcritos y las proteínas de PFKM aumentaron bruscamente, mientras que los genes diana de Wnt y los genes lisosomales disminuyeron. En células musculares humanas y de ratón cultivadas, Wnt llevó rápidamente a PFKM hacia los lisosomas en células tempranas de núcleo único, pero no en fibras maduras multinucleadas. Este patrón respalda un modelo en el que las células indiferenciadas mantienen PFKM bajo—mediante degradación lisosomal—para favorecer el metabolismo protector, y luego lo vuelven a expresar al transitar hacia fibras contráctiles con alta demanda energética.
Qué sucede cuando el interruptor se queda atascado
Para probar cuán crucial es PFKM en la formación muscular, el equipo redujo sus niveles mediante interferencia de ARN. Las células con baja PFKM tuvieron dificultades para activar genes característicos del músculo, produjeron menos proteína miosina y formaron menos y menores fibras multinucleadas, aunque el número total de células no cambió. El perfil de metabolitos reveló una reducción de intermediarios glucolíticos posteriores y de combustibles del ciclo de los ácidos tricarboxílicos, pero un aumento de genes y marcadores de la vía de las pentosas fosfato, junto con una mayor resistencia al estrés oxidativo. De manera importante, suministrar a las células 3‑fosfoglicerato—un intermediario glucolítico que normalmente se encuentra aguas abajo de PFKM—rescató muchos de los defectos de diferenciación. Los marcadores musculares y la formación de fibras se recuperaron, lo que demuestra que los metabolitos faltantes, más que la ausencia de la proteína PFKM en sí, eran el principal cuello de botella. 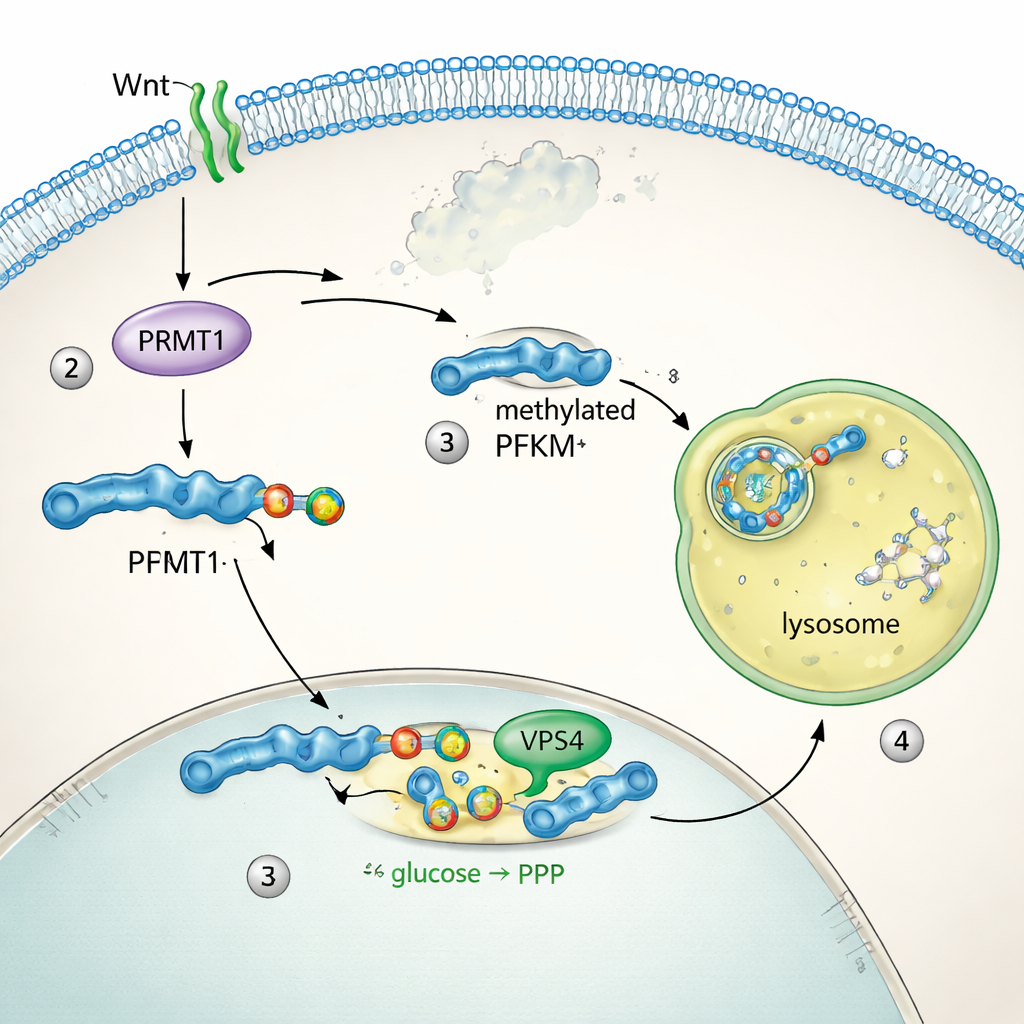
Implicaciones para la salud y la reparación muscular
Para un público no especialista, el mensaje central es que las células musculares no se limitan a “quemar azúcar” más o menos; redirigen cuidadosamente la glucosa entre producción de energía y protección celular según su etapa vital. PFKM actúa como una válvula controlable en este cruce. En células de tipo madre, la etiquetación impulsada por Wnt y la destrucción lisosomal de PFKM reorientan la glucosa hacia una vía que protege a las células y las prepara para un crecimiento futuro. A medida que las células maduran en fibras funcionales, reconstruyen los niveles de PFKM y orientan el metabolismo hacia un uso energético de alta potencia. Alterar este equilibrio, como ocurre en los raros trastornos por deficiencia de PFKM, descarrila el desarrollo muscular normal. Al descubrir el controlador molecular de este interruptor, el estudio sugiere que futuras terapias podrían afinar la regeneración muscular o proteger los músculos en enfermedades y el envejecimiento mediante un ajuste moderado de la actividad de PFKM o suministrando los metabolitos adecuados aguas abajo.
Cita: Campos, M., Nguyen, S.T., Kong, X. et al. PFKM governs metabolic shifts throughout skeletal muscle differentiation. Nat Metab 8, 489–505 (2026). https://doi.org/10.1038/s42255-026-01457-4
Palabras clave: diferenciación del músculo esquelético, metabolismo de la glucosa, enzima PFKM, vía de las pentosas fosfato, degradación lisosomal de proteínas