Clear Sky Science · es
Expresión ectópica de DHODH citosólico desacopla la biosíntesis de novo de pirimidinas del transporte de electrones mitocondrial
Por qué importa romper un vínculo oculto en nuestras células
Cada célula de tu cuerpo debe copiar y reparar su ADN constantemente, un proceso que exige un suministro continuo de “letras” químicas llamadas pirimidinas. En la mayoría de los animales, la producción de estas letras está estrechamente ligada a cómo las mitocondrias —las centrales energéticas de la célula— queman combustible usando oxígeno. Ese acoplamiento significa que cuando la respiración mitocondrial falla, los bloques para construir ADN escasean y las células pierden capacidad de proliferar. El estudio resumido aquí muestra que tomar prestado un único gen de la levadura de pan puede desacoplar de manera limpia estos dos procesos. Ese ajuste genético permite a las células de mamífero seguir fabricando las letras del ADN incluso cuando sus mitocondrias están dañadas, abriendo una nueva vía para estudiar, y quizá algún día tratar, enfermedades impulsadas por un metabolismo energético defectuoso.
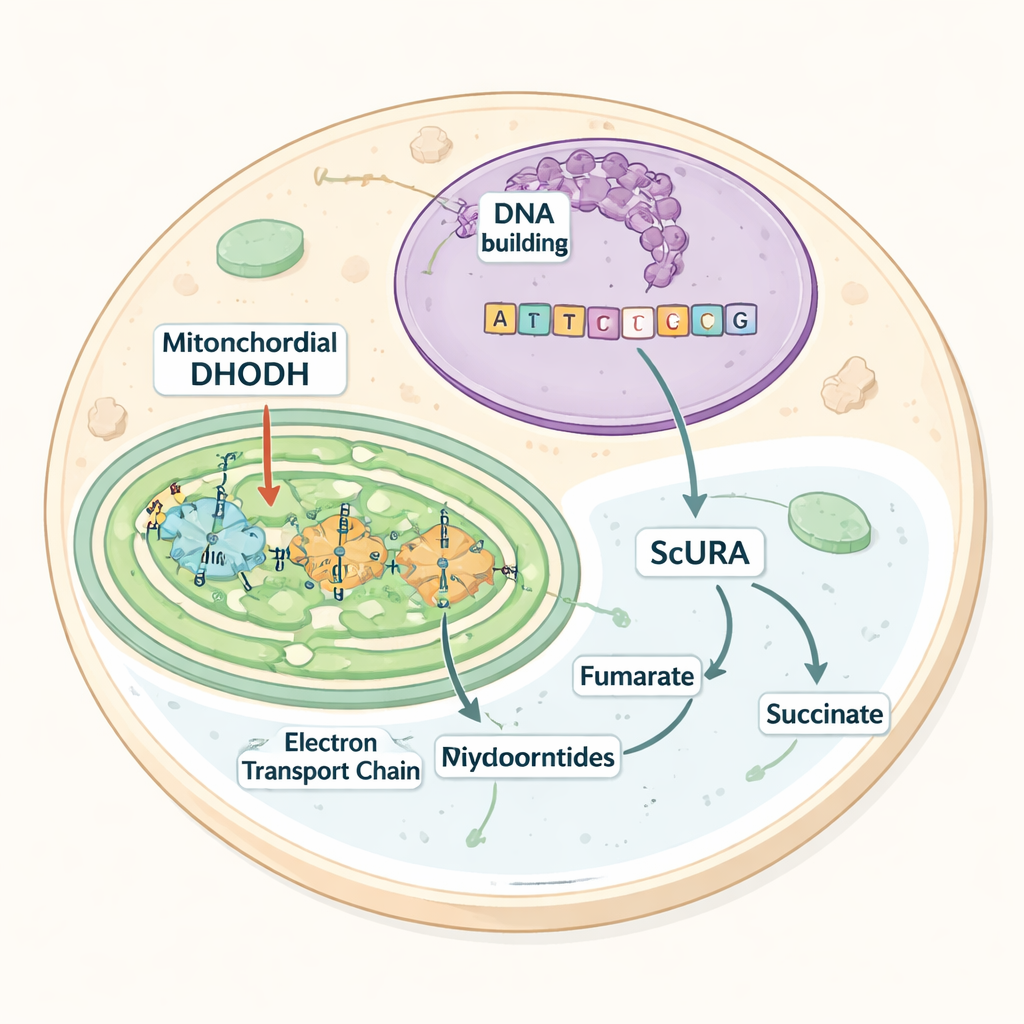
Una herramienta tomada prestada de la levadura
El trabajo se centra en una enzima llamada dihidroorotato deshidrogenasa (DHODH), que realiza un paso clave en la síntesis de pirimidinas. En los mamíferos, la DHODH se localiza en la membrana interna mitocondrial y transfiere electrones a una molécula transportadora que alimenta la cadena respiratoria. Si ese flujo de electrones se bloquea —por ejemplo, por inhibidores farmacológicos o por defectos genéticos— la DHODH se detiene, la producción de pirimidinas cesa y las células pasan a depender de uridina dietaria o suministrada, un bloque prefabricado. Muchos microbios que prosperan sin oxígeno evitan este cuello de botella usando versiones alternativas de DHODH que flotan en el citosol y emplean aceptores de electrones distintos. Los autores se preguntaron si podrían introducir tal vía independiente del oxígeno en células de mamífero.
Reconfigurar cómo se hacen las letras del ADN
Los investigadores introdujeron el gen URA1 de la levadura Saccharomyces cerevisiae en células humanas. URA1 codifica una enzima citosólica, llamada ScURA, que realiza el mismo paso químico que la DHODH mitocondrial pero cede electrones a una molécula llamada fumarato en lugar de al transportador mitocondrial. Ensayos bioquímicos mostraron que ScURA formaba dímeros activos en el citosol y añadía una actividad DHODH resistente a fármacos. En condiciones normales, la adición de ScURA no perturbó la estructura mitocondrial, la respiración ni el crecimiento, lo que indica que actúa como una vía de respaldo más que como una carga adicional.
Células que sortean los obstáculos mitocondriales
Para ver si esta vía de reserva podía sustituir al sistema nativo, el equipo bloqueó químicamente ya fuera la DHODH o la cadena de transporte de electrones mitocondrial, tratamientos que normalmente detienen la división celular salvo que se aporte uridina. Las células que expresaban ScURA continuaron proliferando sin ayuda alguna, incluso bajo una fuerte inhibición del complejo III respiratorio o tras la eliminación genética del gen DHODH endógeno. El trazado detallado de átomos de nitrógeno y carbono a partir de glutamina marcada mostró que las células con ScURA seguían sintetizando nucleótidos de pirimidina a pesar de estos bloqueos. Las mediciones de metabolitos revelaron que, en lugar de acumular precursores tóxicos, las células ScURA canalizaban electrones hacia el fumarato, produciendo succinato y remodelando sutilmente el ciclo de los ácidos tricarboxílicos (TCA) para sustentar un intercambio fumarato–succinato entre citosol y mitocondrias.
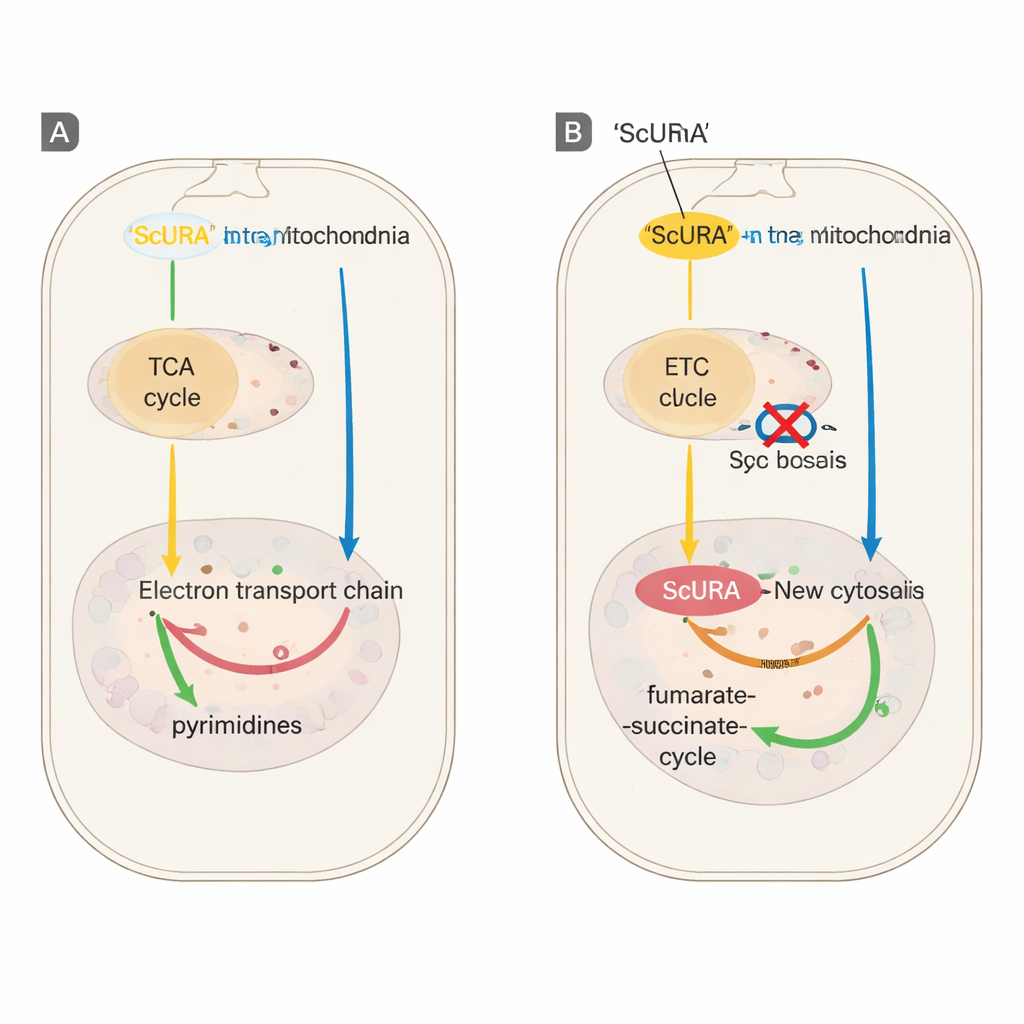
Rescatando células con centrales eléctricas dañadas
Los autores probaron luego ScURA en modelos celulares de enfermedad mitocondrial. Las células carentes de ADN mitocondrial, o que portaban mutaciones que inutilizan los complejos respiratorios III o IV, normalmente dependen de uridina añadida para crecer. Una vez diseñadas para expresar ScURA, estas diversas células mutantes pudieron proliferar sin uridina, aunque todavía requerían piruvato, lo que refleja una necesidad remanente de cierta actividad mitocondrial. A nivel de expresión génica, ScURA también evitó el apagado de genes de proteínas ribosomales que suele seguir a la inhibición crónica del transporte de electrones, al mantener las reservas de bloques de pirimidina lo bastante altas como para sostener la producción de ARN.
Qué significa esto para la salud y la enfermedad
Al separar de forma limpia la síntesis de pirimidinas de la respiración mitocondrial, ScURA ofrece a los investigadores una nueva palanca poderosa: ahora pueden preguntar, en muchos contextos, si un defecto o el efecto de un fármaco se deben realmente a la pérdida de producción de energía o, en cambio, a la escasez de precursores de ADN y ARN. A largo plazo, estrategias similares podrían complementar las terapias génicas existentes para trastornos mitocondriales, o ayudar a explicar por qué algunos tumores dependen tanto de restaurar su función mitocondrial. Aunque traducir una enzima de levadura a un tratamiento humano requerirá gran cautela, este estudio demuestra que un único gen bien elegido puede reescribir una conexión metabólica fundamental que la evolución ha mantenido entrelazada durante mucho tiempo.
Cita: Curtabbi, A., Jaroszewicz, S.N., Sanz-Cortés, R. et al. Ectopic expression of cytosolic DHODH uncouples de novo pyrimidine biosynthesis from mitochondrial electron transport. Nat Metab 8, 454–466 (2026). https://doi.org/10.1038/s42255-026-01454-7
Palabras clave: metabolismo de pirimidinas, función mitocondrial, cadena de transporte de electrones, reconfiguración metabólica, enfermedad mitocondrial