Clear Sky Science · es
El metabolismo del glucógeno regulado por la alimentación impulsa la secreción rítmica de proteínas del hígado
Por qué importa el ritmo diario del hígado
La mayoría de nosotros pensamos en lo que comemos, pero no en cuándo el hígado empaqueta y envía silenciosamente proteínas vitales al torrente sanguíneo. Este estudio revela que el “horario de envío” de proteínas del hígado está lejos de ser constante: sigue un ritmo diario que depende en gran medida de cuándo comemos y de cómo el hígado usa el azúcar almacenado, conocido como glucógeno. Comprender este sistema temporizador ayuda a explicar por qué la hora de las comidas, la obesidad y ciertas enfermedades genéticas raras pueden alterar hormonas, factores de coagulación y muchas otras proteínas plasmáticas que mantienen el equilibrio del organismo.
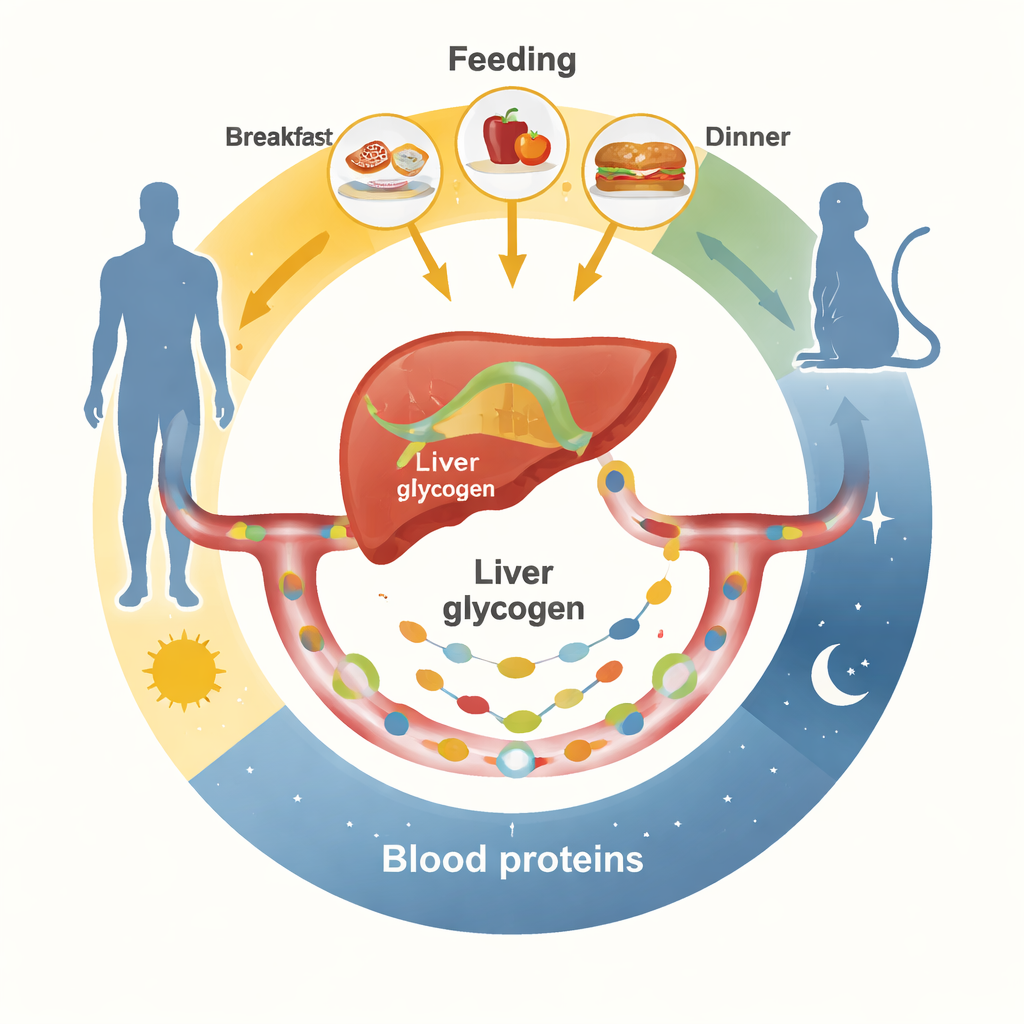
Las comidas marcan el compás de las proteínas sanguíneas
Los investigadores primero siguieron cientos de proteínas sanguíneas durante 24 horas en hombres sanos bajo dos patrones de alimentación controlados. En uno, los voluntarios comían comidas regulares; en el otro, las mismas calorías totales se distribuían de forma continua a lo largo del día despierto. Con comidas regulares, muchas proteínas sanguíneas subieron y bajaron en olas diarias claras, con picos a menudo alrededor de primera hora de la mañana y a última hora de la tarde. Entre ellas figuraban hormonas metabólicas, factores de coagulación, proteínas inmunitarias y transportadores fabricados en gran parte por el hígado. Cuando los alimentos se consumieron lentamente y de forma continuada, la mayoría de estos ritmos se aplanaron. Experimentos similares en ratones, con alimento disponible todo el tiempo o solo en ventanas definidas de día o noche, mostraron que cambiar los horarios de alimentación remodelaba de forma contundente qué proteínas en la sangre eran rítmicas y cuándo alcanzaban su pico.
La vía secretora del hígado funciona con un reloj
Para averiguar cómo surgen estos patrones, el equipo examinó el interior del hígado. Encontraron que las proteínas implicadas en la clásica “vía secretora” —donde las proteínas recién sintetizadas entran en el retículo endoplásmico (RE), se modifican en el aparato de Golgi y luego se liberan— también subían y bajaban a lo largo del día. En lugar de ser una cinta transportadora constante, esta vía está afinada por la hora del día. La mayoría de las proteínas sanguíneas rítmicas llevaban los “péptidos señal” moleculares que las marcan para esta vía, y bloquear el transporte RE–Golgi en rodajas de hígado de ratón redujo drásticamente la liberación de proteínas. En contraste, marcadores de daño celular y degradación proteica no mostraron cambios diarios pronunciados, lo que indica que es la secreción, no la destrucción, la que impulsa principalmente los ritmos observados en la sangre.
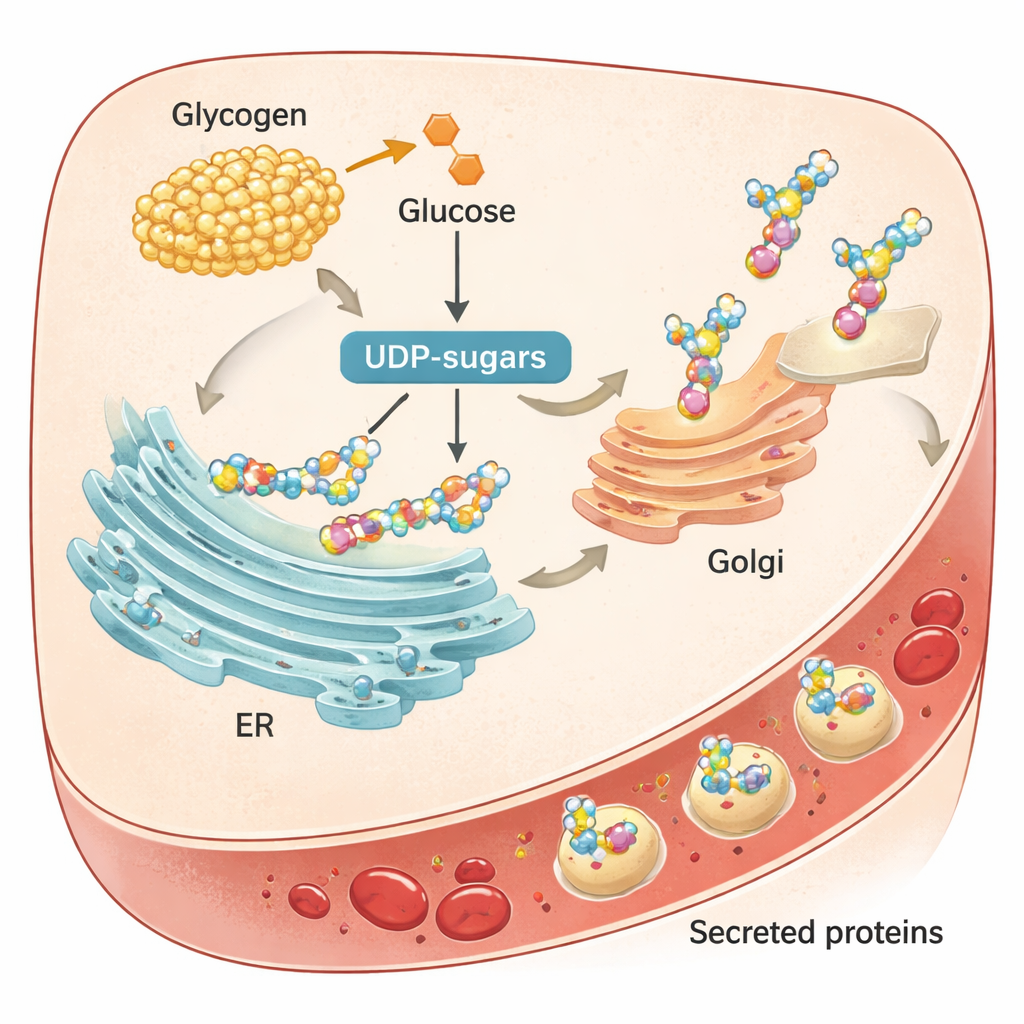
Glucógeno: azúcar almacenada que alimenta el empaquetado de proteínas
Los autores relacionaron entonces estos efectos temporales con la forma en que el hígado gestiona el glucógeno, su principal reserva de carbohidratos. Tras las comidas, el hígado acumula glucógeno; durante el ayuno, degrada glucógeno, un proceso llamado glucogenólisis. Los productos de esa degradación alimentan los “UDP-azúcares”, las unidades de azúcar activadas que se usan para decorar proteínas con cadenas de azúcar, una modificación llamada glicosilación. En ratones, los niveles de UDP-azúcares oscilaron fuertemente a lo largo del día, al compás de la actividad de enzimas que sintetizan y degradan glucógeno. Cuando el equipo bloqueó la enzima clave de la glucogenólisis hepática PYGL con un fármaco, el glucógeno se acumuló, la glucemia disminuyó durante el ayuno y el suministro de UDP-azúcares cayó. Esto condujo a menos glicosilación de proteínas hepáticas, señales de estrés en el RE y una reducción en la secreción de varias proteínas importantes al torrente sanguíneo.
Señales de estrés y vínculos con enfermedades
Interrumpir la degradación del glucógeno hizo algo más que frenar la exportación de proteínas; activó el sistema de alarma de control de calidad celular. Las células hepáticas tratadas con el fármaco inhibidor de PYGL activaron la respuesta a proteínas mal plegadas, un conjunto de vías de estrés del RE que pueden aumentar la degradación proteica y alterar selectivamente qué proteínas se secretan. En ratones obesos, que de forma natural presentan un manejo alterado del glucógeno, las oscilaciones diarias normales del glucógeno se atenúan y el número de proteínas sanguíneas rítmicas disminuye. Lo mismo se observó cuando ratones sanos siguieron una alimentación con tiempo restringido que efectivamente redujo las calorías. Finalmente, en un gran estudio genético humano, personas portadoras de variantes en genes ligados a enfermedades de almacenamiento de glucógeno o a trastornos congénitos de glicosilación mostraron niveles alterados de muchas proteínas sanguíneas, reforzando el vínculo entre el metabolismo del glucógeno, la glicosilación proteica y la secreción.
Qué significa esto para la salud cotidiana
Para un público no especializado, el mensaje es que el hígado opera un negocio de exportación temporizado de proteínas sanguíneas, usando el azúcar almacenado como combustible que posibilita un correcto empaquetado y liberación. Cuando los patrones de alimentación, los relojes internos o los genes que procesan glucógeno se alteran, este horario falla, cambiando los niveles de hormonas, factores de coagulación y proteínas inmunitarias en la sangre. Estos cambios pueden ayudar a explicar por qué la hora de las comidas, la obesidad y ciertas condiciones metabólicas raras se asocian con problemas de salud de amplio espectro. El trabajo sugiere que no solo importa lo que comemos, sino cuándo lo hacemos, pues puede influir en el ritmo diario de envío del hígado, y que los médicos podrían necesitar considerar la hora del día y los horarios de alimentación al interpretar análisis de sangre.
Cita: Weger, M., Mauvoisin, D., Hoyle, D. et al. Feeding-regulated glycogen metabolism drives rhythmic liver protein secretion. Nat Metab 8, 327–349 (2026). https://doi.org/10.1038/s42255-026-01453-8
Palabras clave: ritmo circadiano, glucógeno hepático, secreción de proteínas, hora de las comidas, metabolismo