Clear Sky Science · es
El flujo catabólico de cisteína regulado por Lamin A/C modula el destino celular de las células madre mediante la reprogramación del epigenoma
Cómo el esqueleto celular dialoga con su metabolismo
¿Por qué algunas células se mantienen jóvenes y con flexibilidad en lo que pueden llegar a ser, mientras otras envejecen o quedan atrapadas en una identidad equivocada? Este estudio revela una conversación sorprendente dentro de nuestras células entre el “andamiaje” nuclear que organiza el ADN y un nutriente que contiene azufre, la cisteína. Al mostrar cómo este diálogo dirige a las células madre hacia destinos saludables —o hacia un envejecimiento prematuro—, el trabajo sugiere que lo que las células “comen” y cómo lo procesan podría alguna vez ajustarse para prevenir ciertas enfermedades genéticas y quizá ralentizar aspectos del envejecimiento.
El papel oculto de la cubierta nuclear
En el interior de cada célula, el ADN está presionado contra una malla proteica llamada lámina nuclear, formada en parte por proteínas llamadas lamin A y C. Estos laminados no solo dan forma al núcleo; también ayudan a decidir qué genes quedan bloqueados y cuáles permanecen accesibles. Los autores estudiaron células madre embrionarias de ratón en su estado más flexible, o “naive”, y comprobaron que lamin A/C normalmente restringe a dos enzimas metabólicas, CBS y CTH, que participan en la síntesis y degradación de la cisteína. Cuando lamin A/C está presente y activo, estas enzimas se mantienen bajo control y el procesamiento de la cisteína es bajo, lo que sostiene un estado estable y juvenil de las células madre. 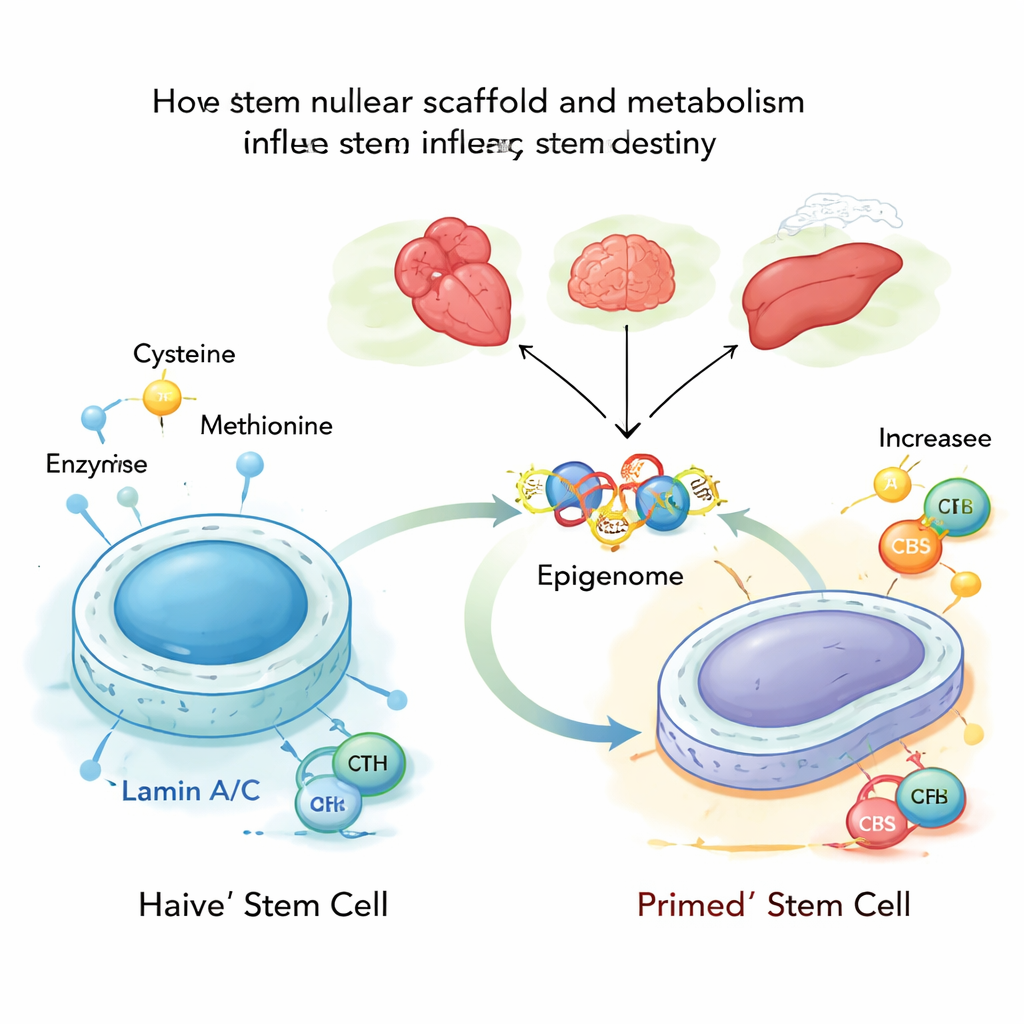
Cuando la estructura falla, el metabolismo se acelera
Después, los investigadores eliminaron lamin A/C o introdujeron una mutación asociada a una enfermedad que imita un trastorno humano de envejecimiento prematuro llamado progeria de Hutchinson–Gilford. Sin lamin A/C normal, los genes CBS y CTH se vuelven más accesibles y presentan una mayor unión por un factor de transcripción llamado SP1, activándolos. Ese cambio empuja más cisteína a través de una vía metabólica que termina en acetil‑CoA, una molécula pequeña que transporta grupos acetilo usados para aflojar el empaquetamiento del ADN. A medida que más cisteína se canaliza hacia acetil‑CoA, los grupos acetilo se añaden preferentemente a lugares específicos en las histonas —especialmente en dos posiciones de la histona H3 conocidas como K9 y K27—, facilitando que los genes cercanos se activen.
De las etiquetas químicas a las decisiones de destino celular
Estos cambios en las “etiquetas” de las histonas actúan como una recalibración global del panel de control de la célula. En las células madre naive, aumentar CBS y CTH, o simplemente suministrar más cisteína, impulsa a las células hacia un estado más avanzado, “primed”, que está más cerca de formar tejidos reales. Los genes implicados en el desarrollo cardíaco y otras líneas celulares se vuelven más activos, y el plegamiento tridimensional del ADN cambia para favorecer estos programas. Por el contrario, reducir CBS y CTH o limitar la cisteína ayuda a restaurar una identidad más naive y juvenil incluso cuando la lámina nuclear está dañada. En modelos embrionarios, este fallo metabólico condujo a una formación desequilibrada de las tres capas germinales —los primeros bloques de construcción de todos los órganos— y a un sesgo anómalo hacia las células del músculo cardíaco a menos que CBS y CTH se reajustaran. 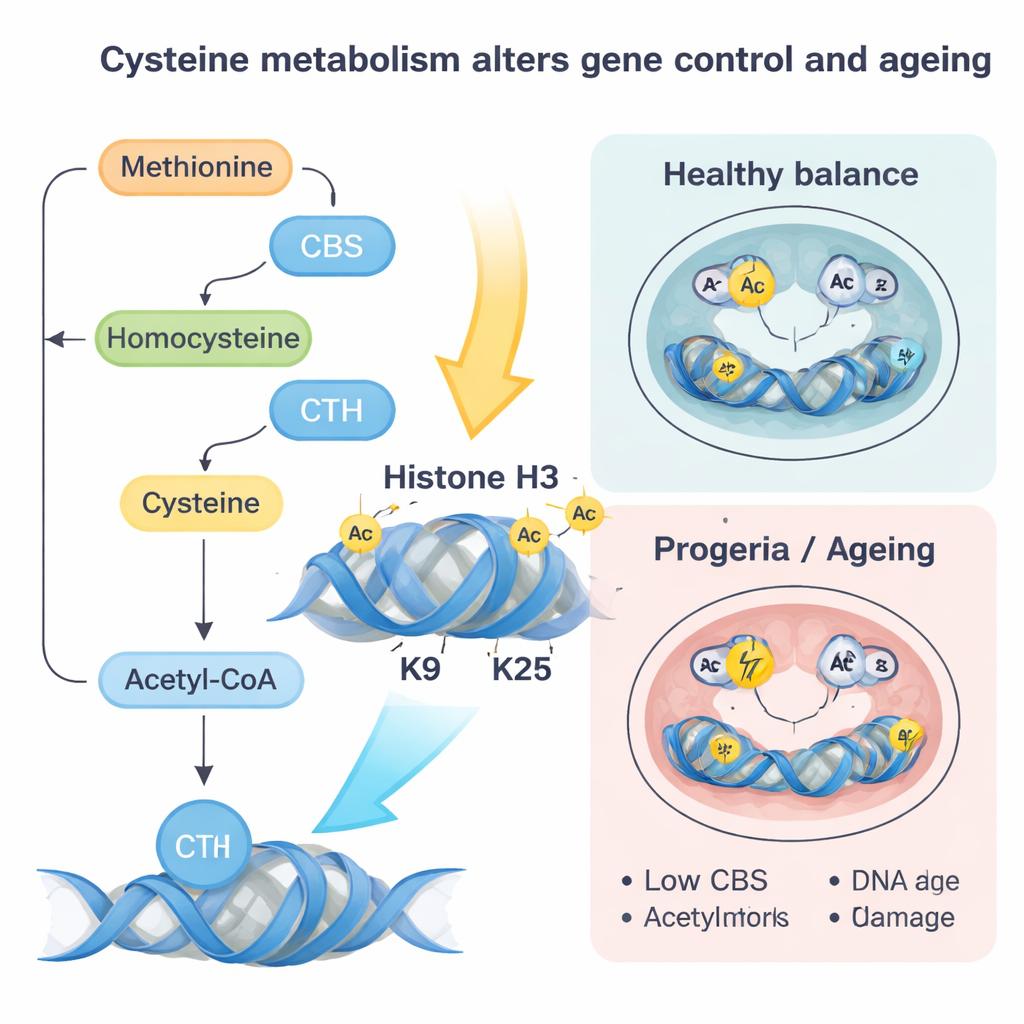
Metabolismo, marcas del ADN y envejecimiento prematuro
La mutación de lamin similar a la progeria contó una historia complementaria. Aquí, los niveles de CBS y CTH disminuyen, reduciendo el flujo de cisteína y la producción de acetil‑CoA por esta vía. Al mismo tiempo, la homocisteína se desvía de nuevo al ciclo de la metionina, aumentando los niveles de SAM, el donante universal de grupos metilo. Esto favorece etiquetas de metilación adicionales, en particular una marca llamada H3K9me3 puesta por la enzima SUV39H1, que compacta la cromatina y se asocia a una reparación del ADN deficiente. Los autores mostraron que restaurar suavemente CBS o restringir la metionina disminuía el SAM, reducía estas marcas metilantes represivas, mejoraba la reparación del ADN, reducía el estrés oxidativo y los marcadores de senescencia, y rescataba parcialmente la diferenciación de células cardíacas. Descensos similares de CBS y aumentos de marcas represivas se observaron en corazones de ratones envejecidos de forma natural y en fibroblastos humanos de personas mayores y pacientes con progeria, lo que sugiere que este circuito también opera en el envejecimiento natural.
Qué significa esto para la salud y el envejecimiento
Para un público no especializado, la idea es que el armazón estructural de la célula y su metabolismo están estrechamente vinculados: cuando la cubierta nuclear formada por lamin A/C se altera, cambia la forma en que se utiliza la cisteína, lo que a su vez reescribe marcas químicas en las proteínas que empaquetan el ADN. Estas marcas deciden qué genes se activan mientras las células madre construyen el cuerpo y ayudan a determinar qué tan bien las células reparan el daño a lo largo de la vida. Al ajustar con cuidado enzimas como CBS y CTH —o regulando el suministro de nutrientes como la metionina y la cisteína— podría ser posible corregir parte de la mala escritura de estas marcas en enfermedades basadas en laminas y quizás mitigar aspectos del envejecimiento prematuro o normal.
Cita: Wang, Y., Shi, H., Wittig, J. et al. Lamin A/C-regulated cysteine catabolic flux modulates stem cell fate through epigenome reprogramming. Nat Metab 8, 431–453 (2026). https://doi.org/10.1038/s42255-025-01443-2
Palabras clave: células madre, lámina nuclear, metabolismo de la cisteína, epigenética, envejecimiento