Clear Sky Science · es
ABEL-FRET salva la brecha temporal en mediciones de una sola molécula de la dinámica estructural del receptor de adenosina A2A
Observando pequeños interruptores celulares en tiempo real
Muchos de los medicamentos actuales actúan al cambiar «interruptores» moleculares en la superficie celular, denominados receptores. Estos interruptores cambian de forma constantemente al activar o apagar señales, pero la mayoría de las herramientas solo puede ver los movimientos más rápidos o los más lentos, no ambos. Este trabajo introduce una forma de observar un único receptor diana de fármaco en solución durante mucho más tiempo que antes, revelando cómo permanece en conformaciones concretas que son cruciales para la acción de los fármacos.
Por qué importan estas proteínas que cambian de forma
El estudio se centra en una clase importante de proteínas de la superficie celular conocidas como receptores acoplados a proteína G, o GPCR. Estas proteínas controlan procesos vitales como la visión, el estado de ánimo, la presión arterial y las respuestas inmunitarias; más de un tercio de los fármacos aprobados actúan sobre ellas. Un miembro bien estudiado, el receptor de adenosina A2A, ayuda a regular el sueño, el dolor, la inflamación y la señalización cerebral, y es una diana prometedora para tratar enfermedades como el Parkinson y el cáncer. Los GPCR son muy flexibles: cuando se unen distintas moléculas, empujan al receptor hacia conformaciones que favorecen unas vías de señalización frente a otras. Esa misma flexibilidad, sin embargo, dificulta diseñar fármacos basándose en instantáneas estáticas de rayos X o criomicroscopía electrónica.
Seguir un solo receptor sin inmovilizarlo
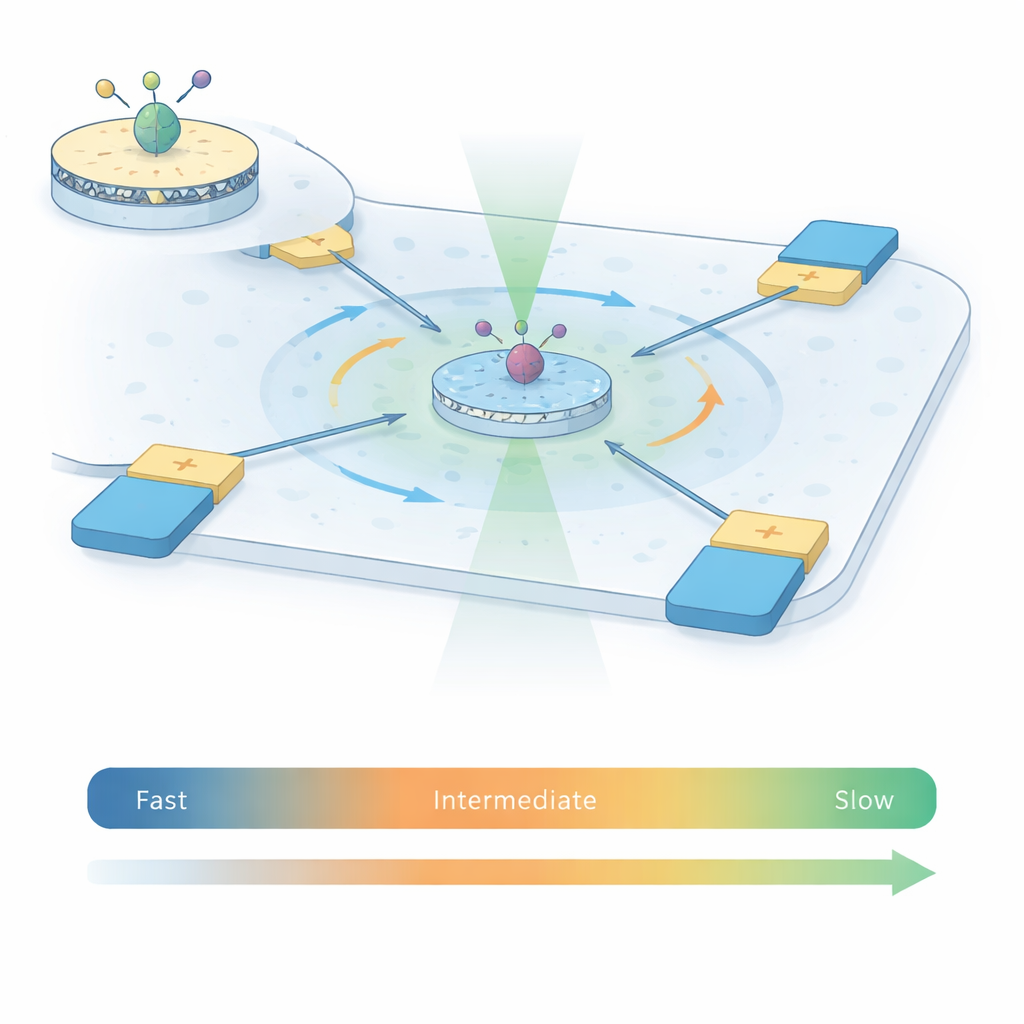
Para capturar cómo se mueven los receptores A2A, los autores combinan dos técnicas potentes en lo que llaman ABEL‑FRET. Primero, reconstituyen receptores individuales en pequeños parches de membrana artificial denominados nanodiscos, proporcionando a cada proteína un entorno más natural que el detergente solo. Colocan un par de tintes fluorescentes en dos partes móviles del interior del receptor. A medida que el receptor cambia de forma, la distancia y la orientación relativa entre estos tintes cambian, modificando la transferencia de energía entre ellos —un fenómeno conocido como transferencia de energía por resonancia de Förster (FRET). Segundo, en lugar de pegar el receptor a una superficie, usan una trampa electrocinética anti‑Browniana (ABEL): una cámara microfluídica con electrodos que detectan dónde está una partícula fluorescente y la devuelven suavemente al centro, contrarrestando el movimiento browniano aleatorio.
Salvando la ventana temporal que faltaba
Los experimentos tradicionales de FRET de una sola molécula observan receptores que se difunden libremente durante solo unos pocos milisegundos, o receptores inmovilizados en una superficie durante segundos o minutos. Cada enfoque cubre una ventana temporal distinta. Usando la trampa ABEL, este trabajo mantiene receptores A2A individuales en vista durante uno o dos segundos mientras permanecen libres en solución, aproximadamente 100 veces más tiempo que en experimentos limitados por difusión. Este tiempo de observación ampliado permite al equipo medir cómo fluctúa la señal FRET dentro de cada ráfaga atrapada y a lo largo de miles de receptores, en cuatro condiciones: sin ligando, con un antagonista y con dos moléculas activadoras (agonistas) distintas. Herramientas estadísticas tomadas del análisis de señales —varianza, correlación y análisis de recurrencia— les permiten distinguir el ruido fotónico aleatorio de cambios estructurales genuinos y lentos en el receptor.
Conformaciones ocultas y de larga duración reveladas
Las lecturas de FRET muestran que los receptores ocupan múltiples conformaciones distintas que no se interconvierten completamente durante los tiempos de observación típicos de unos pocos cientos de milisegundos. En todas las condiciones, la dispersión de valores de FRET es mucho mayor de la esperada por el ruido solo, revelando heterogeneidad estructural: moléculas diferentes residen en conformaciones de larga duración distintas. Cuando se unen moléculas activadoras, el nivel medio de FRET se desplaza hacia arriba, indicando que el receptor pasa más tiempo en una disposición «similar a la activa» de sus hélices internas. Aun así, los análisis de correlación muestran que una vez que un receptor está en un estado de FRET alto o intermedio, hay una fuerte probabilidad de que permanezca allí al menos cientos de milisegundos. Estos resultados actualizan estimaciones anteriores basadas en experimentos más rápidos, extendiendo los tiempos característicos de permanencia en estados de larga duración desde meros milisegundos hasta más de una décima de segundo.
Un nuevo mapa del paisaje energético del receptor
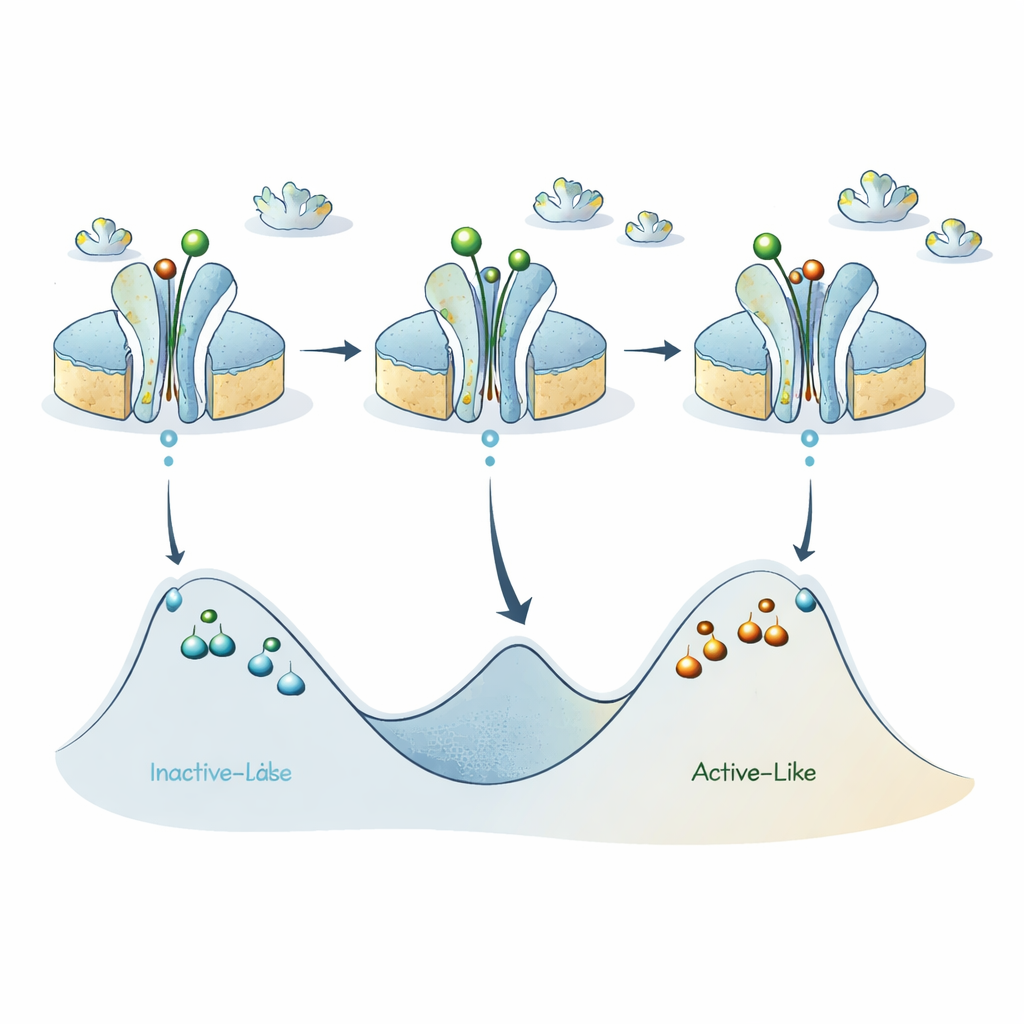
Al juntar estas piezas, los autores refinan un modelo anterior en el que el receptor A2A alterna principalmente entre un estado parecido al inactivo y otro parecido al activo. Sus nuevos datos sugieren que cada una de estas dos categorías amplias oculta en realidad varios subestados separados por barreras energéticas considerables, de modo que receptores individuales pueden permanecer «atascados» en una versión dada de similar al activo o similar al inactivo durante tiempos sorprendentemente largos. Los ligandos activadores reducen la barrera entre las principales cuencas similar al inactivo y similar al activo, favoreciendo conmutaciones rápidas a escala submilisegundo, pero las barreras internas dentro de cada cuenca permanecen altas, dando lugar a los subestados de larga duración que detecta ABEL‑FRET.
Qué significa esto para futuros medicamentos
Para no especialistas, el mensaje clave es que una diana farmacológica como el receptor A2A no se limita a alternar entre «apagado» y «encendido». En vez de eso, explora un paisaje accidentado de conformaciones, algunas de las cuales persisten el tiempo suficiente como para influir en cómo se transmiten las señales dentro de las células y en cómo actúan los fármacos a lo largo del tiempo. Al ampliar el tiempo durante el cual se puede observar cada receptor en su estado natural y sin ataduras, ABEL‑FRET llena una brecha crucial entre mediciones ultrarrápidas y muy lentas. Este enfoque puede aplicarse ahora a muchas proteínas de membrana, ofreciendo una imagen temporalmente más completa de cómo respiran, se desplazan y responden a compuestos terapéuticos las posibles dianas farmacológicas.
Cita: Maslov, I., Borshchevskiy, V., Pérez, I. et al. ABEL-FRET bridges the timescale gap in single-molecule measurements of the structural dynamics in the A2A adenosine receptor. Commun Chem 9, 114 (2026). https://doi.org/10.1038/s42004-026-01941-8
Palabras clave: receptores acoplados a proteína G, FRET de una sola molécula, receptor de adenosina A2A, dynamics conformacionales de proteínas, trampa ABEL