Clear Sky Science · es
Estudio mecanístico sobre la migración de sulfatos en glicosaminoglucanos durante la fragmentación en MS
Por qué importa que las etiquetas químicas se desplacen en los azúcares
Nuestras células están recubiertas por largas cadenas de azúcares que ayudan a controlar procesos tan diversos como la coagulación sanguínea, la defensa inmune y la forma en que los virus se adhieren a las células. Muchas de estas cadenas llevan pequeñas etiquetas químicas llamadas grupos sulfato cuya posición exacta a lo largo del esqueleto azucarado actúa como un código molecular, indicando a las proteínas cuándo y dónde unirse. Los científicos dependen en gran medida de la espectrometría de masas, una técnica potente de pesada, para leer estos códigos. Este estudio revela que, durante tales mediciones, las etiquetas sulfatadas pueden desplazarse silenciosamente, lo que potencialmente engaña a los investigadores sobre la verdadera estructura de estos azúcares biológicamente importantes.
Cadenas de azúcares complejas con etiquetas críticas
Los glicosaminoglucanos son cadenas largas y lineales de azúcares, a menudo unidas a proteínas en la superficie celular. Sus decoraciones sulfato no son aleatorias; cambios sutiles en la posición de un grupo sulfato en una unidad azucarada pueden alterar radicalmente cómo la cadena interactúa con factores de crecimiento, proteínas de la coagulación o patógenos. Por ello, los científicos intentan determinar no solo cuántos sulfatos hay, sino exactamente dónde están situados. La espectrometría de masas, a menudo combinada con la rotura controlada de las cadenas azucaradas, es una de las principales herramientas para ello. Sin embargo, indicios previos sugerían que grupos cargados como los sulfatos podrían moverse durante la medición, complicando los esfuerzos por descifrar el patrón real de modificaciones.
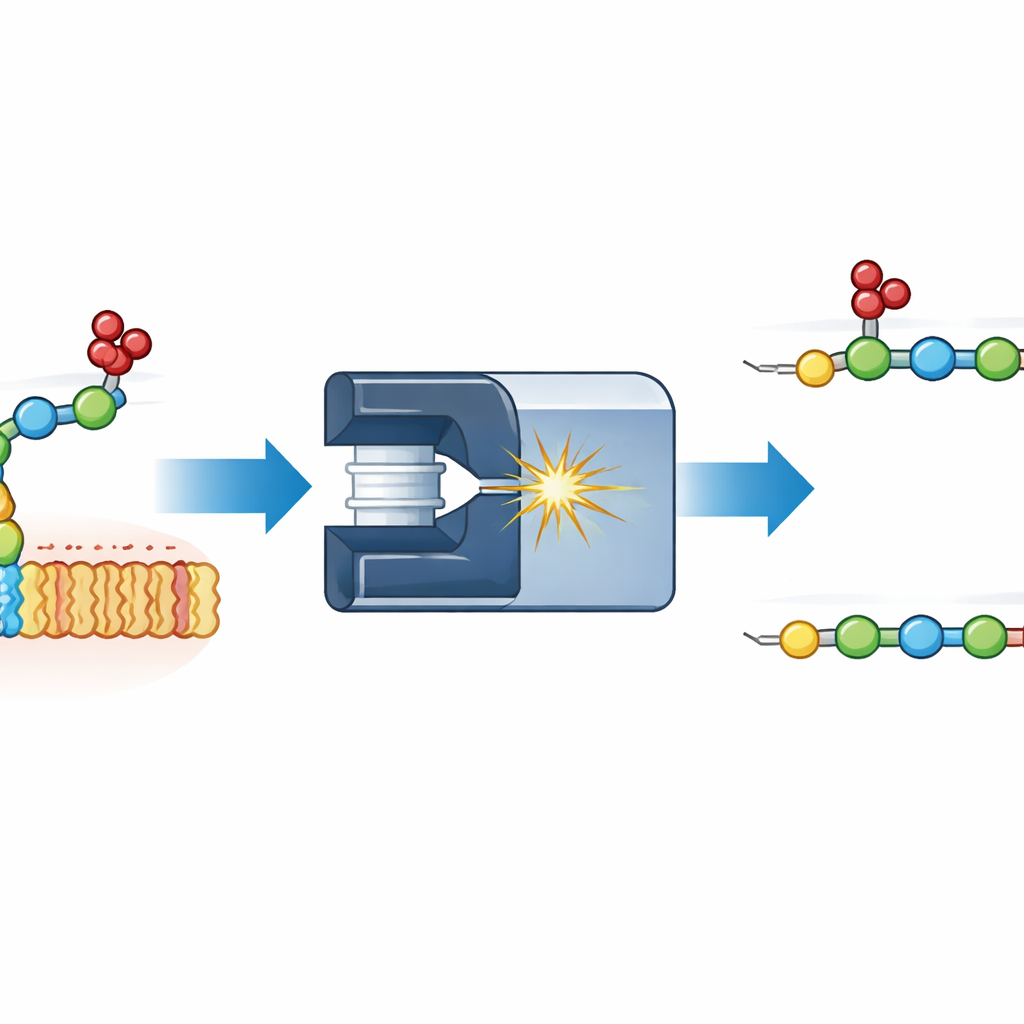
Observando el movimiento de sulfatos durante la medición
Los autores se centraron en un modelo sencillo: un fragmento disacárido de heparán sulfato, uno de los glicosaminoglucanos más conocidos. Adherieron diferentes etiquetas fluorescentes a un extremo del disacárido y lo fragmentaron dentro de un espectrómetro de masas. Midiendo cómo las piezas resultantes derivaban a través de un gas bajo un campo eléctrico —una técnica llamada movilidad iónica— pudieron distinguir conformaciones que, por masa, serían indistinguibles. Apareció un fragmento inesperado que era exactamente más pesado por un grupo sulfato en el lugar equivocado: en vez de permanecer en el primer azúcar, el sulfato se había migrado al segundo. Comparaciones con compuestos de referencia cuidadosamente sintetizados mostraron que el sulfato migrante podía aterrizar en dos puntos distintos del segundo azúcar, dando dos conformaciones diferentes que fueron claramente resueltas por movilidad iónica.
Localizando nuevos puntos de aterrizaje y probando las etiquetas
Para comprender mejor dónde terminaba el sulfato y si otras posiciones eran posibles, el equipo combinó sus mediciones con detalladas simulaciones por ordenador. Calcularon muchas formas tridimensionales posibles para las estructuras candidatas y predijeron cómo debería comportarse cada una en fase gaseosa. Solo los sulfatos ubicados en dos sitios específicos del segundo azúcar —conocidos por los especialistas como las posiciones 6O y 3O— coincidieron con el comportamiento experimental, mientras que otras ubicaciones hipotéticas parecieron poco probables. Los investigadores comprobaron entonces si las propias etiquetas acopladas podrían estar impulsando la reorganización, sustituyendo la etiqueta original por tres más simples. En todos los casos, la migración de sulfato persistió y produjo fragmentos similares, lo que indica que la elección de etiqueta tiene poco efecto sobre si ocurre la migración, aunque puede alterar sutilmente lo fácil que es distinguir los distintos productos.
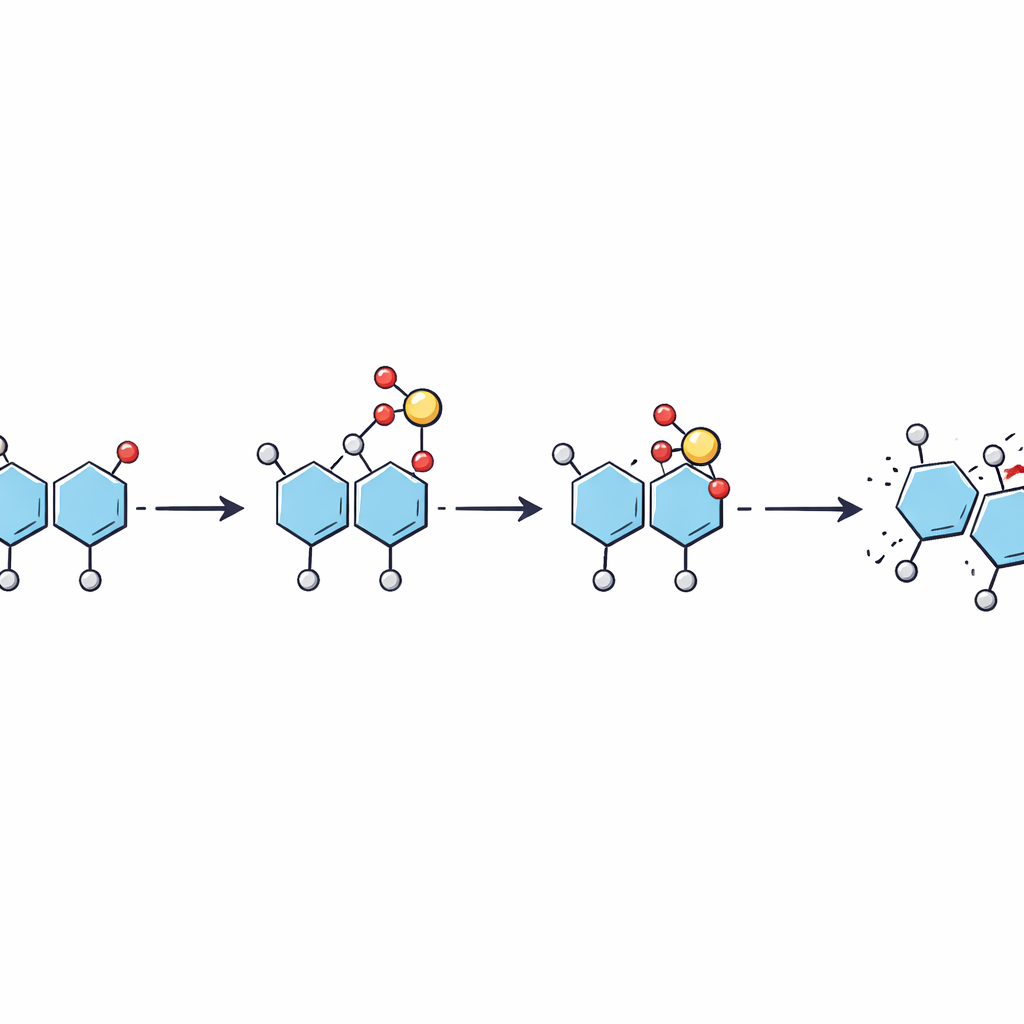
Saltos progresivos en lugar de un único brinco
Usando experimentos de fragmentación ajustados en energía junto con más simulaciones, los autores ensamblaron un cuadro paso a paso de cómo se mueve el sulfato. A medida que el ion se energiza en el espectrómetro de masas, un protón móvil activa primero al grupo sulfato, que luego salta desde el azúcar original hacia un sitio particular del azúcar vecino a medida que se rompe el enlace entre ellos. Esto produce un fragmento en el que el sulfato ocupa una posición intermedia. Con energía adicional, el sulfato puede desplazarse nuevamente a lo largo del mismo azúcar hasta un sitio más estable. El trabajo sugiere que estas reordenaciones pueden ocurrir a energías más bajas que las necesarias para romper el esqueleto azucarado, lo que significa que pueden suceder de forma silenciosa en el trasfondo de los análisis de rutina.
Qué significa esto para descifrar las estructuras azucaradas
Para quienes no son especialistas, el mensaje clave es que las etiquetas químicas en azúcares biológicos importantes no siempre están fijas durante el análisis; pueden desplazarse a lo largo de la cadena mientras la molécula atraviesa el espectrómetro de masas. El estudio muestra en detalle que, al menos para un fragmento representativo de heparán sulfato, un grupo sulfato puede migrar de una unidad azucarada a otra y luego asentarse en nuevas posiciones, produciendo fragmentos engañosos que imitan rasgos estructurales genuinos. Esto significa que algunas mediciones pasadas y futuras podrían leer mal el código de sulfato a menos que se empleen técnicas adicionales, como la movilidad iónica y modelado avanzado, para detectar estos movimientos ocultos. El trabajo reclama estudios más sistemáticos para conocer cuán extendida está esta migración de sulfatos, de modo que los investigadores puedan relacionar con mayor fiabilidad los patrones de azúcares en la superficie celular con la salud y la enfermedad.
Cita: Polewski, L., Yaman, M., Tokić, M. et al. Mechanistic study on the sulfate migration in glycosaminoglycans during MS fragmentation. Commun Chem 9, 130 (2026). https://doi.org/10.1038/s42004-026-01939-2
Palabras clave: heparán sulfato, glicosaminoglucanos, espectrometría de masas, migración de sulfatos, movilidad iónica