Clear Sky Science · es
La profundidad de la pose de unión modula la eficacia de ligandos fotoswitchables en el receptor 5-HT2A
Iluminando los fármacos cerebrales conmutables
Imagínese un medicamento que pueda encenderse y apagarse con un destello de luz, dirigiendo con precisión los receptores cerebrales mientras evita efectos secundarios. Este estudio explora exactamente esa idea para un receptor clave de serotonina vinculado con el ánimo, la percepción y las drogas psicodélicas. Los investigadores indagaron por qué dos moléculas fotosensibles casi idénticas se comportan de forma tan diferente: una actúa casi como un interruptor perfecto de encendido/apagado, la otra se niega tercamente a apagarse por completo. Su respuesta se reduce a un factor sorprendentemente simple: qué tan profundamente se asienta la molécula dentro del receptor.
Medicamentos activados por luz en el cerebro
Los fármacos activados por luz, también llamados herramientas fotofarmacológicas, están diseñados de modo que un haz de luz haga que una parte de la molécula cambie entre dos formas, como una versión doblada y otra recta. Esas formas pueden modificar cuánto se aferra el fármaco a su diana. En este trabajo, la diana es el receptor humano 5-HT2A, una proteína en las células cerebrales que responde a la serotonina y que es central tanto en efectos antipsicóticos como psicodélicos. Las moléculas estudiadas son derivados de la N,N-dimetiltriptamina (DMT), modificados con una unidad fotosensible de azobenceno. Dos versiones difieren solo en dónde se coloca un pequeño grupo metoxi en un anillo —ya sea en posición “para” o “meta”—, y sin embargo su comportamiento biológico bajo la luz es dramáticamente distinto.
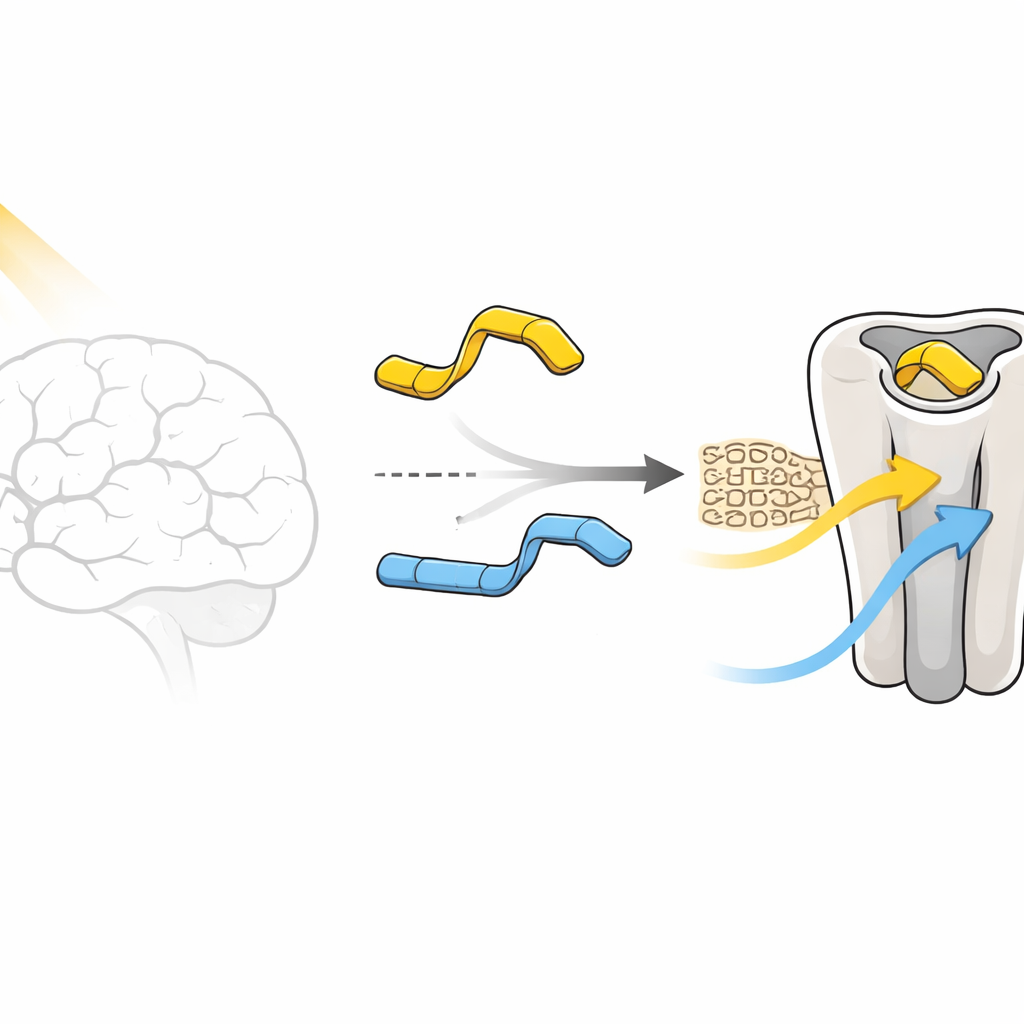
Dos moléculas casi gemelas, interruptores muy distintos
En pruebas celulares, la versión para, llamada compuesto 1, se comporta casi como un interruptor digital. En la oscuridad, su forma “trans” apenas activa el receptor e incluso lo bloquea ligeramente, actuando como un antagonista débil. Cuando la luz la transforma en la forma “cis”, la misma molécula se convierte en un activador moderado, poniendo el receptor parcialmente en marcha. La versión meta, compuesto 2, se niega a cooperar de esa manera: tanto sus formas con luz como sin luz mantienen el receptor bastante activo, nunca ofreciendo un estado verdaderamente “apagado”. El enigma central de este trabajo es por qué un ajuste químico tan mínimo —solo desplazar un pequeño grupo alrededor de un anillo— cambia tan fuertemente la respuesta del receptor.
Mirando dentro con películas a nivel atómico
Para resolverlo, el equipo utilizó extensas simulaciones de dinámica molecular todo-átomo, en la práctica rodando películas detalladas de cada átomo en el receptor, la membrana circundante, el agua y cada ligando durante un total de aproximadamente 80 microsegundos. Simularon ambas moléculas en cada una de sus formas controladas por luz, y en las formas inactiva y activa del receptor 5-HT2A. Al rastrear “microinterruptores” estructurales conocidos dentro de la proteína —como un triptófano clave que gira, un puente salino que se rompe y el movimiento de sodio y agua en el núcleo— pudieron determinar cuándo el receptor se inclinaba hacia un estado apagado o encendido. También compararon cuánto imitaban las nuevas moléculas la postura de unión del LSD, un activador parcial bien estudiado, usando la superposición de sus sistemas de anillo como guía.
La profundidad importa más que la forma por sí sola
La idea central es que la eficacia de las moléculas está gobernada principalmente por qué tan profundamente se insertan en el bolsillo de unión del receptor. En el receptor inactivo, la forma trans del compuesto para establece un conjunto especial de enlaces de hidrógeno que lo atraen inusualmente hacia adentro, por debajo de la región donde ocurren los contactos típicos de activación. Esta “sobreinserción” impide que toque residuos polares clave que ayudan a activar el receptor, por lo que estabiliza el estado apagado. La forma trans del compuesto meta no puede formar los mismos contactos de anclaje y en su lugar se sitúa más arriba en una pose más similar a la del LSD, compatible con la activación, lo que explica su actividad residual. Cuando la luz convierte ambas moléculas en sus formas cis, generalmente se desplazan a posiciones más superficiales, más parecidas a las de un activador. Aun así, la geometría importa: en el receptor activo, el cis del compuesto 2 puede deslizarse más profundamente en un túnel hidrofóbico entre dos hélices y formar un enlace de hidrógeno persistente que refuerza su fuerte comportamiento agonista, mientras que el cis del compuesto 1 está bloqueado estéricamente y no puede hacerlo.
Control fino del agua y los iones internos
Las simulaciones también muestran que la profundidad de unión ajusta sutilmente un bolsillo interno de sodio y una vía de agua que se sabe que influyen en la activación del receptor. La unión profunda y rígida del compuesto para en su forma trans mantiene un ion sodio fuertemente confinado y la región circundante relativamente seca, rasgos asociados a un estado apagado. En contraste, la unión más móvil del compuesto meta o las formas cis permite que más agua invada y afloja el entorno del sodio, predisponiendo al receptor a la activación. Un residuo aromático clave que actúa como “interruptor” puede cambiar de orientación con mayor facilidad cuando los ligandos son flexibles y no están sobranclados, empujando adicionalmente al receptor hacia un estado más encendido, especialmente con el cis del compuesto 2.
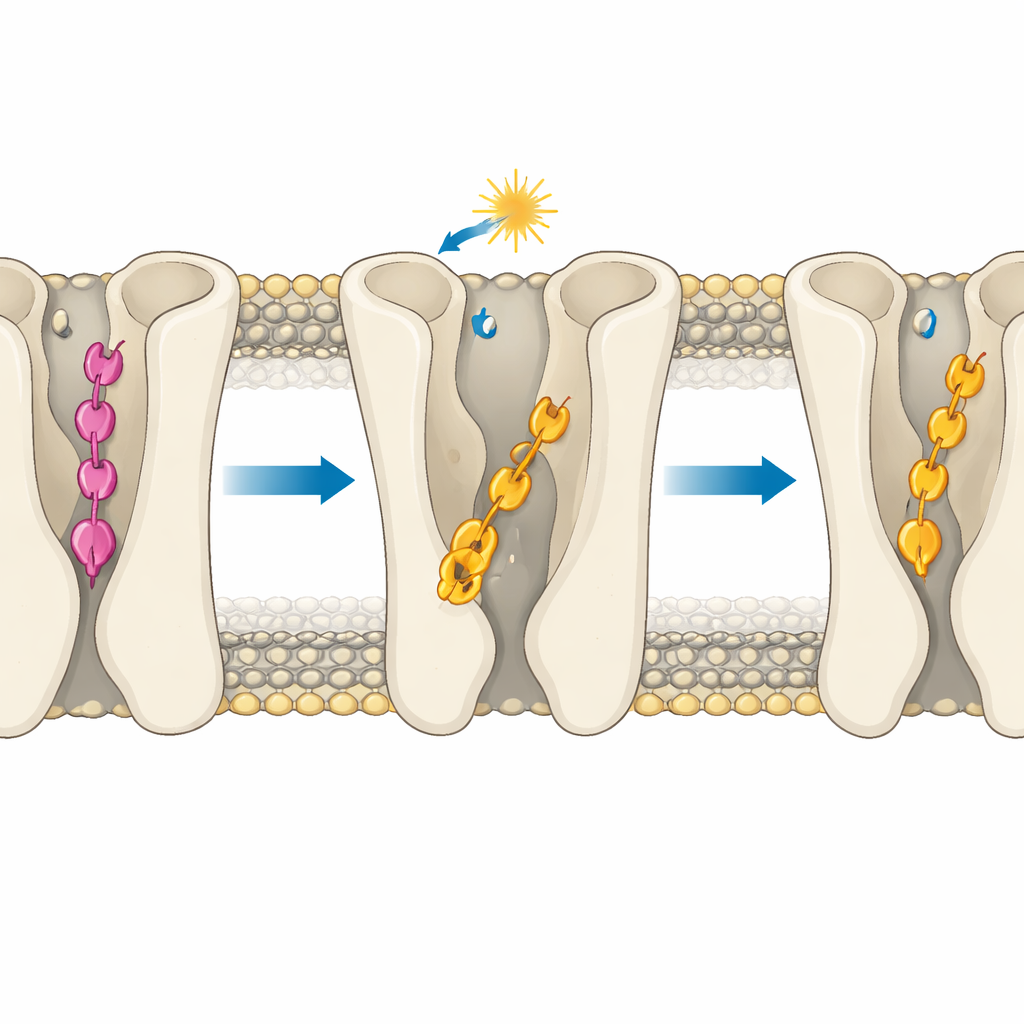
Reglas de diseño para futuros fármacos controlados por luz
Para un lector no especialista, el mensaje es que la profundidad exacta a la que un fármaco se asienta en el bolsillo de su receptor puede marcar la diferencia entre apagado, parcialmente encendido y fuertemente encendido —incluso cuando el cambio químico parece mínimo sobre el papel. Al mostrar cómo un ligando fotoswitchable puede sobreinsertarse y bloquear el receptor, mientras que otro estrechamente relacionado se mantiene a una profundidad compatible con la activación, el estudio ofrece una regla de diseño clara: controle la profundidad de inserción con la misma atención que controla los cambios de forma inducidos por la luz. Estos conocimientos podrían guiar la creación de compuestos fotosensibles de próxima generación que traten trastornos cerebrales con una precisión sin precedentes, modulando vías de señalización de forma controlada y reversible mientras se minimizan los efectos secundarios.
Cita: Weber, V., Salvadori, G., Natale, F. et al. Binding pose depth modulates photoswitchable ligands’ efficacy at the 5-HT2A receptor. Commun Chem 9, 121 (2026). https://doi.org/10.1038/s42004-026-01936-5
Palabras clave: fotofarmacología, receptor de serotonina 5-HT2A, ligandos fotoswitchables, activación de GPCR, simulaciones de dinámica molecular