Clear Sky Science · es
Comportamiento scaffold-client y organización estructural en condensados proteicos multicomponentes revelados al estudiar gotas de tau/TDP-43
Proteínas que se comportan como pequeñas gotas de aceite
Dentro de nuestras células, muchas proteínas no permanecen mezcladas de forma homogénea en el medio acuoso. En su lugar, se agrupan en pequeñas gotas líquidas, algo así como el aceite en el agua. Este estudio analiza cómo dos de esas proteínas, tau y TDP-43, estrechamente vinculadas con la enfermedad de Alzheimer y otras demencias, se agrupan juntas en gotas. Al desentrañar cómo se forman, mezclan y organizan estas gotas, el trabajo aporta pistas sobre por qué aparecen agregados proteicos dañinos en cerebros envejecidos y cómo podríamos algún día controlarlos.
Por qué importan estas dos proteínas cerebrales
Tau y TDP-43 son conocidas por formar agregados tóxicos en enfermedades neurodegenerativas. Tradicionalmente, los científicos las estudiaron por separado, pero las autopsias de cerebros humanos muestran cada vez más que ambas proteínas pueden acabar en las mismas regiones dañadas. Eso plantea una pregunta clave: cuando tau y TDP-43 coexisten en las células, ¿cómo comparten el espacio dentro de las gotas y si ese entorno compartido favorece la agregación asociada a la enfermedad? Los autores eligieron un modelo simplificado pero realista usando tau y la cola de baja complejidad de TDP-43 (LCD), que es la porción más responsable de la formación de gotas y de la eventual solidificación.
Gotas, “andamios” y “clientes”
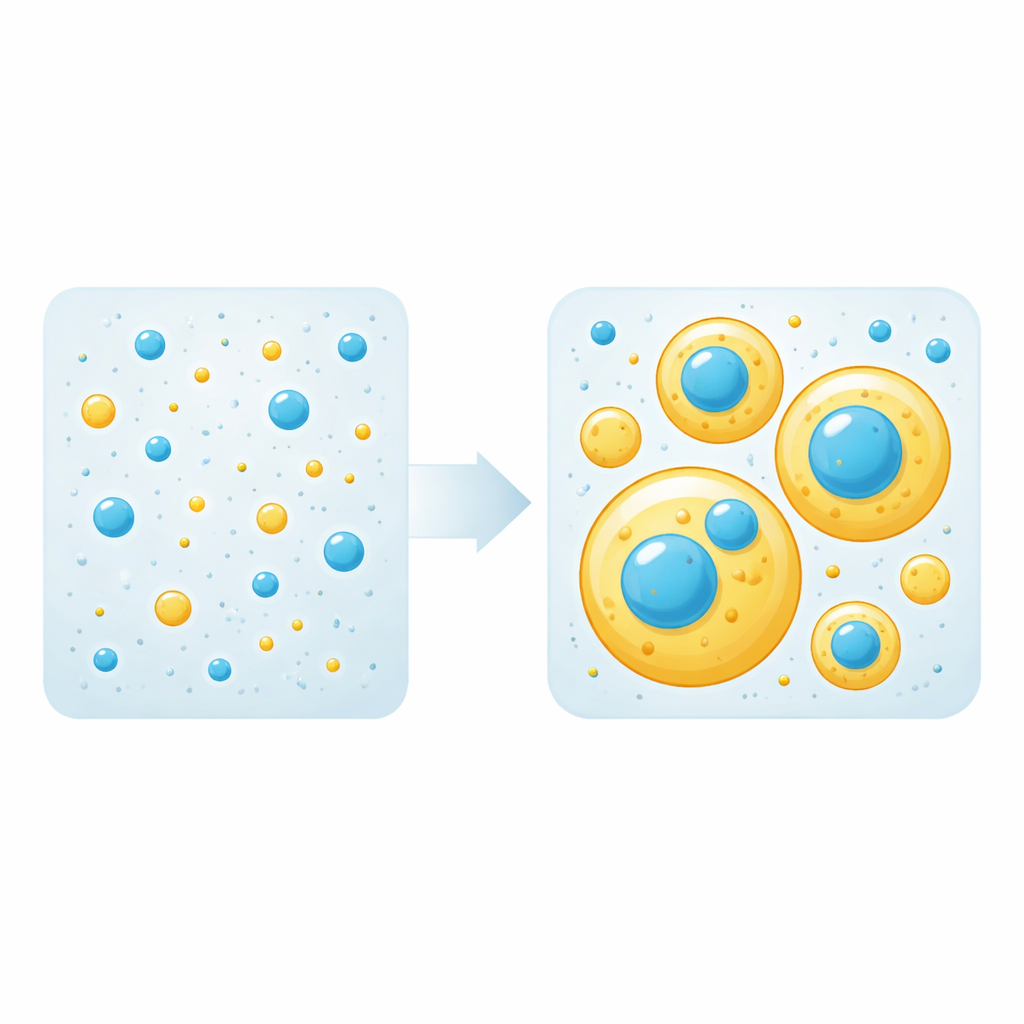
Gotas líquidas como estas se forman cuando las atracciones proteína–proteína superan a las atracciones proteína–agua, provocando que una disolución se separe en una fase densa (gotas) y una fase diluida. En mezclas, solo algunas proteínas son necesarias para construir las gotas; a estas se las llama “andamios” (scaffolds). Otras simplemente se montan dentro de las gotas como “clientes”. El equipo midió primero el umbral de concentración a partir del cual cada proteína sola comienza a formar gotas. Luego mezclaron diferentes cantidades de tau y del LCD de TDP-43 y observaron, mediante microscopía de fluorescencia, si aparecían gotas y cómo se organizaban las proteínas. De forma llamativa, hallaron que cualquiera de las dos proteínas puede actuar como andamio o cliente dependiendo exclusivamente de su concentración: por encima de su propio umbral construye gotas; por debajo de ese umbral se incorpora pasivamente a las gotas formadas por la otra.
Gotas en capas y un halo misterioso
Cuando ambas proteínas eran lo bastante abundantes como para formar gotas por sí solas, no se mezclaban en una única gota uniforme. En lugar de ello, gotas mayores ricas en tau envolvían gotas más pequeñas ricas en TDP-43, creando una estructura multifásica y en capas. Las mediciones de cómo se extienden las gotas sobre el vidrio mostraron que las gotas de TDP-43 tienen mayor tensión superficial, por lo que es energéticamente favorable que se sitúen dentro de las gotas de tau, que mojan más. En estas interfaces surgió una característica llamativa: tau se acumulaba a niveles especialmente altos como un brillante “halo” que recubría la superficie de las gotas ricas en TDP-43, incluso cuando tau por sí sola estaba por debajo de su umbral de formación de gotas. Con el tiempo, las regiones ricas en TDP-43 tendían a endurecerse en un material más parecido a un sólido, mientras que las regiones ricas en tau permanecían líquidas, lo que sugiere diferentes propensiones a convertirse en agregados duraderos.
Ajustar interacciones y sondear el mecanismo microscópico
Los autores probaron después cómo las fuerzas moleculares específicas controlan qué proteína actúa como andamio o cliente. Debilitaron selectivamente las interacciones hidrofóbicas (repelentes al agua) que impulsan la condensación del LCD de TDP-43 con 1,6-hexanodiol, y por separado atenuaron las interacciones electrostáticas (basadas en carga) que impulsan la condensación de tau aumentando la salinidad. En cada caso, desactivar las interacciones clave de una proteína le impidió formar gotas y la convirtió en cliente dentro de las gotas de la otra, emulando lo que ocurre al bajar su concentración. Para entender mejor el halo, variaron la sal y midieron cuánto tau penetraba en las gotas de TDP-43 y usaron simulaciones por ordenador que tratan cada aminoácido como una perla simplificada. Estas simulaciones reprodujeron el halo y mostraron que los primeros ~40 aminoácidos de la región N-terminal cargada negativamente de tau se anclan en la superficie de la gota, mientras que el resto de la molécula se extiende hacia el líquido circundante, creando una cubierta “anfifílica” (parte afín a la gota, parte afín al agua). Experimentos con un fragmento acortado de tau sin este tramo N-terminal confirmaron que, sin él, el halo desaparece.

Qué significa esto para las enfermedades cerebrales
En conjunto, los resultados revelan un conjunto general de reglas sobre cómo se ensamblan y organizan gotas proteicas multicomponentes. En este sistema tau/TDP-43, que refleja situaciones en neuronas enfermas, la concentración y la fuerza de las interacciones determinan conjuntamente qué proteínas construyen las gotas y cuáles simplemente las ocupan. La tensión superficial y las disposiciones anfifílicas esculpen luego gotas en capas y halos que pueden concentrar múltiples proteínas vinculadas a la enfermedad en el mismo espacio confinado, potenciando su endurecimiento en agregados. Para un lector general, el mensaje clave es que tau y TDP-43 no se agregan al azar; se autoorganizan en gotas líquidas estructuradas cuya arquitectura está gobernada por principios físicos sencillos. Comprender y, eventualmente, manipular estos principios podría abrir nuevas vías para frenar o prevenir la acumulación proteica dañina en las enfermedades neurodegenerativas.
Cita: Monnaka, V.U., Shipley, B., Boyko, S. et al. Scaffold-client behavior and structural organization in multicomponent protein condensates as revealed by studying tau/TDP-43 droplets. Commun Chem 9, 126 (2026). https://doi.org/10.1038/s42004-026-01933-8
Palabras clave: condensados proteicos, separación de fases líquido-líquido, tau, TDP-43, neurodegeneración