Clear Sky Science · es
Explorando la estabilidad de BOx sobre diferentes soportes inorgánicos
Combustibles más limpios a partir de un elemento común
Transformar el propano común —el que se guarda en los tanques de las barbacoas— en bloques de construcción más valiosos para plásticos suele requerir procesos calientes y consumidores de energía que además generan mucho dióxido de carbono. Este estudio explora cómo compuestos de boro, un elemento relativamente abundante, pueden ayudar a realizar esta transformación de forma más suave y limpia. Al desvelar cómo se comporta el boro sobre distintas superficies sólidas a altas temperaturas, los autores apuntan nuevas formas de diseñar catalizadores que produzcan químicos útiles con menos residuos y menor consumo energético.
Por qué importa la química de convertir propano en plásticos
La vida moderna depende en gran medida de olefinas ligeras como el propeno y el eteno, que son ingredientes clave para plásticos, fibras y multitud de materiales cotidianos. Hoy, la mayor parte de estos compuestos se obtienen del petróleo o del gas natural mediante rutas intensivas en energía que liberan grandes cantidades de CO₂. Un proceso alternativo, llamado deshidrogenación oxidativa del propano, puede en principio producir estas olefinas a temperaturas más bajas y con menos subproductos indeseados. Los materiales a base de boro han emergido recientemente como catalizadores prometedores para esta reacción porque son muy selectivos: favorecen transformar propano en olefinas en lugar de quemarlo hasta CO₂. Sin embargo, los investigadores todavía no comprenden del todo cómo son las especies de boro “activas” ni dónde ocurre exactamente la reacción: si en la superficie del catalizador, en fase gaseosa, o en ambos lugares.
Movilidad sorprendente del boro en reactores calientes
Los autores se centraron en el óxido de boro, un compuesto simple boro–oxígeno a menudo indicado como BOx, soportado sobre tres materiales inorgánicos comunes: sílice pura, alúmina pura y una sílice–alúmina mixta. Empleando una combinación de técnicas que rastrean los gases que salen de la superficie al calentarse, junto con métodos que sondean la estructura local de los átomos en los sólidos, demostraron que el boro no siempre permanece en su sitio. Sobre sílice, el óxido de boro tiende a formar racimos débilmente enlazados que pueden evaporarse, generando especies volátiles que contienen boro en la corriente de gas. En soportes ricos en alúmina, en cambio, el boro se enlaza con más firmeza a átomos de oxígeno conectados al aluminio, formando una red más estable, similar a un vidrio, que resiste el arrastre hacia la fase gaseosa. Pruebas simples de lavado reforzaron este panorama: la mayor parte del boro podía enjuagarse desde las muestras soportadas en sílice, pero mucho menos desde las basadas en alúmina.
Vinculando la estabilidad del boro con el comportamiento catalítico
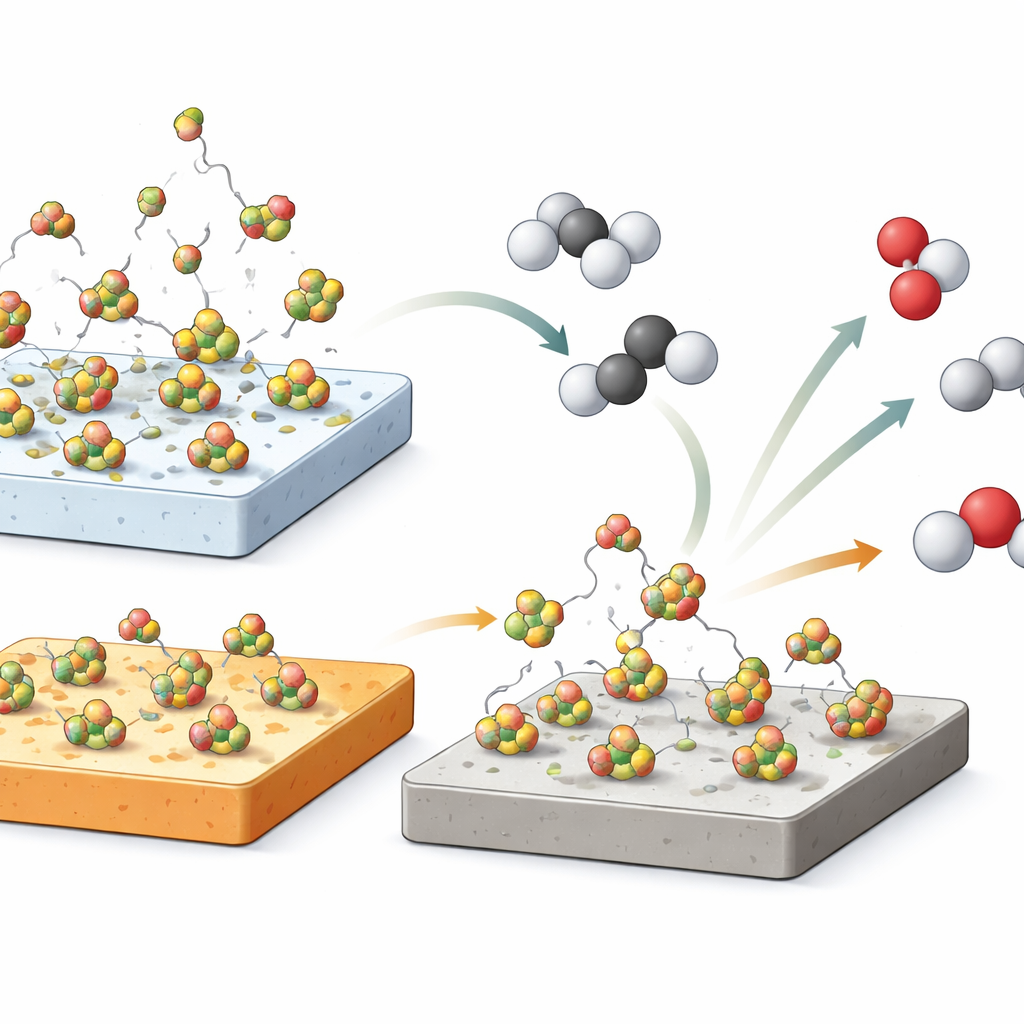
Estas diferencias en la movilidad del boro resultaron correlacionarse estrechamente con el comportamiento de los catalizadores en la reacción del propano. El óxido de boro soportado en sílice empezó a convertir propano en olefinas a temperaturas alrededor de 80 °C más bajas que los catalizadores que contenían alúmina, aunque los tres sistemas mostraron finalmente relaciones muy similares entre cuánto propano convertían y con qué selectividad producían olefinas. Calentar las muestras mientras se monitorizaban fragmentos que contienen boro en la fase gaseosa reveló que la sílice liberaba mucha más cantidad de óxido de boro y especies relacionadas a temperaturas de reacción que la alúmina. Esto sugiere que los soportes que permiten que el boro escape con mayor facilidad pueden desencadenar la reacción antes, porque más intermediarios reactivos que contienen boro entran en la fase gaseosa donde pueden iniciar reacciones en cadena que transforman el propano.
El boro en fase gaseosa como un ayudante invisible
Para comprobar si el boro en la fase gaseosa por sí solo podía impulsar la química, los investigadores llevaron a cabo un experimento llamativo: retiraron por completo el catalizador sólido e inyectaron simplemente un pequeño pulso de solución de ácido bórico, equivalente a aproximadamente una septuagésima parte del boro normalmente presente en un catalizador, directamente en un reactor caliente y vacío. Al descomponerse rápidamente la solución a óxido de boro a 500 °C, la conversión de propano aumentó en torno a un 20 %, con una selectividad a olefinas similar a la observada sobre los catalizadores sólidos. Una prueba de control con agua pura produjo sólo un efecto pequeño y de corta duración. Junto con las mediciones de desorción, este resultado indica firmemente que las especies volátiles de boro en la fase gaseosa desempeñan un papel importante, probablemente iniciando cadenas radicalarias que convierten propano en propeno y eteno.
Qué significa esto para futuros catalizadores
Para los no especialistas, la conclusión principal es que el soporte sólido bajo un catalizador a base de boro no es sólo un armazón inerte: controla activamente cuánto boro puede escapar a la fase gaseosa y, con ello, qué tan fácilmente comienza la reacción. Soportes como la sílice, que liberan boro con más facilidad, permiten la activación del propano a temperaturas más bajas, mientras que los soportes ricos en alúmina retienen el boro con mayor firmeza y requieren temperaturas más altas, aunque todos acaban mostrando selectividades de producto similares una vez que la reacción está en marcha. Esta intuición sugiere que ajustar cuidadosamente la fuerza con que el boro está anclado a su soporte podría permitir a los químicos diseñar catalizadores que equilibren estabilidad y actividad, posibilitando rutas más limpias y energéticamente eficientes desde combustibles simples como el propano hasta las moléculas que sustentan los materiales modernos.
Cita: Johánek, V., Wróbel, M., Knotková, K. et al. Exploring the stability of BOx at various inorganic supports. Commun Chem 9, 116 (2026). https://doi.org/10.1038/s42004-026-01926-7
Palabras clave: catalizadores de óxido de boro, deshidrogenación oxidativa del propano, química radicalaria en fase gaseosa, soportes de sílice y alúmina, producción de olefinas