Clear Sky Science · es
Cristalización desencadenada por difusión de masa a una sobresaturación local menor
Por qué esto importa más allá del laboratorio
Los cristales de sal pueden parecer comunes, pero la manera en que se forman tiene enormes consecuencias: desde la fabricación de medicamentos hasta la recuperación de recursos de efluentes salinos. Este estudio revela que los cristales pueden comenzar a formarse antes, y en lugares distintos, cuando el líquido se desequilibra suavemente por gradientes de temperatura y concentración. Comprender este comportamiento sutil podría ayudar a diseñar formas más limpias y económicas de gestionar salmueras, fabricar materiales mejores y controlar la incrustación indeseada en tuberías y equipos.

Cómo suelen nacer los cristales
La cristalización ocurre cuando una sustancia disuelta, como cloruro de potasio (KCl) en agua, supera la cantidad que puede permanecer disuelta cómodamente. Este estado se denomina sobresaturación. Las teorías clásicas sostienen que los cristales aparecen solo cuando la sobresaturación es lo bastante alta para superar una barrera energética, y que la nucleación debería comenzar donde la solución está más sobresaturada. En la industria, normalmente se llevan las disoluciones a ese estado enfriándolas, evaporando el disolvente o añadiendo un “antisolvente”. Bajo estas condiciones convencionales y casi uniformes, los investigadores han trazado una zona metaestable: una ventana donde el líquido está sobresaturado pero aún no han aparecido cristales visibles.
Tres formas distintas de hacer cristalizar la misma sal
Los autores examinaron cómo aparecen los cristales de KCl en tres escenarios cuidadosamente controlados dentro de una célula plana construida a medida con control de temperatura independiente en la parte superior e inferior. Primero realizaron experimentos de enfriamiento estándar, disminuyendo la temperatura de manera uniforme desde 20 °C y observando cuándo aparecían los primeros cristales. Esto estableció un límite de referencia en el mapa concentración–temperatura: por debajo de cierta temperatura, los cristales siempre se formaban; por encima, la disolución permanecía sin cristales durante horas. Luego compararon este punto de referencia con dos situaciones más complejas en las que la solución experimentó transporte direccional de masa en lugar de un enfriamiento simple y uniforme.
Cuando el calor impulsa el movimiento de la sal
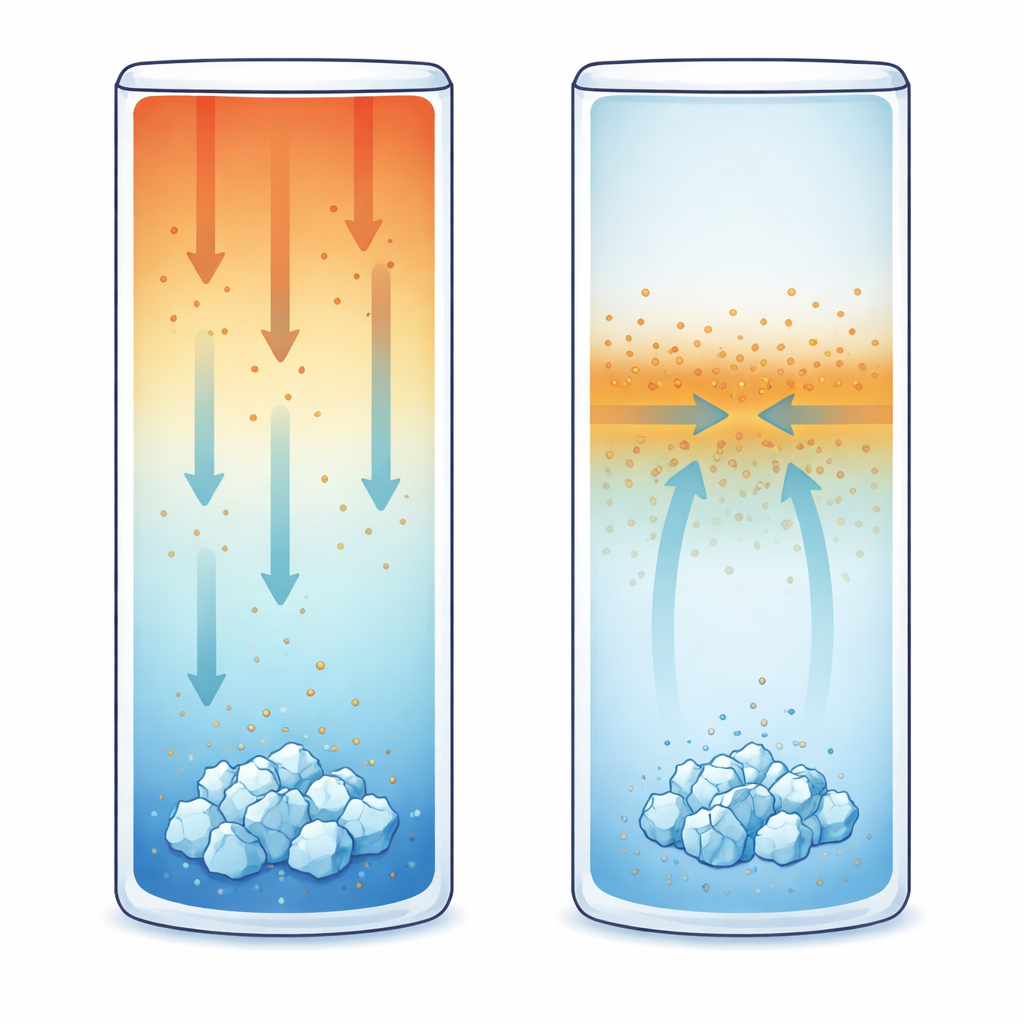
En el segundo conjunto de experimentos, la solución partía de la misma composición pero se mantuvo con la parte superior a 20 °C y la inferior enfriada a 15 °C. Este gradiente vertical de temperatura provoca termodifusión, lo que significa que los iones disueltos se desplazan en respuesta a la temperatura, no solo a la concentración. Para KCl en el rango probado, el comportamiento es termofóbico: los iones tienden a moverse hacia la región más fría, acumulando más sal cerca de la parte inferior. Utilizando un método óptico sensible llamado interferometría de cambio de fase, los investigadores siguieron pequeños cambios en el índice de refracción que revelan cómo evolucionan la concentración y la temperatura. Encontraron que los cristales se formaban de manera consistente en la pared fría inferior, en regiones donde el gradiente de concentración era más pronunciado; sin embargo, la sobresaturación local allí era ligeramente menor que en el caso de enfriamiento uniforme. En otras palabras, la presencia de un flujo de masa sostenido permitió que la cristalización comenzara antes de lo esperado.
Cuando la sal difunde en una temperatura perfectamente uniforme
El tercer escenario eliminó por completo las diferencias de temperatura. Toda la célula se mantuvo a 17 °C uniformes, inicialmente llenada con la disolución de referencia. Luego se inyectó suavemente desde una esquina superior un volumen menor de disolución de KCl más diluida, creando un contraste de concentración agudo pero casi sin agitación del fluido. La difusión suavizó ese contraste a medida que los iones migraban desde la región más concentrada hacia la más diluida. De nuevo, la interferometría reveló cómo evolucionó el campo de concentración con el tiempo. Sorprendentemente, los primeros cristales visibles no aparecieron donde la solución estaba más sobresaturada. En su lugar, se formaron aproximadamente a mitad de altura de la célula, cerca de la interfaz donde el gradiente de concentración —y por tanto el flujo difusivo de masa— era más fuerte.
Qué implica esto para la teoría y la tecnología
En los tres métodos —enfriamiento, termodifusión y difusión isotérmica—, los primeros cristales que aparecieron eran muy similares: principalmente cristales cúbicos de KCl con formas de crecimiento familiares. Lo que cambió no fue la estructura cristalina sino las condiciones que desencadenaron su aparición. Bajo flujos de masa impuestos, los cristales surgieron a una sobresaturación local menor y en ubicaciones gobernadas por gradientes en lugar de por picos de concentración. Esto sugiere que el tráfico molecular direccional en el líquido puede ayudar a que los iones se alineen en parches densos que actúan como núcleos tempranos, estrechando efectivamente la zona metaestable. Aunque la teoría clásica de la nucleación no puede explicar completamente este comportamiento, las ideas más recientes de nucleación en múltiples pasos son coherentes con los hallazgos. En la práctica, el trabajo apunta hacia un control más inteligente de la cristalización en procesos como la desalinización de descarga cero de líquidos, donde aprovechar la termodifusión podría ayudar a convertir salmueras residuales en sales sólidas usando menos energía y menos productos químicos.
Cita: Xu, S., Torres, J.F. Crystallisation triggered by mass diffusion at a lower local supersaturation. Commun Chem 9, 125 (2026). https://doi.org/10.1038/s42004-026-01925-8
Palabras clave: cristalización, termodifusión, sobresaturación, desalinización, transporte de masa