Clear Sky Science · es
Efectos sinérgicos catión‑faceta aceleran la cinética de evolución de hidrógeno en medios alcalinos sobre superficies escalonadas de Pt
Por qué esto importa para la energía limpia
Producir hidrógeno limpio a partir del agua es una pieza clave en muchos planes de energía neta‑cero, pero los dispositivos más prácticos de hoy desperdician energía porque la reacción que genera las burbujas de hidrógeno puede ser sorprendentemente lenta en soluciones alcalinas (básicas). Este estudio profundiza hasta el nivel de átomos y moléculas de agua para explicar por qué algunas superficies de platino funcionan mejor que otras y cómo iones comunes disueltos en el líquido pueden colaborar con la superficie metálica para acelerar la producción de hidrógeno.
Moldear las superficies metálicas para orientar el agua
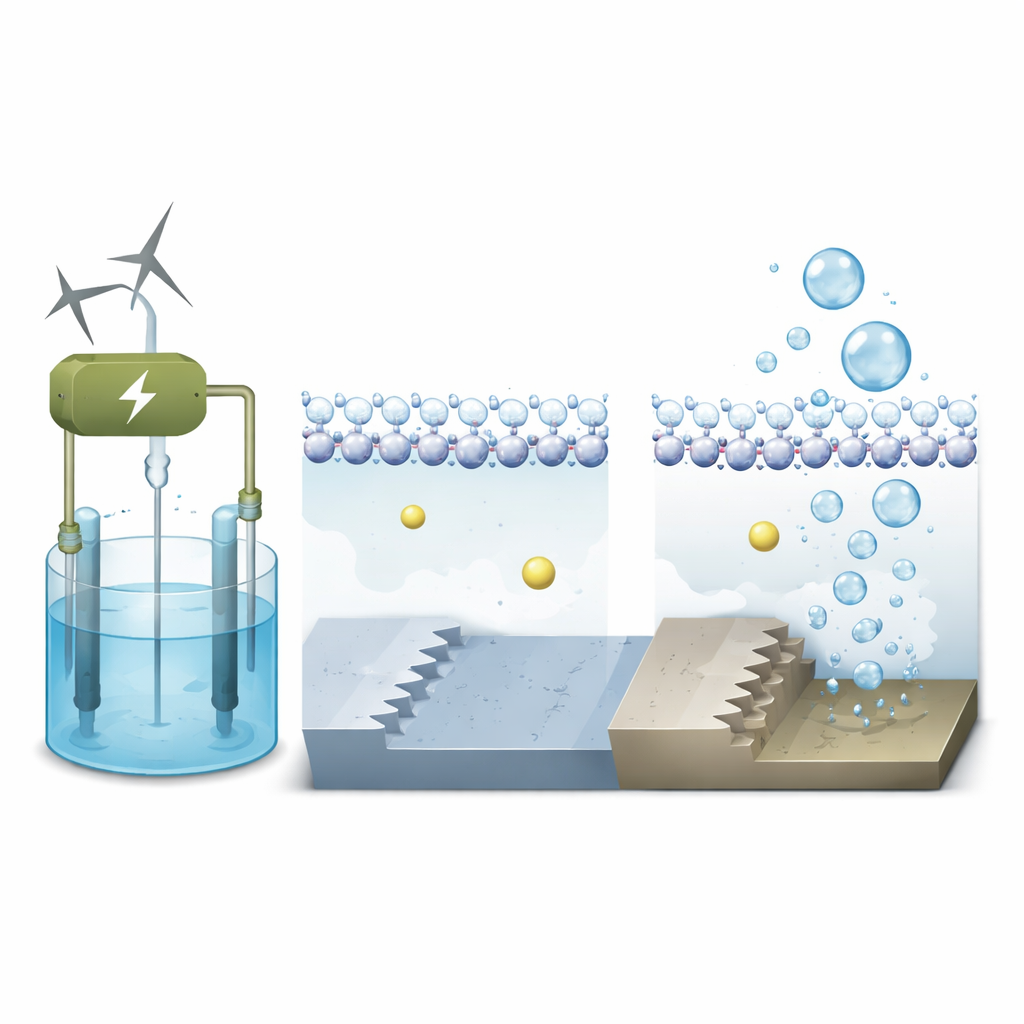
Los investigadores se centran en el platino, el material de referencia para dividir el agua, y comparan dos tipos de paisajes atómicos en su superficie. Uno es plano, como una terraza lisa (denotado Pt(111)); el otro es escalonado, similar a una pequeña escalera (Pt(311)). Usando simulaciones cuántico‑mecánicas avanzadas que incluyen tanto electrones como moléculas de agua en movimiento, modelan cómo se comportan estas diferentes superficies bajo voltajes de operación realistas en un electrolizador alcalino. El objetivo es ver cómo el entorno local justo junto al metal —donde se encuentran agua, iones y electrones— controla la velocidad del primer paso en la formación de hidrógeno.
Iones de sal como ayudantes ocultos
En los electrolizadores alcalinos, el líquido contiene iones de metales alcalinos como el sodio. Estos iones cargados positivamente hacen algo más que flotar; pueden agruparse cerca del electrodo y remodelar sutilmente el campo eléctrico en la interfaz. Las simulaciones muestran que en la terraza plana de platino, el agua forma una capa densa y ordenada con los átomos de hidrógeno apuntando hacia abajo, hacia la superficie cargada negativamente. Los iones sodio permanecen más alejados, separados del metal por esta lámina de agua, por lo que su influencia en la reacción es modesta. En la superficie escalonada, sin embargo, los átomos con menor coordinación en el borde del escalón enlazan el agua con más fuerza y crean una estructura local del agua más rugosa y desordenada.
Un clúster especial cerca de la superficie que atrae iones
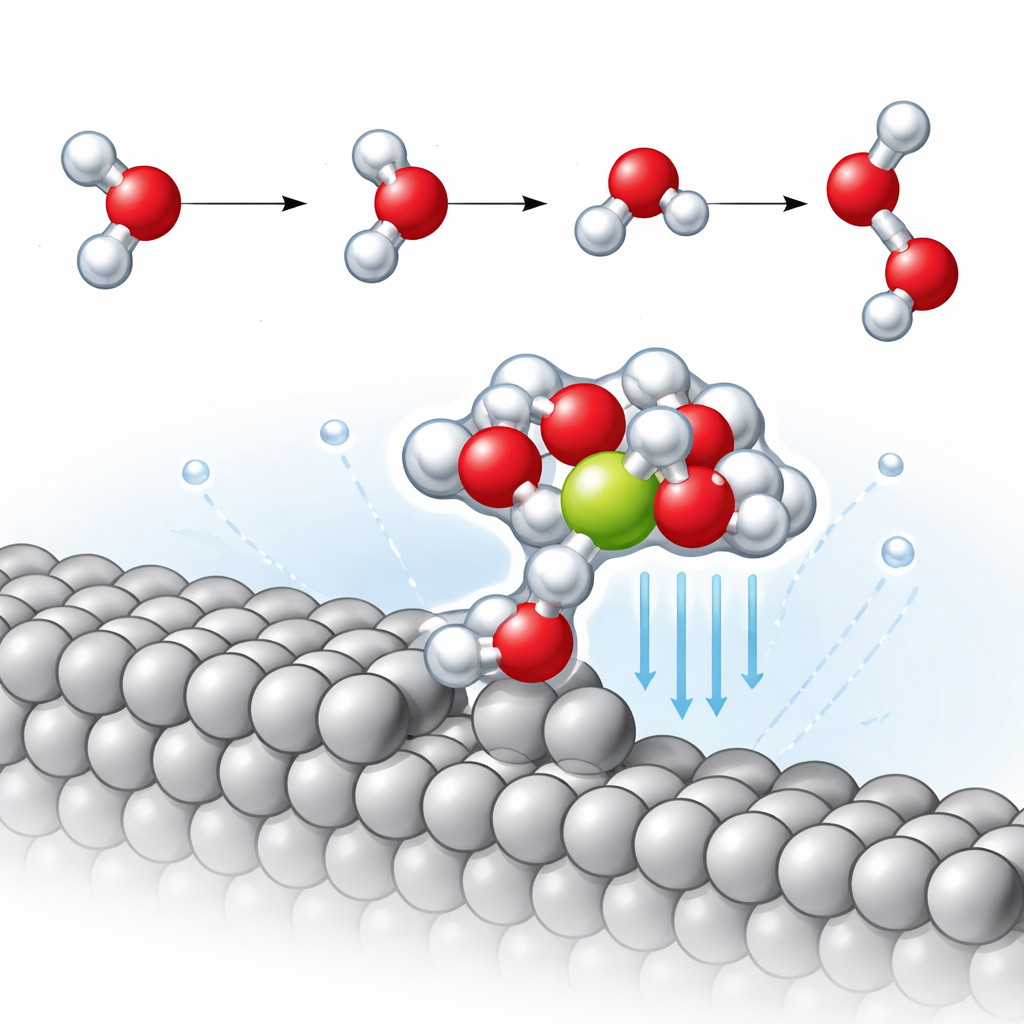
En estos bordes de escalón, el equipo descubre un motivo estructural recurrente: una molécula de agua unida directamente al escalón de platino que, a su vez, retiene un ión sodio cercano rodeado por moléculas de agua adicionales. Este compacto clúster platino–agua–sodio efectivamente arrastra el ión unos 2,3 angstroms más cerca del metal que en la superficie plana. Estar más próximo refuerza considerablemente el campo eléctrico local en esta minúscula región, lo que polariza fuertemente las moléculas de agua vecinas. Las simulaciones revelan que uno de los enlaces O–H en estas moléculas de agua se estira más de lo habitual, indicando que está parcialmente hacia la ruptura incluso antes de que la reacción proceda formalmente.
Reduciendo la barrera para formar hidrógeno
El paso clave y lento en la evolución de hidrógeno en medio alcalino se conoce como el paso de Volmer, en el que una molécula de agua se divide: el hidrógeno se une al metal mientras el hidróxido restante se desplaza hacia el líquido. Siguiendo la trayectoria de reacción de energía mínima, los autores encuentran que en la superficie plana de platino el sodio tiene solo un efecto pequeño sobre la barrera de energía para este paso. En contraste, en la superficie escalonada, el clúster estabilizado por sodio cercano reduce la energía de activación en aproximadamente 0,14 electronvoltios—aproximadamente tres veces la mejora observada en la faceta plana. Un análisis detallado de los movimientos vibracionales muestra que el enlace O–H orientado hacia la superficie se debilita de forma significativa en presencia del ión cercano, lo que facilita su ruptura y, por tanto, acelera la formación de hidrógeno.
Una regla de diseño para mejores catalizadores de hidrógeno
En conjunto, el estudio concluye que el mejor rendimiento en la producción de hidrógeno alcalino no surge solo de la superficie metálica ni del electrolito por separado, sino de su sinergia. Sitios escalonados de platino capaces de anclar clústeres especiales agua–ión atraen cationes alcalinos, intensifican el campo eléctrico local, pre‑debilitan parcialmente enlaces en el agua y aceleran con fuerza el primer paso crucial de la evolución de hidrógeno. Para un lector no especializado, la conclusión es que, al esculpir cuidadosamente la forma microscópica de las superficies catalíticas y elegir electrolitos que lleven los iones adecuados a los lugares adecuados, los ingenieros pueden superar algunas de las ralentizaciones fundamentales de los dispositivos alcalinos y diseñar sistemas más eficientes y que ahorren energía para la producción de hidrógeno limpio.
Cita: Zhang, Q., Sun, P., Li, H. et al. Synergistic cation-facet effects boost alkaline hydrogen evolution kinetics on stepped Pt surfaces. Commun Chem 9, 113 (2026). https://doi.org/10.1038/s42004-026-01924-9
Palabras clave: evolución de hidrógeno, electrólisis alcalina, catálisis de platino, agua interfacial, cationes de metales alcalinos