Clear Sky Science · es
Base estructural de la formación de filamentos de la RegⅢα humana
Cómo nuestros intestinos combaten los gérmenes
Nuestros intestinos están expuestos constantemente a miles de millones de bacterias, muchas de las cuales son inofensivas o incluso beneficiosas. Pero cuando aparecen microbios peligrosos, nuestro organismo necesita formas rápidas y precisas de atacarlos sin dañar sus propios tejidos. Este estudio examina de cerca una de esas proteínas defensivas naturales, denominada RegIIIα, y revela cómo cambia de forma para matar bacterias y luego se transforma en una forma más segura y menos dañina. Comprender este cambio de conformación podría ayudar a los científicos a entender mejor cómo mantenemos el equilibrio de la microbiota intestinal y qué falla en las enfermedades.
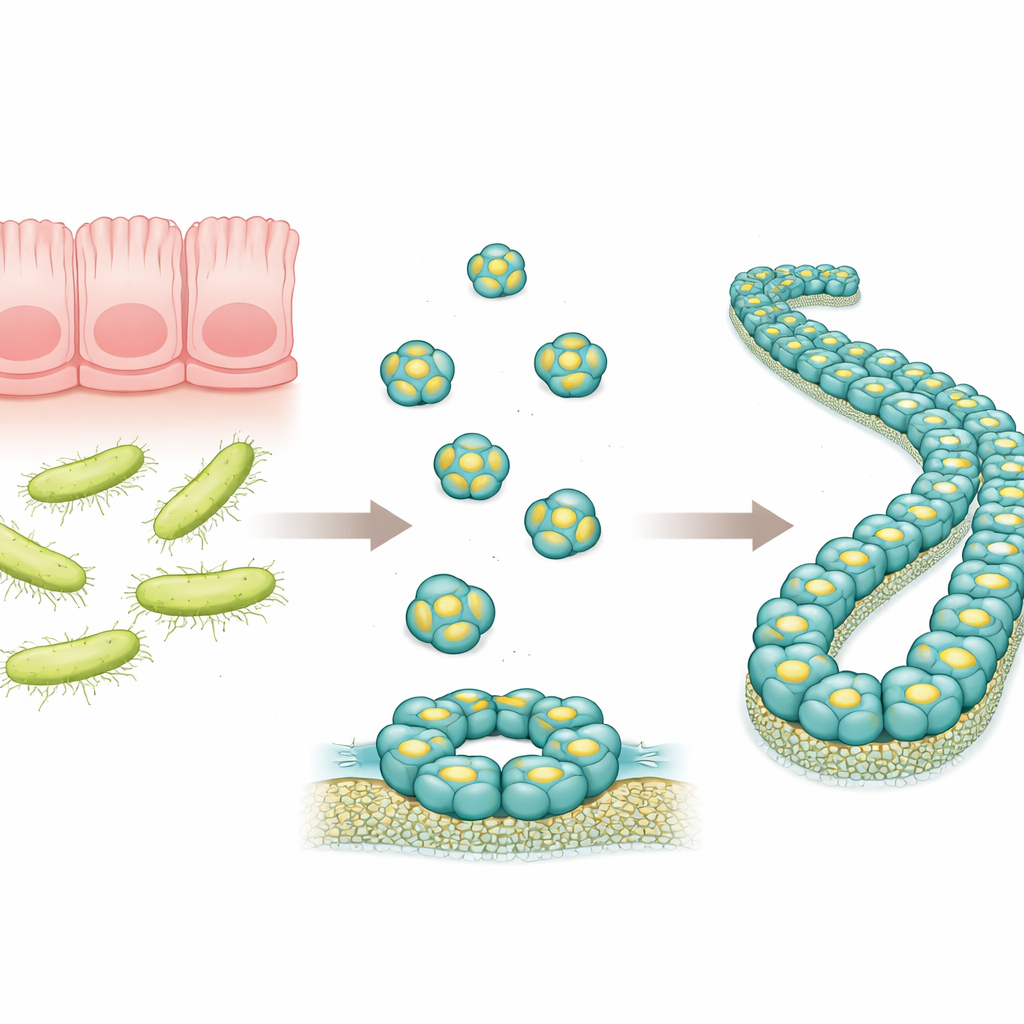
Un pequeño defensor en el intestino
RegIIIα es una proteína producida en el tracto digestivo que se dirige a ciertas bacterias, especialmente a las de pared externa gruesa conocidas como bacterias Gram positivas. Trabajos previos sugerían que RegIIIα puede perforar las membranas bacterianas formando estructuras en forma de anillo, permitiendo que el contenido microbiano se escape y provocando su muerte. Los investigadores también observaron que, con el tiempo, estas estructuras en anillo pueden apilarse en filamentos largos, que parecen reducir el poder bactericida de la proteína. Sin embargo, la disposición exacta de las moléculas de RegIIIα en estos ensamblajes mayores no se conocía con detalle, lo que dificultaba entender cómo funciona la proteína y cómo se regula su actividad.
Ver el filamento con detalle atómico
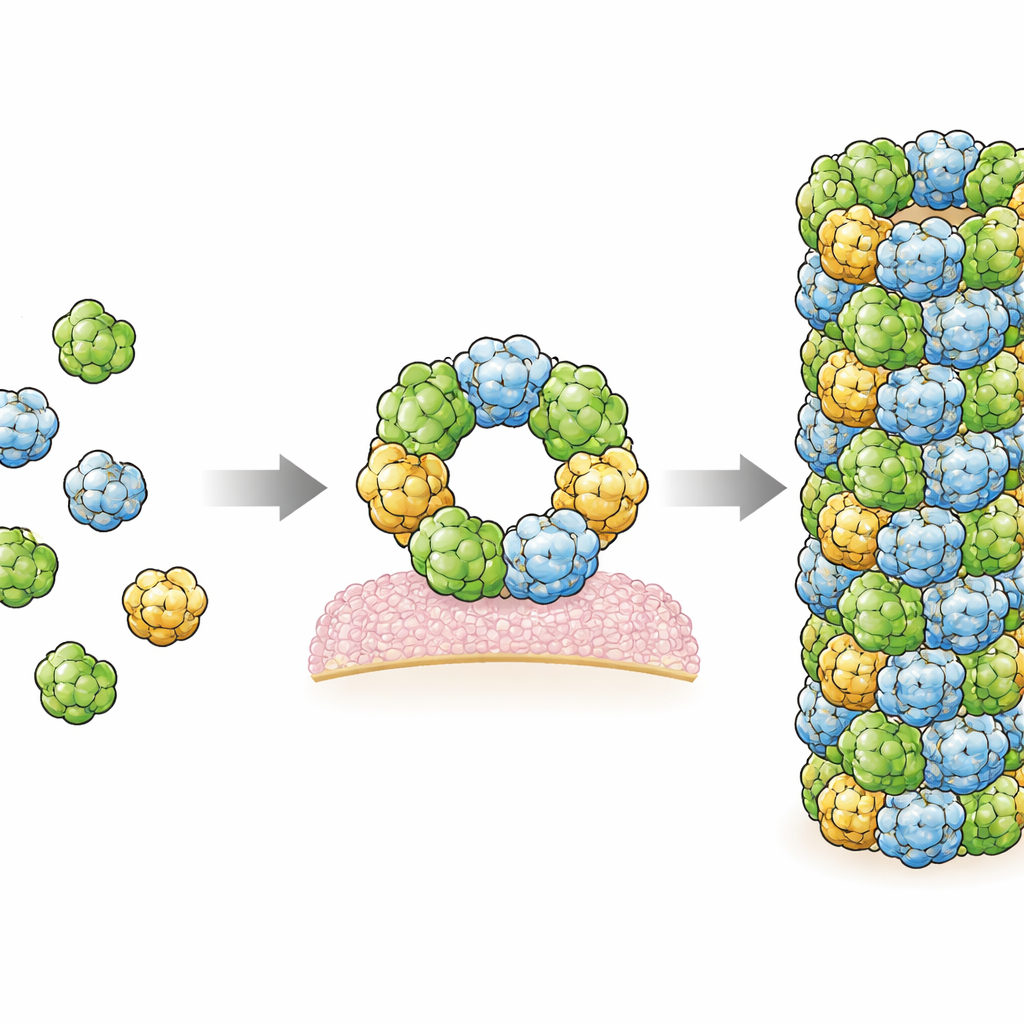
En este trabajo, los autores produjeron RegIIIα humano en bacterias y, a continuación, lo indujeron a ensamblarse en filamentos en condiciones controladas. Emplearon un método de imagen potente llamado crio-microscopía electrónica, que puede visualizar moléculas biológicas congeladas en una fina capa de hielo a resolución casi atómica. Encontraron que los filamentos se construyen a partir de conjuntos repetidos de tres unidades idénticas de RegIIIα, llamadas trírmeros, que se apilan en un patrón helicoidal regular. Cada molécula individual de RegIIIα se parece mucho a lo visto anteriormente en estructuras cristalinas, pero su orientación dentro del filamento difiere de la de un modelo anterior de menor resolución. Esta orientación corregida cambia la forma en que los científicos piensan que la proteína interactúa con las membranas bacterianas y con su propio segmento regulador.
Cómo se enlazan las proteínas y por qué importan los lípidos
Al examinar la estructura de cerca, los investigadores identificaron dos regiones de contacto principales, o interfaces, donde las moléculas vecinas de RegIIIα se tocan y mantienen unido el filamento. Luego modificaron aminoácidos específicos en estas interfaces y demostraron que estos cambios impedían la formación de filamentos, confirmando que estos sitios de contacto son esenciales. De manera interesante, en ambas interfaces, los mapas de crio-EM mostraron regiones borrosas adicionales que probablemente representan pequeñas moléculas alargadas incrustadas entre las superficies proteicas. Su forma y entorno químico sugieren que pueden ser lípidos, los mismos tipos de moléculas oleosas que forman las membranas celulares. Esto respalda indicios previos de que los lípidos ayudan a promover el ensamblaje de RegIIIα, posiblemente actuando como un pegamento molecular que estabiliza las conexiones entre subunidades.
El interruptor de encendido-apagado: pH y un segmento oculto
El equipo también investigó qué controla cuándo RegIIIα puede ensamblarse. Antes de volverse activa, la proteína porta un corto “pro-segmento” que debe ser cortado por enzimas digestivas. En su estructura de filamento de alta resolución, no hay espacio en el centro del ensamblaje para acomodar este fragmento adicional, lo que implica que el pro-segmento bloquea la capacidad de RegIIIα para formar los anillos formadores de poros y los filamentos en primer lugar. Encontraron que la tendencia a formar filamentos también depende de la acidez: los filamentos se forman con facilidad a un pH similar al del intestino delgado, pero pobremente a un pH más ácido. Un único aminoácido, la histidina 50, parece actuar como un interruptor sensible al pH; cuando se sustituye por otro residuo, la formación de filamentos pierde gran parte de su sensibilidad al pH. En conjunto, estas características—corte enzimático, unión a lípidos y pH—crean un sistema de control por capas que ajusta cuándo y dónde RegIIIα está activo.
Qué significa esto para la salud intestinal
En conjunto, este trabajo ofrece la imagen más detallada hasta la fecha de cómo las moléculas de RegIIIα se ensamblan en estructuras mayores relacionadas tanto con su acción antibacteriana como con su comportamiento auto-limitante. Las mismas interfaces que construyen los filamentos también forman los anillos hexaméricos que se piensa crean poros en membranas bacterianas, lo que sugiere un equilibrio delicado entre una forma potente de matar y un estado más moderado y seguro. Mapear mutaciones asociadas a enfermedades sobre esta estructura muestra que muchas se sitúan en puntos de contacto clave, lo que indica que las alteraciones en el ensamblaje pueden estar en la base de ciertos trastornos intestinales o pancreáticos. Al aclarar cómo se activa este antibiótico natural, cómo lo guían los lípidos y cómo lo modula el pH local, el estudio sienta las bases para futuros esfuerzos destinados a modular nuestras defensas innatas—ya sea potenciándolas frente a infecciones o calmándolas cuando se desregulan.»
Cita: Han, J., Cao, Q. Structural basis for human RegⅢα filament formation. Commun Chem 9, 117 (2026). https://doi.org/10.1038/s42004-026-01921-y
Palabras clave: RegIIIα, inmunidad intestinal, crio-microscopía electrónica, filamentos proteicos, péptidos antibacterianos