Clear Sky Science · es
Glicosidos anfifílicos jano ionizables puenteados con azobenceno para la entrega de pDNA controlada por luz, de componente único y modulable por órgano
Iluminando una entrega génica más inteligente
Las terapias génicas prometen tratar las enfermedades en su origen al entregar fragmentos de código genético directamente en nuestras células. Pero dirigir esta carga frágil de forma segura a través del torrente sanguíneo, hacia los órganos correctos y dentro de las células diana sigue siendo un gran obstáculo. Este estudio presenta una nueva clase de partículas diminutas basadas en azúcares cuyo comportamiento puede conmutarse con luz antes incluso de entrar en el cuerpo, lo que permite a los investigadores redirigir dónde termina un gen terapéutico y con qué intensidad se expresa, todo ello manteniendo las células en gran medida indemnes. 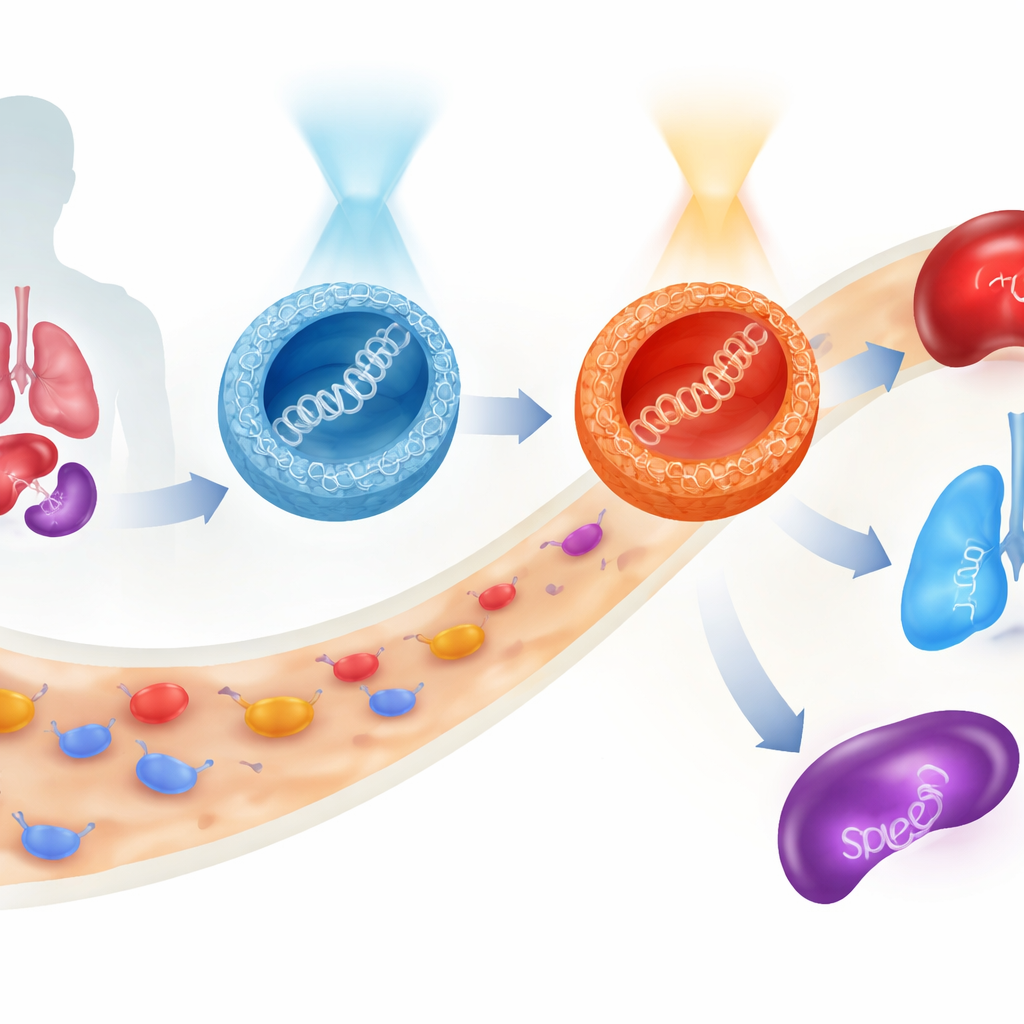
La necesidad de mensajeros genéticos precisos
Los vehículos de entrega génica más exitosos hoy en día son las nanopartículas lipídicas, que hicieron posible las vacunas de ARNm contra la COVID-19. Estas gotas multicomponentes envuelven y protegen los ácidos nucleicos, pero tienden a acumularse principalmente en el hígado y a liberar solo una pequeña fracción de su carga dentro de las células. Ajustar sus composiciones puede cambiar qué órganos prefieren, sin embargo las mezclas son complejas y difíciles de controlar con precisión. El equipo detrás de este trabajo, en cambio, se propuso diseñar moléculas únicas y bien definidas que se ensamblen en nanopartículas con formas y comportamientos predecibles—y que puedan ajustarse activamente desde el exterior mediante un simple disparador de luz.
Una balanza molecular controlada por la luz
En el corazón del nuevo sistema están los diales gemelos «Janus» glicosídicos: moléculas formadas por dos unidades de glucosa, provistas de cabezas cargadas hidrofílicas y colas hidrofóbicas, unidas por una «bisagra» central de azobenceno. El azobenceno puede alternar entre dos formas espejo, llamadas E y Z, cuando se expone a diferentes colores de luz. En agua con ADN presente, muchas copias de estas moléculas se agrupan espontáneamente en partículas suaves y estratificadas que envuelven hebras de ADN plasmídico. Los investigadores prepararon dos versiones—una con puentes de oxígeno y otra con puentes de azufre entre el azúcar y la bisagra—para ajustar sutilmente la estabilidad y el comportamiento biológico. Mediante la preirradiación de las soluciones, pudieron enriquecer ya sea la forma E o la Z y estudiar cómo cada estado moldea las partículas resultantes de entrega génica.
Cómo se comportan las partículas que cambian de forma
Las mediciones de tamaño de partícula, carga superficial y estructura interna mostraron que la conmutación inducida por luz entre los estados E y Z tiene consecuencias físicas claras. En general, la forma Z produjo nanopartículas más pequeñas, de forma más uniforme y con un interior más ordenado y estratificado que la forma E. La microscopía reveló que estos arreglos internos se asemejan a láminas alternadas de material tipo lípido y ADN. De forma importante, ambos estados protegieron el ADN de la degradación enzimática. En cultivos celulares procedentes de riñón, hígado y tejido inmune, los distintos estados isómeros produjeron niveles marcadamente diferentes de expresión génica, aunque el ADN subyacente fuera idéntico. Pulsos de luz repetidos aplicados después de que las partículas hubieran entrado en las células incrementaron la expresión génica varias veces, lo que sugiere que el sacudimiento mecánico derivado del cambio ayuda a aflojar las partículas y liberar su carga, y puede también facilitar su escape de compartimentos intracelulares. 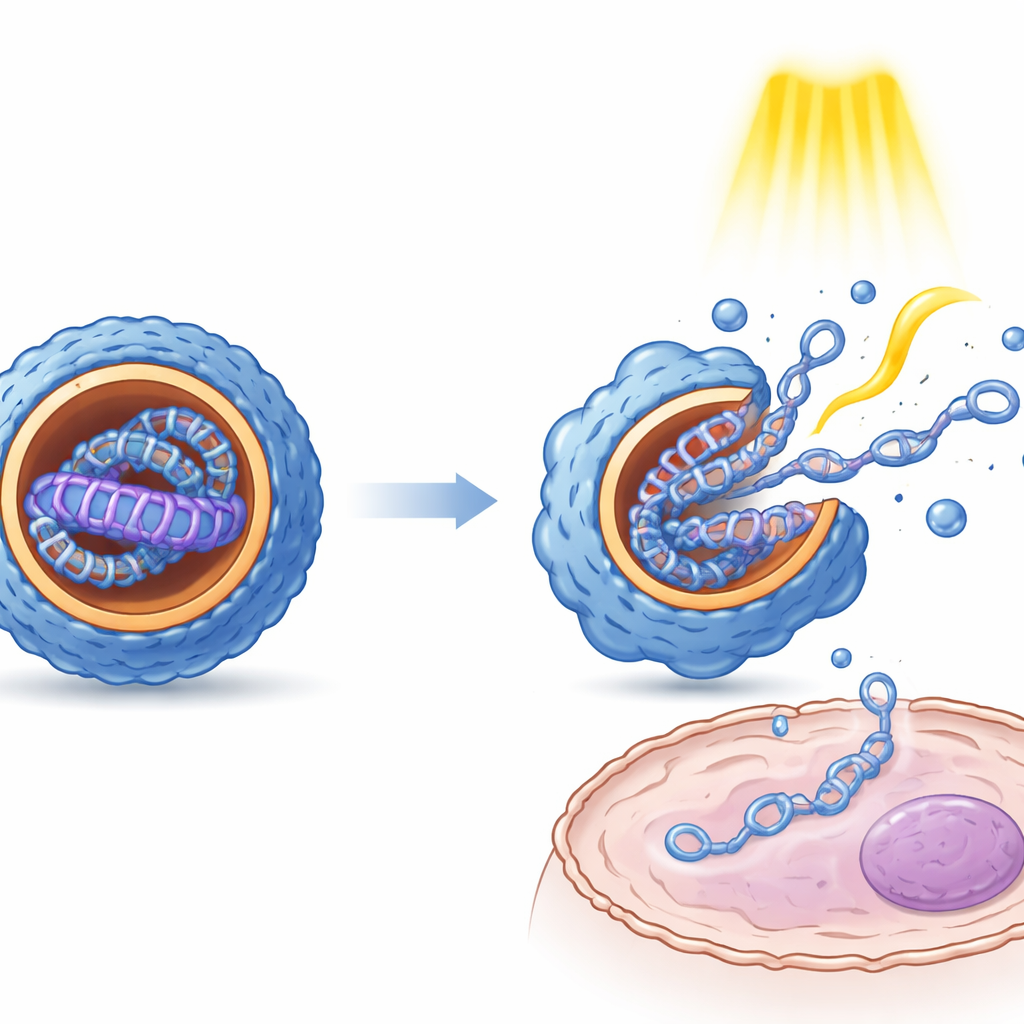
Guiando genes hacia órganos específicos
El comportamiento más sorprendente apareció en ratones. Cuando las partículas puenteadas con oxígeno se administraron en su forma rica en E, la expresión de un gen marcador se produjo mayoritariamente en el hígado con algo en los pulmones. Preconmutarlas a la forma Z antes de la inyección no solo aumentó la expresión total, sino que además desplazó el equilibrio hacia los pulmones. Las partículas puenteadas con azufre contaron otra historia: su forma Z favoreció el bazo, un órgano clave del sistema inmune. Así, con el mismo armazón molecular básico—y sin cambiar la carga de ADN—los investigadores pudieron dirigir la actividad génica predominantemente al hígado, pulmón o bazo simplemente eligiendo el enlace (oxígeno o azufre) y la forma activada por luz (E o Z) del transportador. A lo largo de estas pruebas, la viabilidad celular se mantuvo alta, lo que sugiere que el sistema es relativamente suave.
Una vía modulable por luz hacia futuras medicinas génicas
En términos cotidianos, el equipo ha construido un diminuto transbordador de ADN con conmutador de luz. Antes de la inyección, un breve tratamiento lumínico «programa» los transbordadores en una de dos formas. Cada forma se ensambla en nanopartículas con tamaño y tacto superficial característicos, lo que a su vez determina con qué fuerza se adhieren a distintos tipos celulares y dónde acaban en el cuerpo. Dado que el mismo andamiaje químico puede modificarse de muchas maneras pequeñas, y porque la conmutación es reversible y no altera el ADN en sí, esta plataforma ofrece una vía flexible para afinar dónde y cómo actúan las terapias génicas. Aunque queda mucho trabajo antes del uso clínico, el estudio muestra que transportadores de molécula única cuidadosamente diseñados y controlados por luz podrían convertirse en herramientas poderosas para medicinas genéticas más seguras y precisas.
Cita: Wang, Z., Rivero-Barbarroja, G., Benito, J.M. et al. Azobenzene-bridged ionizable amphiphilic Janus glycosides for light-controlled, single-component and organ-modulable pDNA delivery. Commun Chem 9, 118 (2026). https://doi.org/10.1038/s42004-026-01920-z
Palabras clave: entrega génica, nanopartículas sensibles a la luz, conmutadores de azobenceno, terapia dirigida con ADN, nanomedicina