Clear Sky Science · es
La proteasa S9 WprP2 cataliza un corte uniforme en el péptido precursor en la biosíntesis de RiPP
Por qué importan las pequeñas herramientas de corte en las células
Dentro de las bacterias, unas tijeras moleculares especializadas cortan largas cadenas de aminoácidos en fragmentos más pequeños y activos que con frecuencia se convierten en antibióticos u otros productos naturales útiles. Este estudio descubre una herramienta de corte desconocida hasta ahora —una proteasa llamada WprP2— que recorta su péptido diana con una precisión inusual. Comprender cómo funciona esta enzima podría ayudar a los científicos a diseñar nuevos péptidos bioactivos y antibióticos de próxima generación.
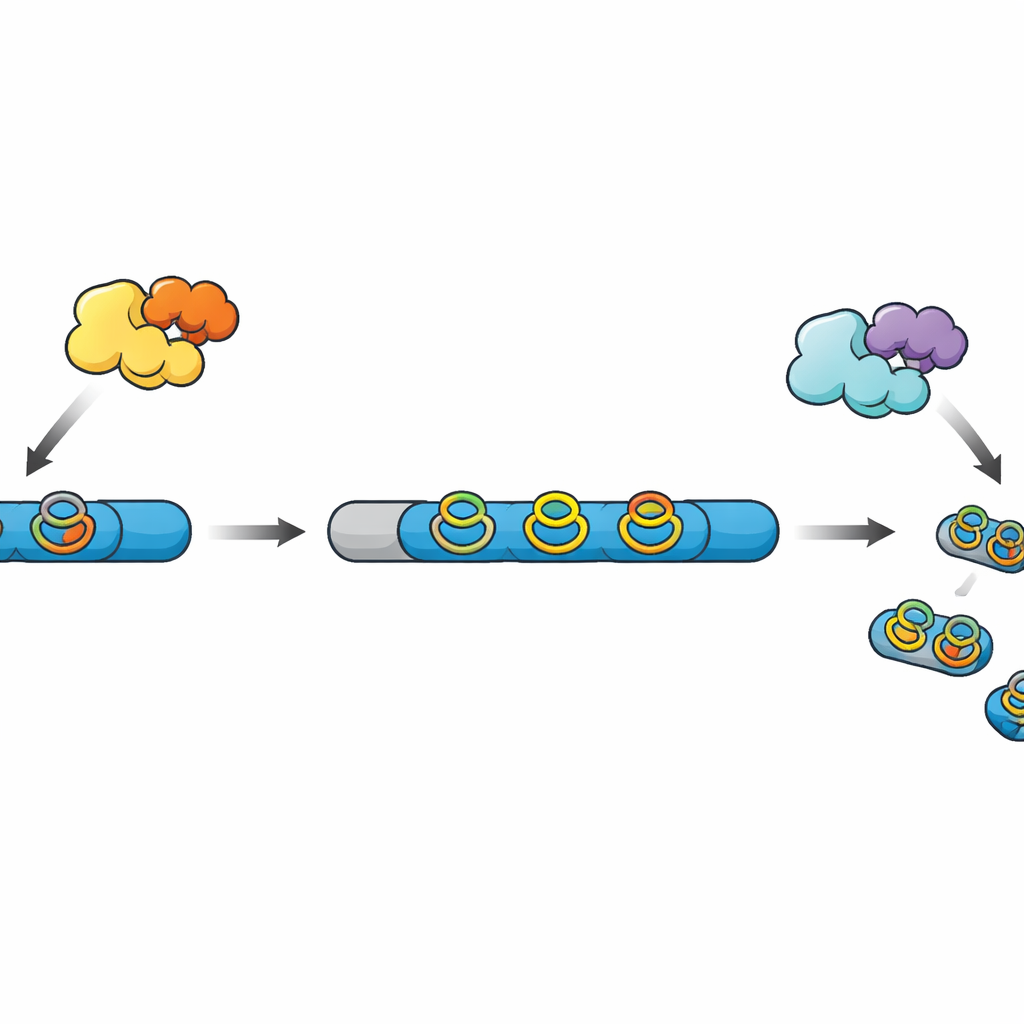
De cadenas brutas a mini‑medicamentos terminados
Muchos productos naturales modernos basados en péptidos, conocidos colectivamente como RiPPs, comienzan como cadenas sencillas sintetizadas en el ribosoma. Estas cadenas contienen una región líder que actúa como un asa y una región núcleo que se convertirá en el producto final tras una serie de modificaciones químicas. Otras enzimas añaden enlaces transversales y anillos que hacen al péptido más estable y más activo, y finalmente una proteasa elimina la región líder y libera la molécula madura. En una familia de RiPPs descubierta recientemente, las enzimas radical SAM construyen anillos compactos tipo “ciclofano” que involucran aminoácidos aromáticos, pero en la mayoría de los clústeres de genes conocidos falta la proteasa correspondiente, lo que deja misteriosos los pasos finales del procesamiento.
Rastreando a la enzima compañera perdida
Los autores habían estudiado previamente una enzima radical SAM llamada WprB1 que instalaba enlaces idénticos en tres repeticiones WPR de un péptido precursor. En el trabajo nuevo, buscaron en genomas bacterianos parientes de esa enzima y examinaron los genes cercanos en busca de posibles codificadores de una proteasa. En Streptomyces venezuelae encontraron un clúster prometedor que contenía una enzima de entrecruzamiento similar, su proteína ayudante, un péptido precursor compatible con tres repeticiones WPR y una candidata proteasa de serina de la familia S9, que nombraron WprP2. Esto convirtió al sistema en un banco de pruebas ideal para descubrir cómo se corta finalmente el péptido para liberar los fragmentos activos.
Observando cómo se corta el péptido
Para sondear a WprP2, el equipo produjo el péptido precursor en bacterias, tanto con la enzima de entrecruzamiento como sin ella, lo purificó y luego lo mezcló con la proteasa en reacciones in vitro controladas. La espectrometría de masas reveló que WprP2 primero corta la cadena inmediatamente después de cada segmento WPR y luego realiza un segundo corte a una distancia fija antes de una prolina concreta más adelante en la secuencia. Estos dos pasos crean una serie de fragmentos más pequeños y uniformes. De manera notable, WprP2 efectuó este patrón de cortes tanto si la enzima de entrecruzamiento ya había instalado los anillos ciclofano como si no, lo que muestra que los anillos no son necesarios para el reconocimiento. En comparación con la tripsina comercial, que no puede cortar en ciertos sitios entrecruzados, WprP2 siguió funcionando, subrayando su inusual robustez.
Descifrando qué reconoce la enzima
Los investigadores preguntaron después qué características del péptido reconoce realmente WprP2. Al cambiar sistemáticamente aminoácidos individuales alrededor de los sitios de corte, encontraron que alterar muchos residuos cercanos tenía poco efecto, pero modificar una arginina clave dentro del segmento WPR o la glutamina o la prolina en el segundo sitio de corte podía bloquear ese paso particular. Experimentos con un péptido precursor relacionado que llevaba residuos flanqueantes distintos mostraron que la proteasa seguía cortando tras las repeticiones WPR pero solo efectuaba el segundo corte cuando estaba presente un par glutamina‑prolina. Modelos estructurales generados por ordenador con AlphaFold3 respaldaron este panorama: en los complejos predichos, los sitios basados en WPR y en glutamina‑prolina se alineaban a su vez con el centro catalítico de la enzima, coherente con un mecanismo secuencial de dos pasos.
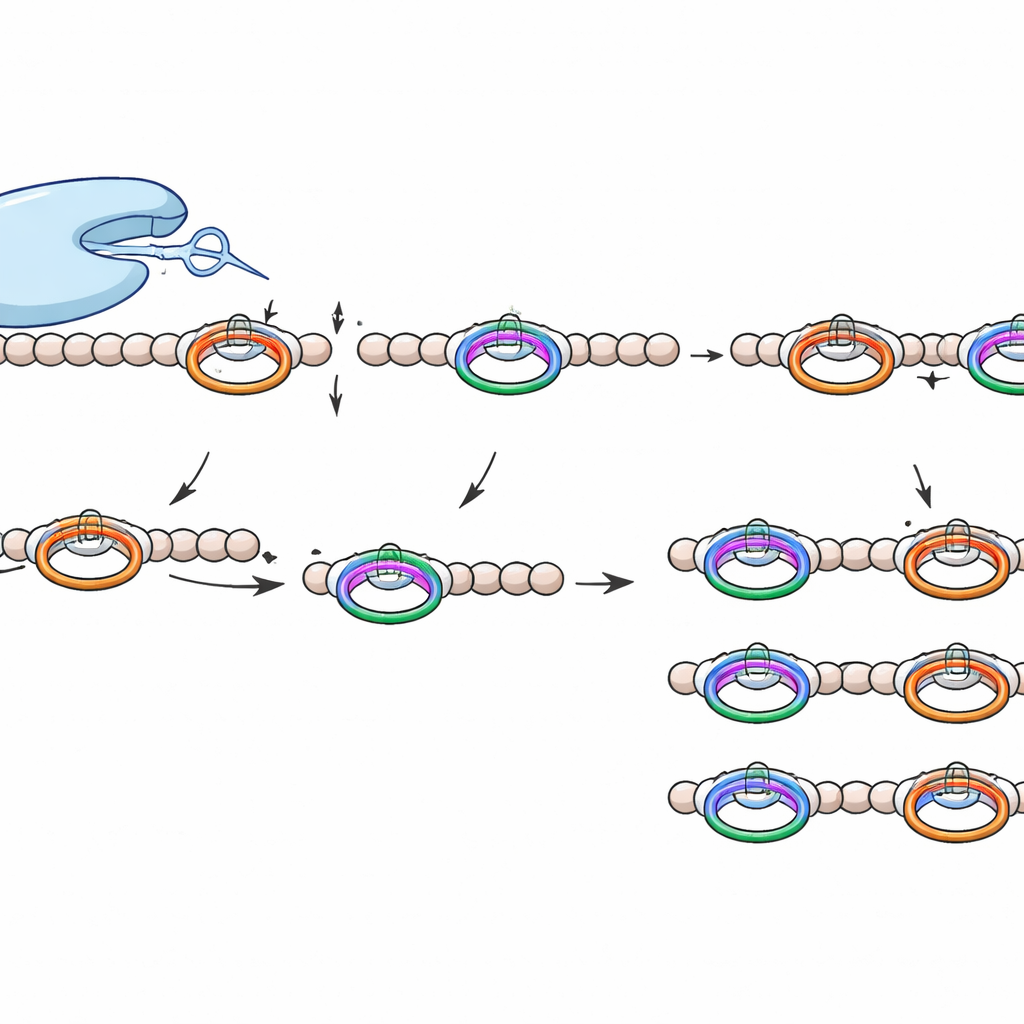
Qué hace especial a esta herramienta de corte
WprP2 pertenece a una amplia familia S9 de proteasas que ya incluye enzimas de relevancia médica, pero destaca por varios motivos. Corta en el lado N‑terminal de una prolina en lugar de después de ella, actúa sobre un motivo repetido para generar fragmentos de tamaño uniforme a lo largo de toda la cadena precursora y muestra una gran tolerancia a los aminoácidos que yacen entre sus dos sitios de reconocimiento. Esta combinación de precisión y flexibilidad no se había observado antes en proteasas relacionadas con RiPP.
Cómo podría emplearse este descubrimiento
Al revelar una proteasa que reconoce señales de secuencia sencillas y realiza cortes uniformes y repetidos, este trabajo añade una nueva herramienta potente al creciente conjunto de recursos para la ingeniería de péptidos. En términos prácticos, WprP2 podría aprovecharse para liberar o remodelar péptidos diseñados, incluidas aquellas moléculas con entrecruzamientos complejos que resisten a enzimas estándar como la tripsina. Para el público general, la idea clave es que los científicos han descubierto un nuevo tipo de tijeras moleculares que cortan largas cadenas peptídicas en piezas precisas y de tamaño uniforme, abriendo la puerta a una producción más controlada de potenciales antibióticos y otras moléculas bioactivas.
Cita: Haedar, J.R., Khan, A.H., Ma, S. et al. S9 protease WprP2 catalyzes uniform cleavage on the precursor peptide in RiPP biosynthesis. Commun Chem 9, 108 (2026). https://doi.org/10.1038/s42004-026-01915-w
Palabras clave: RiPP peptides, serina proteasa, WprP2, productos naturales ciclofano, ingeniería de péptidos