Clear Sky Science · es
Sonda de emisión inducida por confinamiento estérico para monitorizar conformaciones proteicas en células vivas
Vigilar proteínas que cambian de forma en tiempo real
Dentro de cada célula viva, las proteínas cambian de forma constantemente mientras transmiten señales, perciben su entorno y realizan tareas vitales. Muchas enfermedades surgen cuando estos cambios conformacionales fallan, pero ha sido notablemente difícil observar tales movimientos directamente en células vivas, especialmente abarcando tanto escalas temporales muy rápidas como lentas. Este trabajo presenta una nueva sonda emisora de luz, llamada BIOSCE, que convierte pequeños movimientos proteicos en destellos visibles, permitiendo a los investigadores seguir proteínas individuales mientras se doblan, giran e interactúan en tiempo real dentro de células vivas. 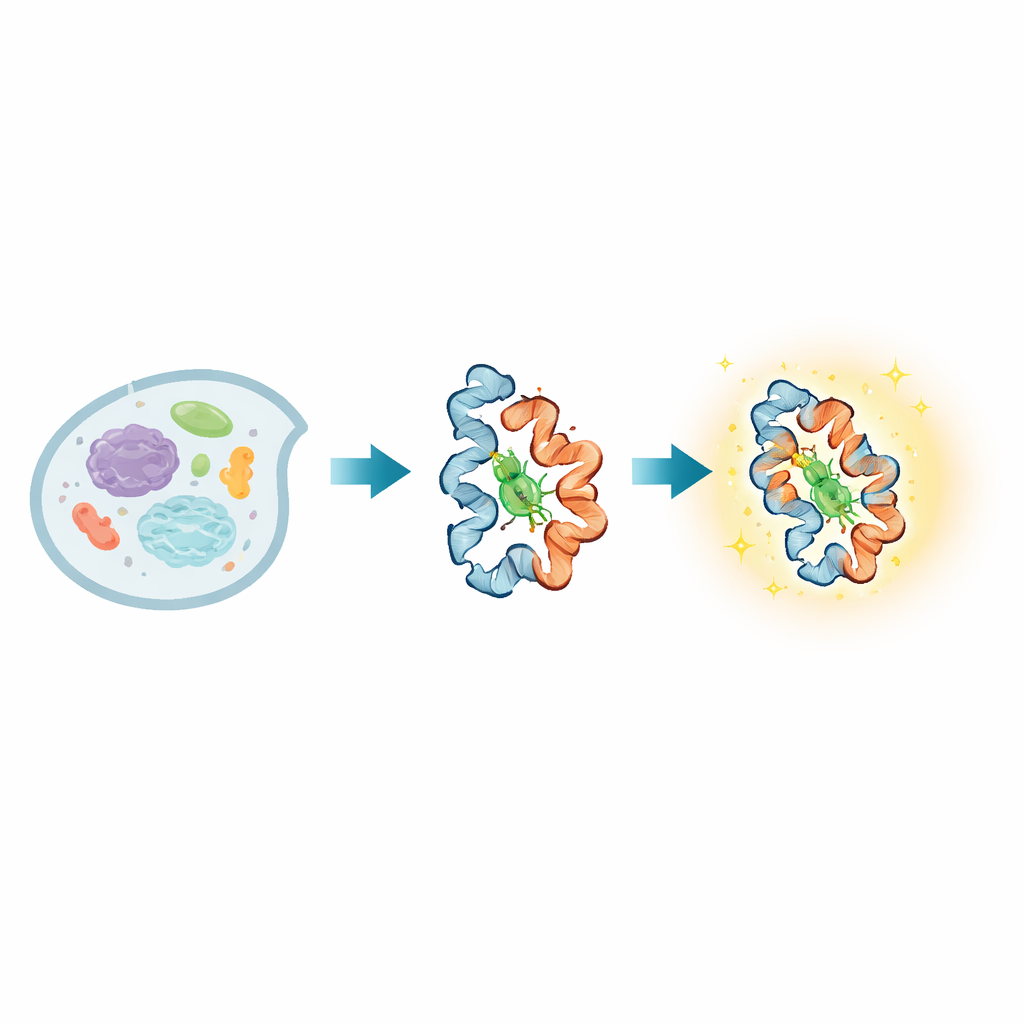
Un nuevo interruptor lumínico para proteínas en movimiento
En el núcleo de BIOSCE hay una pequeña molécula colorante, MTPABP-Cl, que se vuelve más brillante cuando se la comprime. Los autores unen este colorante a una etiqueta proteica de uso general llamada HaloTag, que puede fusionarse genéticamente a casi cualquier proteína de interés. Cuando la proteína etiquetada cambia de forma o se empaqueta más estrechamente con sus vecinas, altera el “espacio” que tiene el colorante para moverse. En un entorno holgado, las partes internas del colorante pueden rotar libremente y la mayor parte de la luz absorbida se pierde en movimiento; en un bolsillo más estrecho, esos movimientos quedan bloqueados y el colorante libera más de esa energía en forma de luz. Esta “emisión inducida por confinamiento estérico” convierte desplazamientos sutiles en la aglomeración local alrededor de una sola proteína en un cambio continuo de brillo, en lugar de una señal simplemente de encendido/apagado, lo que hace que la sonda sea muy sensible a pequeños cambios conformacionales.
Construcción y prueba del colorante sensible a la compresión
El equipo diseñó y sintetizó en primer lugar MTPABP-Cl para que fuera tenue en solución pero se iluminara cuando quedara fijado por HaloTag o por una proteína de fusión más compacta. Mediciones cuidadosas mostraron que el colorante absorbe luz azul y emite en el rojo lejano, lo que favorece la imagen en profundidad dentro de las células y la observación a largo plazo. Cuando está unido solo a HaloTag, su emisión aumentó; cuando HaloTag se fusionó a una proteína compañera que se plegó alrededor del colorante, el brillo se incrementó aún más. Simulaciones por ordenador confirmaron que, en arreglos proteicos más compactos, el colorante experimenta una mayor congestión, una superficie expuesta menor y más contactos estabilizadores, todo lo cual restringe el movimiento y mejora la emisión. El colorante también se une de forma rápida y específica a HaloTag, muestra muy bajo fondo en células que carecen de la etiqueta y permanece no tóxico a las concentraciones de trabajo, lo que respalda su uso en experimentos en células vivas. 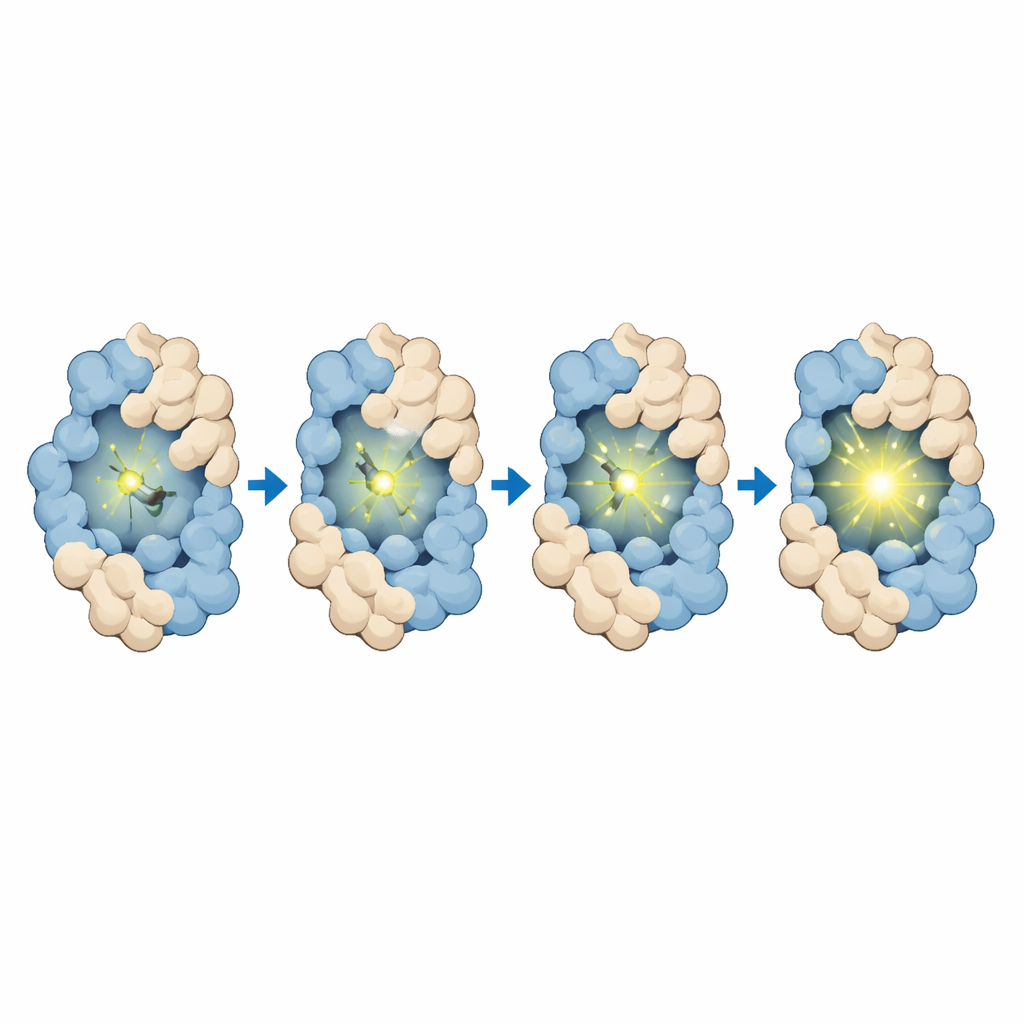
Siguiendo señales rápidas y encuentros proteicos
Para demostrar lo que BIOSCE puede hacer, los autores lo aplicaron a varios procesos celulares bien conocidos. Primero, adaptaron un sensor de calcio basado en calmodulina, una proteína que cambia de forma al unirse a iones calcio —mensajeros centrales en la actividad neuronal y muchos otros eventos celulares. Al fusionar calmodulina a HaloTag y etiquetarla con MTPABP-Cl, crearon un indicador quimigenético llamado SCECaMP. En células humanas y células de tipo neuronal, este indicador se iluminó y se apagó al ritmo de los picos de calcio inducidos por estimulación con potasio, con velocidades de respuesta comparables a las de las proteicas fluorescentes GCaMP ampliamente utilizadas. Dado que la señal BIOSCE depende directamente de la aglomeración local alrededor del colorante, puede reflejar fielmente los cambios estructurales de la calmodulina al tiempo que ofrece una fluorescencia estable y duradera adecuada para imágenes prolongadas.
Ver interacciones inducidas por fármacos y daños por toxinas
Los investigadores preguntaron a continuación si BIOSCE podía seguir cuando dos proteínas se aproximan por acción de un fármaco. Usaron un sistema clásico en el que la rapamicina acerca a dos socios, FKBP y FRB, en una vía clave de control del crecimiento. Al unir HaloTag a FKBP o a FRB y etiquetar con MTPABP-Cl, observaron aumentos rápidos de fluorescencia en escala de milisegundos cuando la rapamicina indujo que estas proteínas se aproximaran y reordenaran. El incremento de brillo reflejó un microentorno más estrecho alrededor del colorante conforme los socios se pusieron en proximidad cercana. En una prueba más compleja, estudiaron SNAP25, una proteína terminal nerviosa crucial para la liberación de neurotransmisores y el principal blanco de la neurotoxina botulínica A. Colocando HaloTag a ambos lados del sitio de corte de la toxina y etiquetando con el colorante, pudieron seguir por separado los movimientos de los fragmentos N-terminal y C-terminal tras la escisión. El seguimiento de partículas individuales reveló que un fragmento permanecía anclado cerca de la membrana celular, mientras que el otro se difundía con mayor libertad por el citoplasma, y que el patrón exacto dependía de si el marcado se realizó antes o después de la exposición a la toxina. La sonda incluso informó de ajustes conformacionales rápidos inducidos por zinc en SNAP25 durante este proceso.
Qué significa esto para la biología y la medicina
En conjunto, estos resultados muestran que BIOSCE es una nueva y versátil manera de visualizar cómo las proteínas individuales se mueven, pliegan e interactúan dentro de células vivas a lo largo de una amplia gama de escalas temporales. Como el método se basa en una fusión general HaloTag y una sola molécula colorante pequeña, en principio puede aplicarse a muchas proteínas distintas sin rediseñar por completo el sensor en cada caso. El cambio continuo de brillo dependiente del confinamiento permite a los investigadores detectar desplazamientos estructurales sutiles en lugar de solo eventos grandes y binarios. De cara al futuro, los autores planean mejorar la entrega de la sonda y la profundidad de imagen para que BIOSCE pueda usarse en tejidos y animales enteros. Si tiene éxito, este enfoque podría convertirse en una herramienta poderosa para vincular dónde están las proteínas, cómo se mueven y qué hacen en la salud y la enfermedad, y podría en última instancia alimentar modelos computacionales detallados del comportamiento celular.
Cita: Jia, H., Yang, L., Yang, Y. et al. Steric confinement-induced emission probe for monitoring protein conformations in live cells. Commun Chem 9, 109 (2026). https://doi.org/10.1038/s42004-026-01914-x
Palabras clave: dinámica conformacional de proteínas, imagen en células vivas, biosensores fluorescentes, sondas HaloTag, neurotoxina botulínica