Clear Sky Science · es
Diazotización directa de indoles con nitrito de 2-metoxietilo
Convertir un gas problemático en química útil
El óxido nítrico suele considerarse un gas industrial problemático: es tóxico, difícil de manipular y normalmente tratado como residuo. Sin embargo, también es rico en nitrógeno, un elemento clave en muchos medicamentos. Este estudio muestra cómo los químicos pueden domar el óxido nítrico convirtiéndolo en un reactivo líquido estable que, a su vez, ayuda a construir moléculas complejas relacionadas con candidatos farmacéuticos. El trabajo ofrece una vía para transformar un subproducto peligroso en una herramienta para fabricar compuestos valiosos de forma más segura y limpia.
Una nueva molécula auxiliar para reacciones difíciles
Los químicos recurren con frecuencia a compuestos “diazo”: moléculas que contienen un par de átomos de nitrógeno muy reactivo, para construir entramados carbonados intrincados. Estos entramados aparecen en muchos fármacos, especialmente los basados en indoles, un sistema de anillos común en productos naturales y medicamentos. Las formas tradicionales de preparar compuestos diazo suelen emplear azidas explosivas o grandes cantidades de ácidos y bases fuertes, lo que plantea problemas de seguridad y medioambientales. Los autores se centran en una alternativa más segura: un líquido llamado nitrito de 2‑metoxietilo, o MOE‑ONO, que puede obtenerse directamente a partir de óxido nítrico gaseoso, oxígeno y un alcohol simple, generando solo agua como subproducto.
Reaccionando directamente un anillo importante similar a fármacos
El equipo se propuso instalar grupos diazo directamente sobre indoles, modificándolos en una posición precisa del anillo sin condiciones agresivas. Descubrieron que combinar MOE‑ONO con un radical orgánico común, TEMPO, y una pequeña cantidad de una sal metálica catalítica a base de escandio desencadena esta transformación de forma eficiente. En comparación con las mezclas clásicas de nitrito de sodio y ácido, o con otros donantes líquidos de óxido nítrico como el nitrito de terc‑butilo, la nueva combinación ofrece rendimientos superiores, muchos menos subproductos no deseados y funciona en tiempos mucho más cortos. Incluso indoles que habían resistido métodos anteriores —como aquellos con grupos fenilo voluminosos— pudieron convertirse limpiamente usando este enfoque.
Un método, muchos bloques de construcción
Tras optimizar la reacción, los investigadores evaluaron su alcance. Encontraron que una amplia variedad de derivados de indol toleraban las condiciones, incluidos aquellos que llevan ésteres, cetonas, amidas y distintos sustituyentes alrededor del anillo, desde grupos alquilo y metoxi ricos en electrones hasta halógenos y grupos ciano. El método también se extendió más allá de los indoles a compuestos relacionados como los naftoles, formando derivados diazo que previamente requerían procedimientos largos y en varios pasos. Es notable que la reacción siguiera funcionando cuando se realizó en agua, aunque los materiales de partida no sean muy solubles en ella. Este comportamiento denominado “en agua” sugiere que simplemente agitar la mezcla en agua proporciona un medio más ecológico que ayuda a que la reacción progrese mientras reduce la dependencia de disolventes orgánicos.
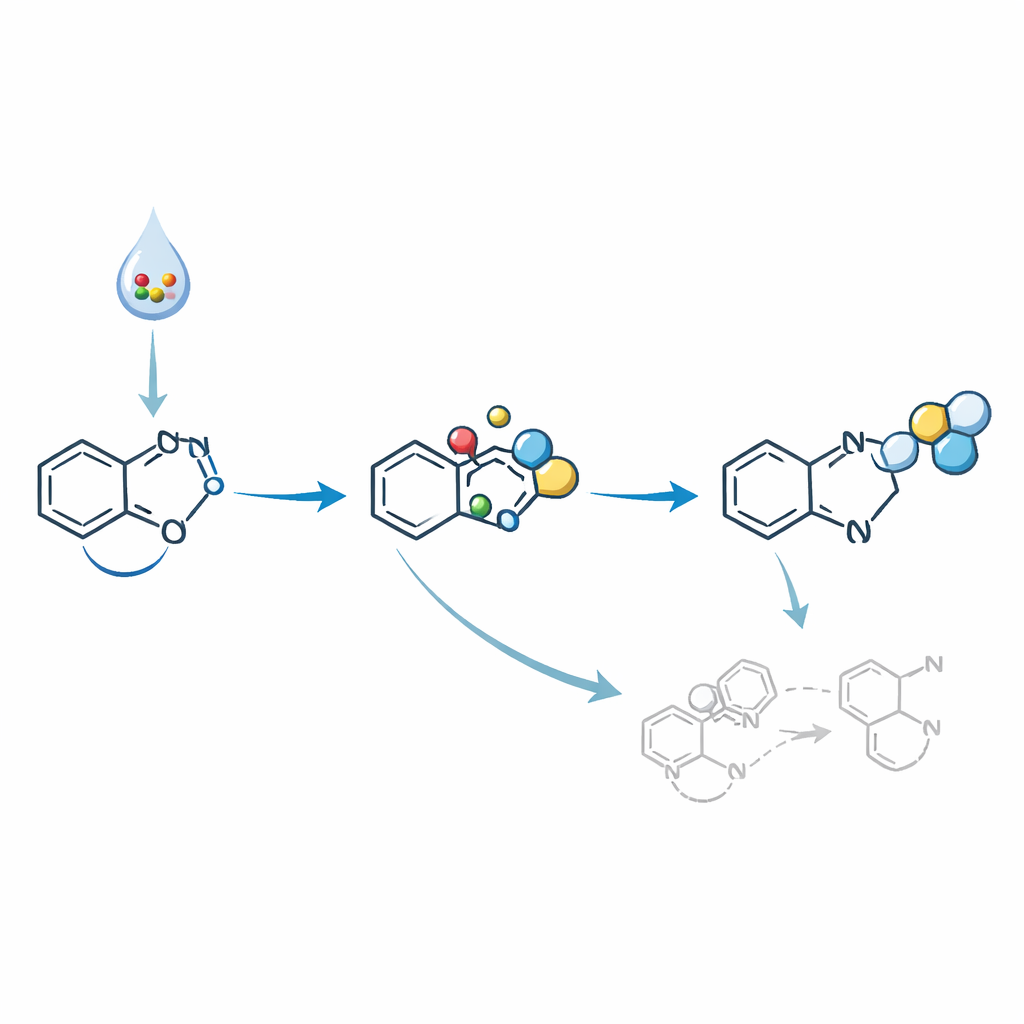
De intermedios reactivos a candidatos farmacéuticos
Para mostrar el valor de estos diazoindoles, los autores los transformaron además en moléculas más elaboradas. Usando un catalizador de rodio, convirtieron el grupo diazo en un intermediario muy reactivo llamado carbeno, que luego formó nuevos enlaces para construir anillos de ciclopropano en posiciones específicas del indol. En otra secuencia, ensamblaron un candidato modulador para un receptor implicado en el control del azúcar en sangre, demostrando la relevancia del método para la química medicinal. También mostraron que reactivos de Grignard —herramientas clásicas para añadir carbonos— podían unirse selectivamente en una posición del diazoindol dejando intacto el grupo diazo, abriendo la puerta a la construcción escalonada de estructuras densamente sustituidas de indol e indolina.
Cómo la reacción se mantiene en la senda correcta
Tras bambalinas, varias vías competitivas podrían dar lugar a productos indeseados como nitro o oxima en lugar de los diazo deseados. Experimentos mecanísticos sugieren que TEMPO ayuda a encauzar la química al atrapar radicales nocivos y capturar un fugaz intermedio nitroso antes de que pueda reordenarse. Moléculas adicionales de óxido nítrico se añaden después en secuencia, produciendo finalmente el grupo diazo y liberando nitrato inocuo. La sal de escandio parece promover la descomposición de MOE‑ONO en especies reactivas y activar el núcleo del indol, mejorando aún más la eficiencia. La detección de nitrato en la mezcla final respalda esta ruta propuesta desde el donante de óxido nítrico hasta el producto diazo.
Vía segura y sostenible hacia moléculas complejas
En conjunto, este trabajo presenta una forma práctica de instalar grupos diazo altamente útiles en anillos de indol sin depender de reactivos explosivos ni de condiciones agresivas. Al usar un líquido estable derivado del óxido nítrico gaseoso, el método tanto “recicla” una emisión industrial problemática como agiliza el acceso a moléculas complejas con carácter farmacológico. Para los no especialistas, el mensaje clave es que la química ingeniosa puede transformar un gas tóxico de desecho en un bloque de construcción versátil para futuros medicamentos, al tiempo que reduce el impacto ambiental.
Cita: Hashidoko, A., Kitanosono, T., Nakao, Y. et al. Direct diazotization of indoles with 2-Methoxyethyl nitrite. Commun Chem 9, 104 (2026). https://doi.org/10.1038/s42004-026-01910-1
Palabras clave: reciclaje de óxido nítrico, diazoindoles, síntesis orgánica ecológica, fármacos basados en indoles, reactivos donantes de NO