Clear Sky Science · es
Consumo de muestra minimizado para cristalografía serial resuelta en el tiempo aplicada al ciclo redox de la NQO1 humana
Observar enzimas en acción con menos muestras valiosas
La biología moderna suele apoyarse en potentes láseres de rayos X para ver cómo se mueven y cambian de forma las moléculas de la vida, pero estos experimentos normalmente consumen grandes cantidades de proteína preparada con mucho esfuerzo. Este estudio presenta una nueva manera de “alimentar” diminutos cristales de proteína hacia un láser de electrones libres de rayos X con mucha más eficiencia, reduciendo el material necesario hasta en un 97%. Además, muestra que este método más económico puede captar los primeros pasos en la actividad de una enzima humana de interés médico, abriendo la puerta a grabaciones más rutinarias de proteínas en acción. 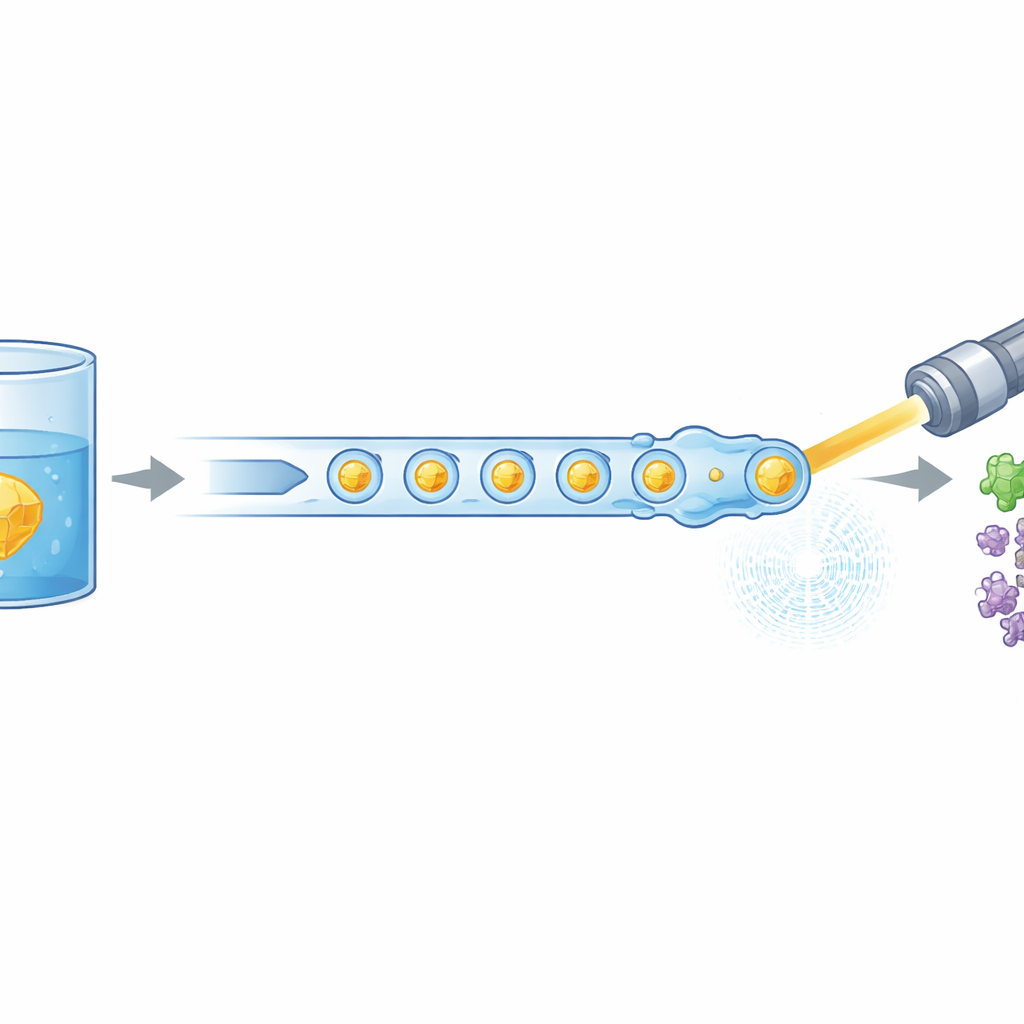
Por qué hacer películas moleculares resulta tan costoso
Para entender cómo realizan realmente su trabajo las proteínas, los científicos recurren cada vez más a “películas” en tiempo real en lugar de instantáneas estáticas. Un enfoque puntero, la cristalografía serial resuelta en el tiempo, pulveriza millones de cristales microscópicos de una proteína frente a un haz de rayos X ultraintenso. Cada cristal recibe un solo pulso, proporcionando una visión libre de daños de la estructura, y miles de esas imágenes se combinan para obtener una imagen completa. El problema es que cada instante a lo largo de una reacción—décimas de segundo, segundos completos, etc.—requiere un nuevo lote de cristales. Dado que la preparación de proteínas puede ser lenta y cara, el consumo de muestra se ha convertido en un cuello de botella importante, especialmente en instalaciones de vanguardia como el European XFEL, donde los pulsos de rayos X llegan en trenes rápidos a frecuencias de megahercios.
Una nueva forma de dispensar pequeñas gotas a tiempo
Los investigadores abordaron este problema rediseñando cómo se entregan los cristales al haz de rayos X. En lugar de un flujo líquido continuo, generan un tren cuidadosamente espaciado de gotas microscópicas, cada una conteniendo cristales de proteína, separadas por una fase oleosa. Un dispositivo miniatura impreso en 3D combina dos corrientes—cristales de proteína y un reactivo disuelto—en volúmenes mezclados diminutos, que luego se separan en gotas. Estas gotas se guían a través de una boquilla enfocada por gas que forma un chorro estrecho compatible con el vacío y la velocidad del XFEL. De manera crucial, la producción de gotas se sincroniza eléctricamente con el tiempo de los trenes de pulsos de rayos X para que casi cada pulso útil golpee una gota, en lugar de líquido vacío. 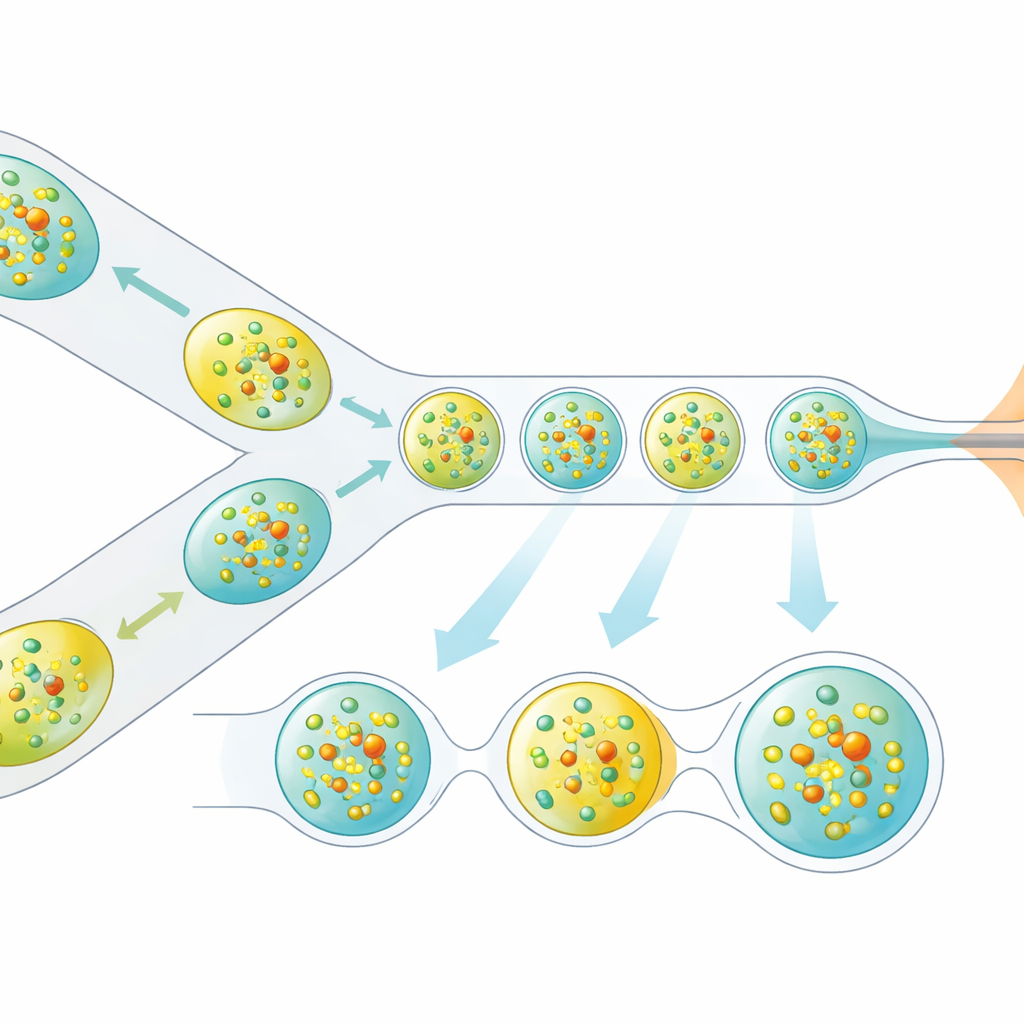
Poner el método a prueba con una enzima humana
Para demostrar que este enfoque basado en gotas funciona para preguntas biológicas reales, el equipo estudió la NAD(P)H:quinona oxidorreductasa 1 (NQO1), una enzima humana implicada en el equilibrio redox celular y asociada a enfermedades. Mezclaron microcristales de NQO1 con su cofactor natural, NADH, y sondearon el sistema en dos tiempos tempranos: 0,3 segundos y 1,2 segundos tras la mezcla. Al examinar los patrones de difracción de rayos X resultantes, reconstruyeron estructuras tridimensionales de la enzima en cada retraso. A pesar de usar mucha menos proteína que en experimentos convencionales de flujo continuo, la calidad de los datos fue suficiente para revelar sutiles características de densidad electrónica en los sitios activos de la enzima, coherentes con moléculas de NADH comenzando a unirse con baja ocupación.
Lo que revelan las primeras instantáneas estructurales
Las estructuras muestran que poco después de la mezcla no todos los sitios activos en el cristal se comportan igual. A 0,3 segundos, aparecen claramente señales de NADH en tres de los cuatro sitios activos de la celda unitaria, y a menudo en más de una conformación, lo que sugiere que el cofactor explora varias posiciones antes de asentarse. A 1,2 segundos, algunas de estas características se afinan hacia un modo de unión dominante, pero la imagen general sigue siendo la de una interacción flexible y solo parcialmente ocupada. Este comportamiento desigual y cambiante concuerda con evidencias bioquímicas anteriores de que las dos unidades compañeras en un dímero de NQO1 no actúan al unísono perfecto, sino que muestran actividad de “medio sitio”, donde un lado del par se involucra primero mientras el otro se retrasa. Los datos resueltos en el tiempo ofrecen así una temprana visión estructural de cómo se manifiesta esta asimetría en el espacio real.
Ahorrar muestra manteniendo la ciencia
Desde un punto de vista práctico, el método segmentado de gotas redujo el uso de proteína aproximadamente seis veces para las mediciones de 0,3 segundos y hasta un 97% para los experimentos de 1,2 segundos, en comparación con chorros continuos tradicionales en condiciones similares. Aun así, proporcionó información estructural fiable a temperatura ambiente, compatible con la exigente estructura de pulsos del European XFEL. Para no especialistas, la conclusión es que los investigadores pueden ahora observar cómo enzimas como NQO1 comienzan su trabajo en casi tiempo real, usando solo miligramos de muestra preciosa por punto temporal. Esto hace mucho más realista el estudio de muchos tiempos de reacción y de muchas proteínas diferentes, ayudando en última instancia a revelar cómo las enzimas de interés médico se mueven, se flexionan y cooperan al llevar a cabo la química de la vida.
Cita: Doppler, D., Grieco, A., Koh, D. et al. Minimized sample consumption for time-resolved serial crystallography applied to the redox cycle of human NQO1. Commun Chem 9, 107 (2026). https://doi.org/10.1038/s42004-026-01908-9
Palabras clave: cristalografía serial, láser de electrones libres de rayos X, microfluidos en gotas, dinámica enzimática, NQO1