Clear Sky Science · es
Las variantes oncogénicas de PI3Kα revelan un espectro conformacional gradual con bolsillos crípticos específicos de la mutación
Cuando un solo cambio en el ADN no basta
El cáncer se describe a menudo como una enfermedad de mutaciones, pero este estudio muestra que no todas las mutaciones actúan de forma aislada. Los investigadores examinaron una enzima clave del control del crecimiento, PI3Kα, y encontraron que cuando dos cambios específicos en el ADN ocurren juntos en la misma copia de su gen, pueden empujar a esta proteína hacia conformaciones más activas que cualquiera de los cambios por sí solo. Esto importa porque la PI3Kα hiperactiva no solo impulsa cánceres, sino que también está implicada en síndromes benignos de sobrecrecimiento y en trastornos del desarrollo cerebral, y ayuda a explicar por qué algunos tumores responden mal a los fármacos actuales.
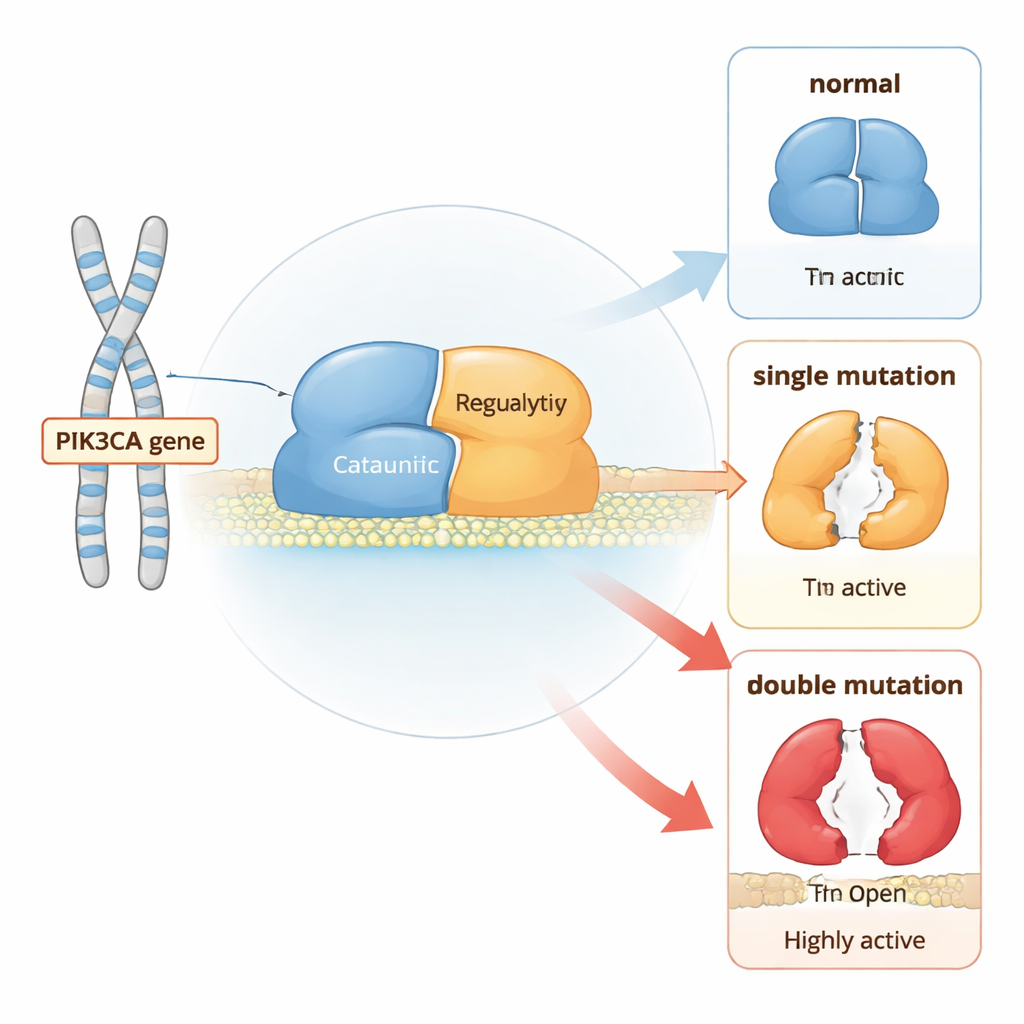
Un interruptor molecular para el crecimiento celular
La PI3Kα es una proteína de dos partes que se sitúa cerca de la membrana celular y transmite señales de crecimiento. En condiciones normales, permanece mayormente en una posición de “apagado” hasta que los receptores en la superficie celular se activan. Entonces, la PI3Kα se desplaza a la membrana y convierte un lípido llamado PIP2 en PIP3, que indica a la célula que crezca y se divida. Para impedir un crecimiento descontrolado, varias regiones de la proteína actúan como frenos incorporados: una región sujeta el núcleo catalítico, otra mantiene cerca un lazo de activación flexible, y una subunidad compañera ayuda a mantener todo el complejo bajo control.
Cómo las mutaciones simples y dobles inclinan el equilibrio
Utilizando simulaciones computacionales de larga duración a nivel atómico, los autores compararon la PI3Kα normal con versiones que portan ya sea mutaciones cancerígenas “punto caliente” simples o combinaciones de un punto caliente con una mutación más débil en la misma molécula. Encontraron que cada mutación altera la frecuencia con la que la proteína visita conformaciones más abiertas y activas, pero los dobles mutantes desplazan el equilibrio mucho más que los simples. En particular, algunos pares de mutaciones actúan en conjunto para aflojar los contactos que mantienen en su lugar a una pieza reguladora (llamada nSH2) y para desplazar otro segmento (iSH2) alejándolo de su sitio de acoplamiento. Este movimiento coordinado desencierra el núcleo catalítico, facilitando que la proteína se desplace a la membrana e inicie la señalización.
Ayudando al sustrato a alcanzar el sitio de reacción
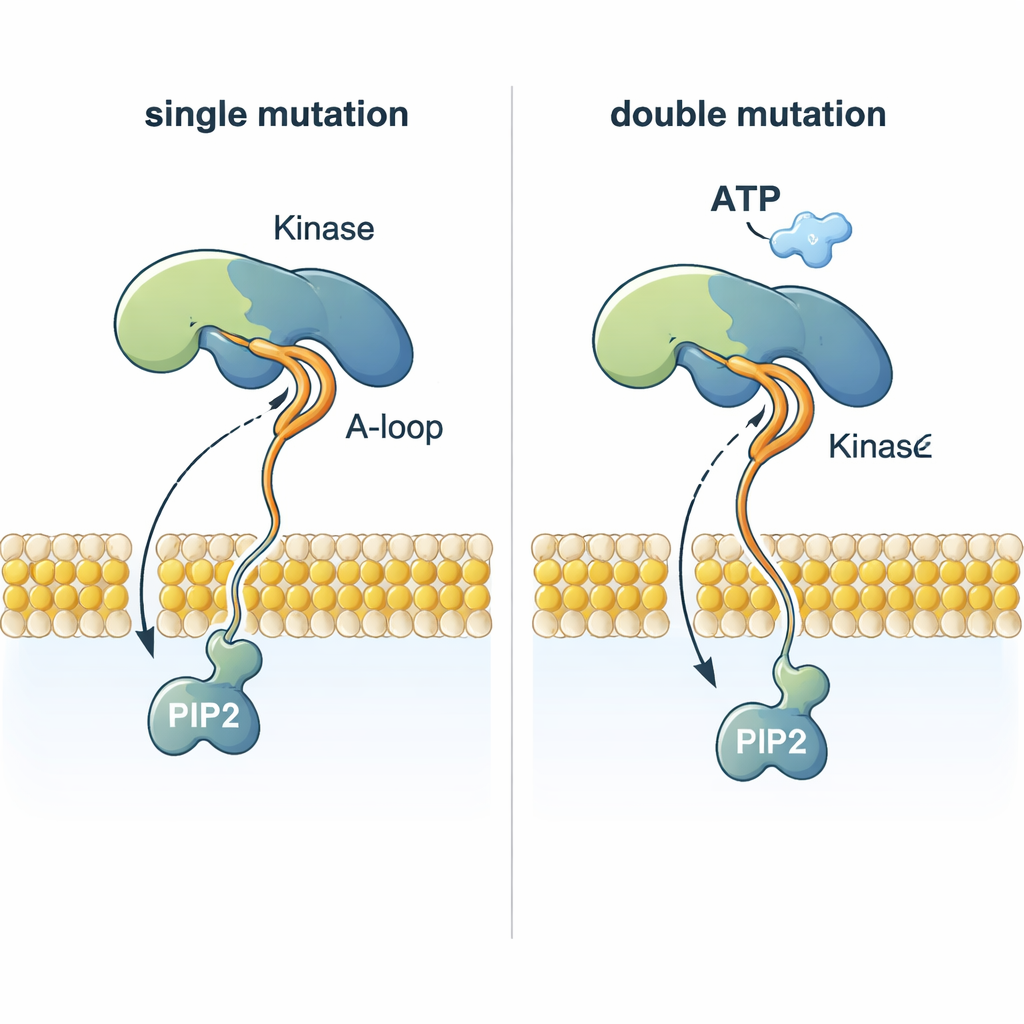
Un enigma llamativo es cómo la PI3Kα puede transferir un grupo fosfato desde el ATP —que está casi a 2 nanómetros por encima de la membrana— al PIP2, que está incrustado en la membrana. Las simulaciones muestran que ciertas mutaciones remodelan un lazo de activación flexible de modo que un tramo altamente cargado positivamente se proyecta hacia la membrana. Este lazo puede atrapar la cabeza cargada negativamente del PIP2, sacarla de la capa lipídica y guiarla hacia el ATP. Los dobles mutantes que combinan una mutación que ancla a la membrana con otra que modifica este lazo coordinan el PIP2 con mucha más eficiencia que la PI3Kα normal o los mutantes simples, ofreciendo una explicación estructural de por qué los tumores con dos mutaciones en PI3Kα pueden ser especialmente agresivos.
Sitios ocultos para fármacos revelados por el movimiento
Puesto que la PI3Kα es grande y flexible, un fármaco único dirigido a su sitio activo a menudo tiene dificultades para funcionar contra todas las formas mutantes y puede causar efectos secundarios como alteraciones graves del azúcar en sangre. Al rastrear cómo la proteína respira y se flexiona con el tiempo, los investigadores descubrieron bolsillos “crípticos”: hendiduras temporales que se abren solo en ciertas conformaciones mutantes y son invisibles en estructuras cristalinas estáticas. Estos bolsillos aparecen en ubicaciones específicas de la mutación, por ejemplo cerca de regiones que se mueven con mayor intensidad en dobles mutantes particulares. Eso sugiere que fármacos alostéricos diseñados con cuidado, que se unan lejos del sitio activo, podrían personalizarse para bloquear variantes mutantes individuales en conformaciones más seguras y menos activas.
Hacia tratamientos combinados más inteligentes
En conjunto, el trabajo apoya una visión de “golpe doble” de la genética del cáncer: una mutación fuerte en un punto caliente más un compañero más débil en la misma molécula de PI3Kα pueden crear un espectro gradual de conformaciones más activas, a menudo vinculadas a resultados clínicos más graves. Para la terapia, los autores sostienen que en lugar de depender de un solo inhibidor, puede ser más eficaz combinar fármacos que apunten a distintos bolsillos—uno en el sitio activo y uno o varios sitios alostéricos que existen solo en mutantes específicos. Tales cócteles podrían, en principio, reducir la actividad de la PI3Kα con mayor precisión, disminuir los efectos tóxicos y ajustar mejor el tratamiento al patrón exacto de mutaciones presente en el tumor de un paciente.
Cita: Jang, H., Yavuz, B.R., Zhang, M. et al. Oncogenic PI3Kα variants reveal graded conformational spectrum with mutation-specific cryptic pockets. Commun Chem 9, 100 (2026). https://doi.org/10.1038/s42004-026-01906-x
Palabras clave: PI3K alfa, mutaciones oncogénicas, inhibidores alostéricos, dinámica molecular, transducción de señales