Clear Sky Science · es
Dinámica dependiente de la secuencia y de la escala de longitud en biocondensados de proteínas desordenadas altamente cargadas
Por qué importan las diminutas gotas de proteína
Dentro de nuestras células, muchas reacciones vitales ocurren en estructuras blandas parecidas a gotas que carecen de membrana. Estos “condensados biomoleculares” se comportan como pequeños compartimentos líquidos y con frecuencia están formados por proteínas flexibles y muy cargadas. Experimentos han mostrado que las moléculas dentro de algunas de estas gotas pueden moverse sorprendentemente rápido, aunque las gotas en su conjunto sean bastante densas y pegajosas. Este trabajo plantea una pregunta simple pero importante: ¿cómo controla el orden exacto de cargas positivas y negativas a lo largo de estas proteínas la rapidez con la que se mueve la materia dentro de tales gotas?
Construyendo gotas a partir de cadenas flexibles y cargadas
Los autores se centran en proteínas intrínsecamente desordenadas —cadenas largas y flexibles que no se pliegan en formas rígidas. Muchas de estas cadenas llevan tanto cargas positivas como negativas, dispuestas en distintos patrones a lo largo de su longitud. Mediante simulaciones por ordenador a gran escala, el equipo creó gotas modelo formadas por muchas copias de dichas proteínas, junto con agua e iones pequeños, para imitar el interior abarrotado de condensados reales. Cambiaron de forma sistemática cuán “agrupado” estaba el patrón de cargas, desde secuencias donde las cargas positivas y negativas se alternan hasta secuencias en las que todas las cargas positivas están agrupadas y las negativas forman un bloque separado.
Contenido de agua y flujo ejercen influencia sobre el movimiento
Las simulaciones revelaron que estas gotas aún pueden comportarse como líquidos verdaderos con un contenido de agua muy alto—entre aproximadamente un 55% y un 84%, según el patrón de cargas. Esa cantidad de agua implica que el flujo del fluido, o hidrodinámica, no está completamente suprimido como sugerirían muchas teorías para soluciones poliméricas densas. Al rastrear cómo se desplazan con el tiempo los segmentos proteicos, los autores encontraron patrones de movimiento característicos de cadenas cuya movilidad está ayudada por el fluido circundante, en lugar de ser frenada únicamente por la fricción. Esta influencia hidrodinámica persiste hasta e incluso más allá de la escala de una cadena proteica completa, sobre todo en gotas formadas por secuencias con cargas más mezcladas y, por tanto, con más agua.
Los patrones locales de carga controlan la flexibilidad a microescala
Mirando más de cerca, los autores examinaron cómo se relajan y reordenan secciones cortas de cada cadena dentro de la gota. Diferentes porciones de la misma proteína, que contienen el mismo número de bloques básicos, podían moverse a ritmos muy distintos según su mezcla local de cargas positivas y negativas. Las secciones con carga más equilibrada se relajaban más rápidamente, mientras que tramos dominados por un tipo de carga se movían de forma más lenta. De manera sorprendente, estas diferencias se mantenían fuertes pese a que argumentos sencillos de apantallamiento predecirían que los efectos electrostáticos deberían ser de corto alcance en condiciones tan salinas y abarrotadas. El trabajo muestra que el hecho de que las cargas estén ligadas a lo largo de una cadena conserva correlaciones eléctricas de largo alcance que afectan con fuerza al movimiento local.
La viscosidad depende del tamaño de lo que se explora
El equipo preguntó entonces cuán “espesas” se sienten estas gotas a diferentes escalas de longitud. Usando un método que vincula pequeñas ondulaciones en el momento del fluido con su resistencia al flujo, calcularon una viscosidad que depende de la longitud de sondeo. Para todas las secuencias, el fluido parece más fluido cuando se lo sondea a escalas muy pequeñas y más viscoso cuando se lo sondea a través de toda la gota. Esta dependencia del tamaño es especialmente dramática para las secuencias con cargas agrupadas: para el patrón más segregado, la viscosidad a escala macroscópica supera en más de veinte veces la viscosidad local a nivel de monómero. En contraste, las gotas procedentes de secuencias bien mezcladas muestran una brecha mucho menor. En conjunto, la viscosidad a gran escala crece bruscamente con la concentración de proteínas, en línea con el comportamiento de soluciones densas de polímeros neutros, aun cuando las propias proteínas son altamente cargadas.
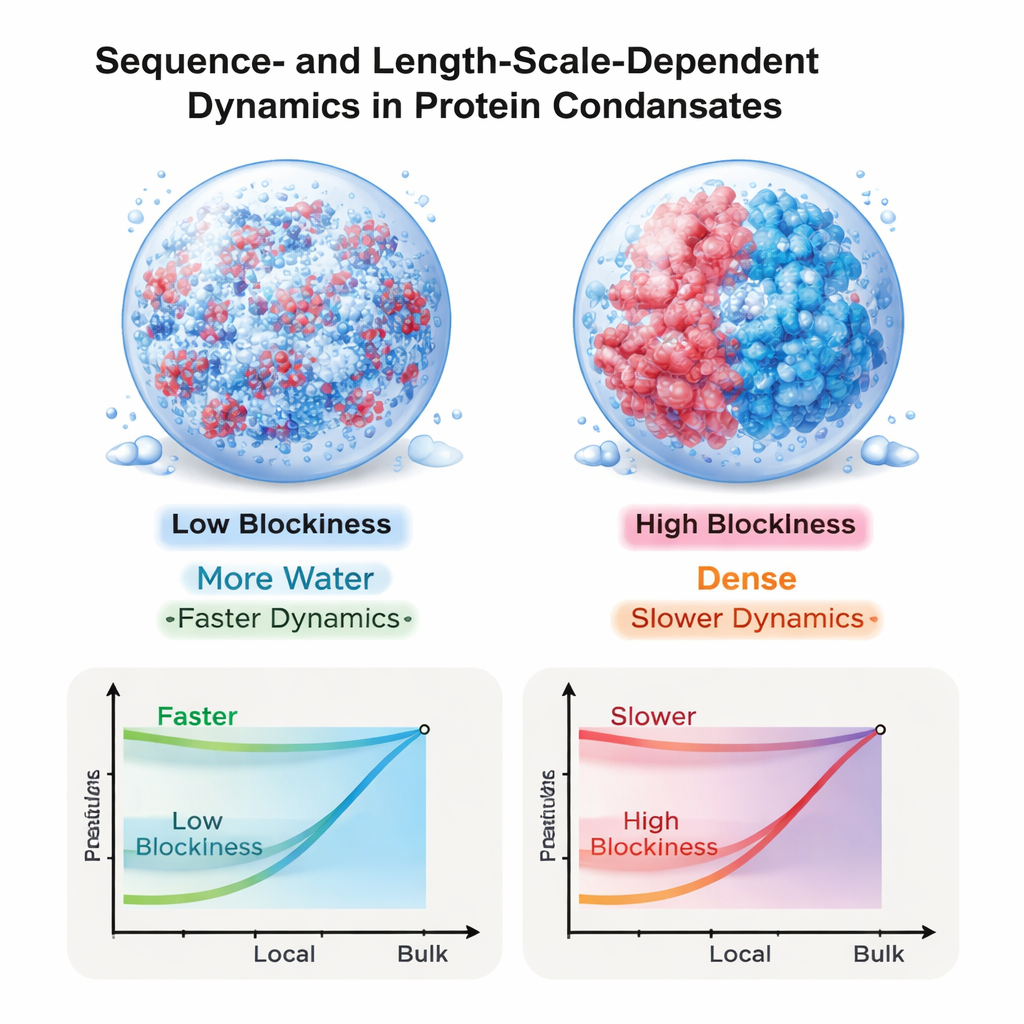
Conectando las simulaciones con experimentos desconcertantes
Estos resultados ayudan a resolver una aparente paradoja observada en experimentos recientes: ¿cómo pueden pequeñas moléculas y segmentos proteicos difundirse tan deprisa dentro de condensados que, medidos en su conjunto, parecen extremadamente viscosos? La respuesta que emerge de este trabajo es que tanto el flujo del agua como las interacciones eléctricas de largo alcance siguen siendo importantes en estas gotas, y su impacto está estrechamente controlado por cómo se ordenan las cargas a lo largo de cada cadena. Las secuencias con patrones de carga agrupada producen gotas densas y muy viscosas que, no obstante, siguen siendo relativamente fluidas a escalas microscópicas, mientras que las secuencias más mezcladas generan entornos de movilidad uniformemente mayor. Al demostrar que la secuencia de cargas puede ajustar el movimiento de forma distinta según la escala de longitud, el estudio ofrece un principio de diseño para ingeniería de materiales sintéticos a base de proteínas y arroja luz sobre cómo las células podrían programar el comportamiento de los condensados mediante la secuencia detallada de sus proteínas desordenadas.
Cita: Zhou, H., Wu, Z., Jiang, L. et al. Sequence and length-scale dependent dynamics in biocondensates of highly charged disordered proteins. Commun Chem 9, 98 (2026). https://doi.org/10.1038/s42004-026-01903-0
Palabras clave: condensados biomoleculares, proteínas intrínsecamente desordenadas, patronización de cargas, dinámica de proteínas, viscosidad