Clear Sky Science · es
Dinámica de la fotooxidación de CO a CO2 en rutilo (110)
Por qué importa observar moléculas en una billonésima de segundo
La vida moderna depende de reacciones químicas que limpian nuestro aire y agua y convierten la luz solar en energía utilizable. Muchas de estas reacciones ocurren en las superficies de materiales sólidos llamados fotocatalizadores, impulsados por la luz. Este estudio examina una de esas reacciones: cómo el venenoso monóxido de carbono (CO) se convierte en dióxido de carbono (CO2) sobre una superficie de dióxido de titanio, en escalas de tiempo de apenas cuatrillonésimas de segundo. Comprender estos pasos ultrarrápidos puede ayudar a los científicos a diseñar materiales más inteligentes para el control de la contaminación, superficies autolimpiantes y tecnologías de energía solar.
Un equipo de limpieza impulsado por la luz
El dióxido de titanio es un material todoterreno presente en ventanas autolimpiantes, recubrimientos purificadores de aire y dispositivos experimentales para combustibles solares. Es barato, estable y puede usar la luz para desencadenar reacciones de limpieza potentes en su superficie. Pero no todas las formas de dióxido de titanio se comportan igual. Dos formas comunes, llamadas anatasa y rutilo, difieren en la eficiencia con que impulsan reacciones como la conversión de CO en CO2. Aunque la anatasa suele ser más activa en general, el cronometraje detallado de los pasos individuales de la reacción—especialmente cómo se activa el oxígeno del aire—no estaba del todo claro. Este estudio se centra en la forma rutilo con una orientación superficial específica, conocida como (110), para ver exactamente qué tan rápido se oxida el CO una vez que la luz incide en el material.
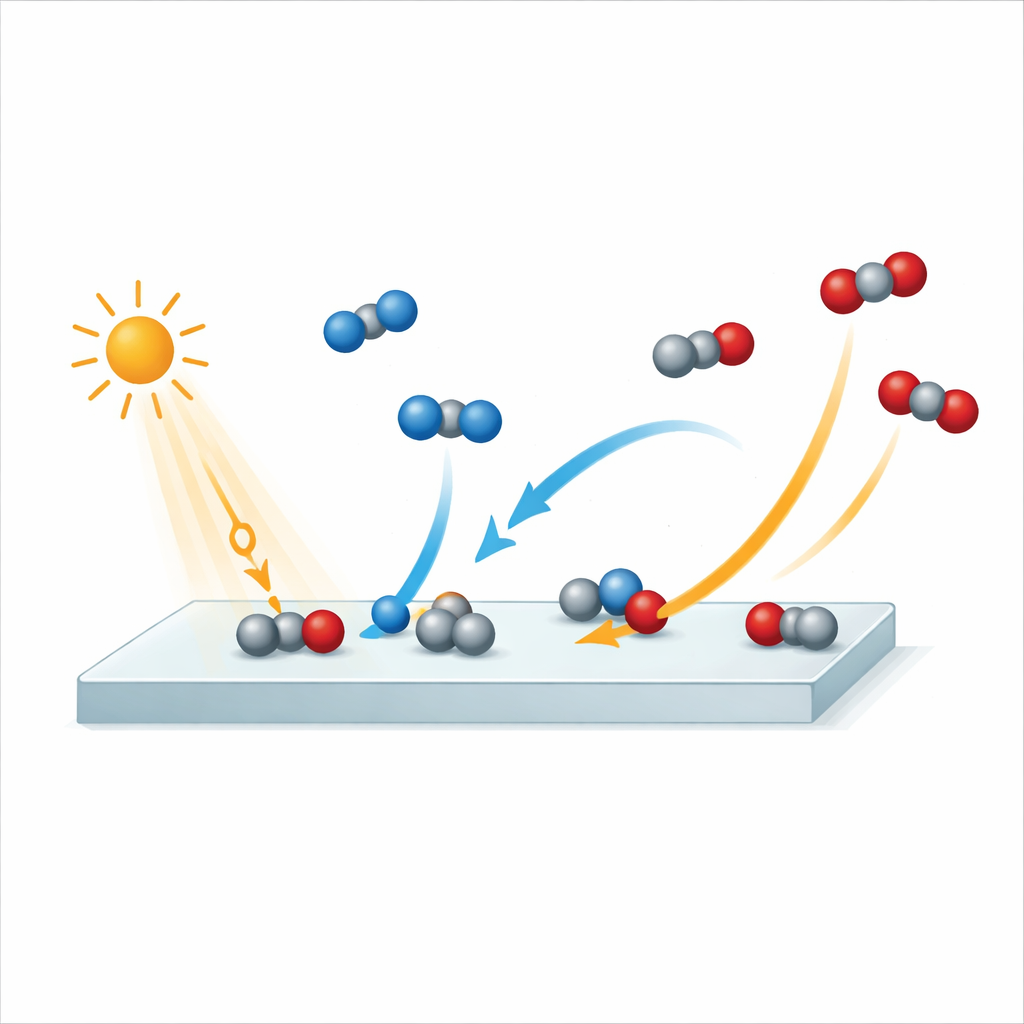
Filmando una reacción a velocidad extrema
Para capturar este proceso, los investigadores utilizaron una instalación con láser de electrones libres en Hamburgo que produce destellos extremadamente cortos de rayos X. Primero golpearon la superficie de rutilo con un pulso de luz infrarroja, que actuó como un diminuto flash de cámara que inicia la reacción. Un pulso de rayos X, cuidadosamente sincronizado, sondó cómo cambiaban los átomos y electrones en la superficie. Repitiendo esta secuencia con distintos retrasos entre los pulsos de luz y de rayos X, construyeron una especie de “película molecular” de la reacción con una resolución temporal de aproximadamente 250 femtosegundos—un femtosegundo es una millonésima de una milmillonésima de segundo. El equipo monitorizó señales de los átomos de oxígeno en la superficie y en las moléculas gaseosas, lo que les permitió distinguir entre CO, CO2, agua y el óxido mismo a medida que se desarrollaba la reacción.
Atrapar CO2 en menos de una billonésima de segundo
La observación clave es que aparece nuevo CO2 en la superficie de rutilo en tan solo 200 a 800 femtosegundos después del pulso de luz. Eso significa que el oxígeno de las moléculas O2 cercanas se activa, se rompen enlaces y el CO se convierte en CO2 en menos de una billonésima de segundo. Tras aproximadamente 0,8 picosegundos, la señal del CO2 recién formado se atenúa a medida que el producto se desorbe de la superficie. Sorprendentemente, toda esta secuencia ocurre más rápido en rutilo que en anatasa, donde trabajos anteriores encontraron el primer CO2 solo después de unos 1,2 a 2,8 picosegundos en condiciones comparables. Aunque la anatasa produce más CO2 en total y se considera el fotocatalizador más potente, el rutilo realiza el paso crucial de oxidación con más rapidez.
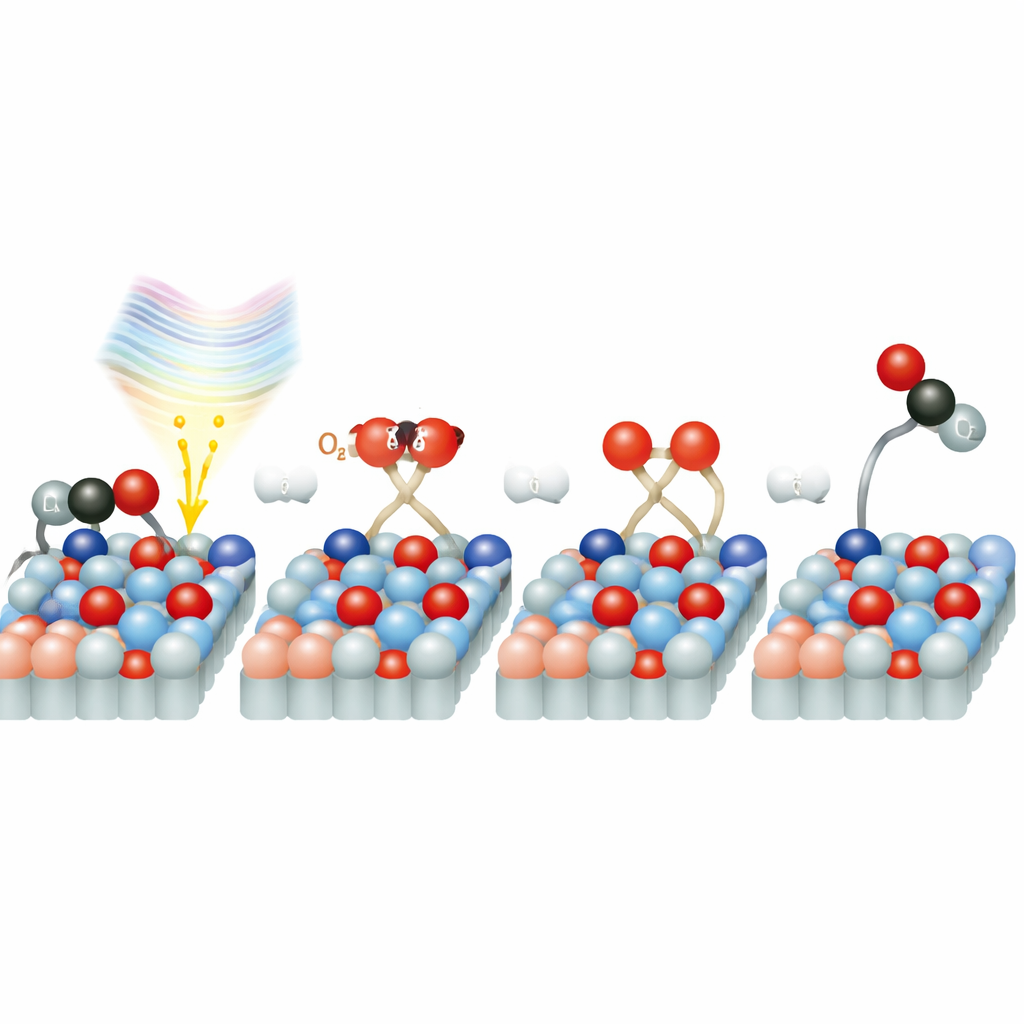
Una vía directa para el oxígeno
¿Por qué es tan rápida la reacción en rutilo? Simulaciones detalladas por ordenador sugieren que las moléculas de oxígeno adsorbidas en la superficie crean estados electrónicos especiales que actúan como un puente entre el sólido y el O2. Cuando se absorbe la luz láser de 770 nanómetros, puede moverse directamente un electrón desde el dióxido de titanio hacia la molécula de oxígeno, formando una especie de oxígeno cargada y activada. Este “atajo” evita la ruta más lenta en la que los electrones primero viajan por el volumen del sólido y luego se desplazan hacia la superficie. Una vez activado, el oxígeno se divide rápidamente y un átomo de oxígeno se combina con el CO para formar CO2. El estudio también encuentra que trazas de agua en la superficie pueden tanto bloquear sitios de reacción como, en niveles bajos, potencialmente ayudar en esta transferencia de carga y activación del oxígeno, añadiendo otra capa de complejidad.
Conectando la estructura electrónica con el rendimiento real
En conjunto, el trabajo muestra que pequeños detalles en cómo se mueven los electrones entre una superficie y las moléculas cercanas pueden cambiar dramáticamente las velocidades de reacción, incluso entre dos materiales estrechamente relacionados. Mientras que la anatasa sigue siendo superior en términos de rendimiento fotocatalítico total, el rutilo exhibe un paso de activación del oxígeno más rápido vinculado a esta ruta especial de transferencia de carga. Al combinar mediciones ultrarrápidas y simulaciones avanzadas, el estudio proporciona una hoja de ruta para diseñar superficies de modo que las reacciones desencadenadas por la luz ocurran con mayor eficiencia. A largo plazo, tales conocimientos podrían ayudar a los ingenieros a diseñar mejores recubrimientos para la purificación del aire, superficies antibacterianas más efectivas y materiales mejorados para la producción de combustibles solares y la división del agua.
Cita: Gleissner, H., Wagstaffe, M., Wenthaus, L. et al. Dynamics of CO photooxidation to CO2 on rutile (110). Commun Chem 9, 127 (2026). https://doi.org/10.1038/s42004-026-01901-2
Palabras clave: fotocatálisis, dióxido de titanio, espectroscopía ultrarrápida, química de superficies, oxidación de monóxido de carbono