Clear Sky Science · es
Desarrollo de un nanomodelo de puntos de carbono cuádruple-conjugados para la terapia dirigida del glioma
Nueva esperanza para tumores cerebrales resistentes
Los tumores cerebrales de alto grado, como el glioblastoma, están entre los cánceres más difíciles de tratar. Muchos fármacos que funcionan en otras partes del cuerpo no pueden cruzar la barrera hematoencefálica protectora o dañan el tejido sano en el proceso. Este estudio describe una nanopartícula “inteligente” diseñada en laboratorio que pretende infiltrarse con mayor precisión en los tumores cerebrales, transportar un cóctel farmacológico potente y liberarlo directamente dentro de los núcleos de las células tumorales, donde puede hacer el mayor daño al cáncer mientras preserva las células normales.
Un pequeño camión de reparto hecho de carbono
En el corazón del nuevo enfoque están los puntos de carbono: partículas a escala nanométrica hechas de carbono que son baratas de producir, se mezclan bien con el agua y brillan bajo ciertos tipos de luz. Debido a que sus superficies están llenas de ganchos químicos, pueden decorarse con múltiples componentes biológicos a la vez. En este trabajo, los investigadores crearon un nanomodelo “cuádruple-conjugado”: cada punto de carbono fue químicamente enlazado, en una única reacción en un solo recipiente, a dos péptidos diana distintos y a dos cargas anticancerígenas. Este diseño modular convierte cada punto en un pequeño camión de reparto capaz de reconocer células tumorales, atravesar barreras celulares y llevar fármacos a la dirección intracelular adecuada.
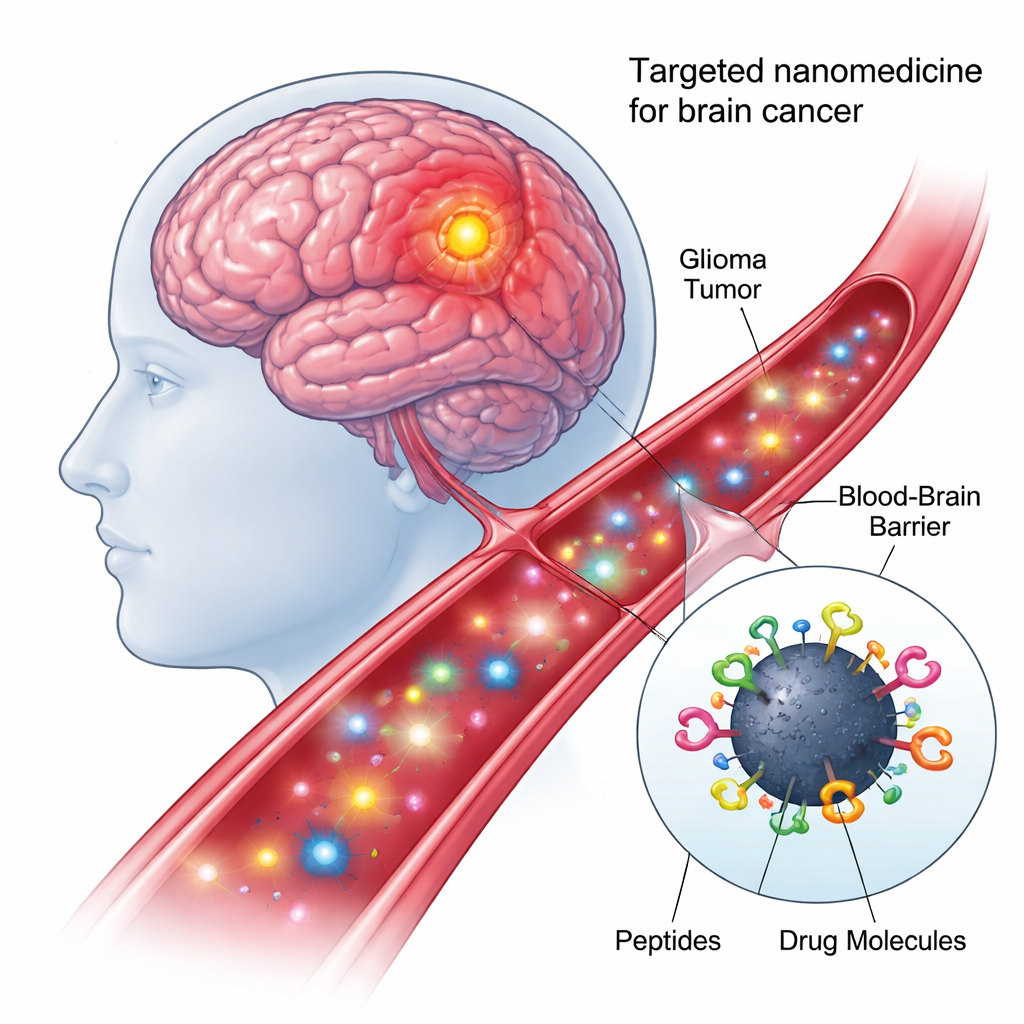
Encontrar y entrar en las células cerebrales correctas
El primer péptido en la nanopartícula, llamado shPep-1, está diseñado para reconocer un receptor denominado IL13Rα2. Este receptor se encuentra en niveles elevados en muchos tumores cerebrales agresivos—incluidos el glioblastoma en adultos y pediátrico y el glioma pontino intrínseco difuso—pero aparece débilmente en las células cerebrales normales. Al unirse a IL13Rα2, shPep-1 ayuda a los puntos de carbono a localizar las células tumorales y a entrar en ellas mediante captación mediada por receptor. El segundo péptido, más largo, lnPep-1, contiene una señal de localización nuclear: una corta secuencia que facilita que la carga cruce la membrana nuclear y alcance el centro de control de la célula, donde se almacena el ADN. Juntos, estos dos péptidos dan a la nanopartícula tanto preferencia por el tumor como la capacidad de alcanzar el núcleo una vez dentro.
Entregando un ataque farmacológico coordinado
La carga terapéutica consiste en dos pequeñas moléculas. La primera es epirrubicina, un fármaco quimioterapéutico bien conocido que mata células cancerosas al intercalarse en el ADN y bloquear enzimas necesarias para reparar roturas de doble cadena. La segunda es un metabolito llamado 5-aminoimidazol-4-carboxamida (AIC), producido a partir del fármaco para tumores cerebrales temozolomida a pH fisiológico. En trabajos anteriores, el mismo grupo mostró que combinar epirrubicina y AIC en un punto de carbono aumentaba la muerte de células cancerosas en comparación con cada fármaco por separado. En el nuevo diseño, ambos se coadministran en la nanopartícula de doble péptido, buscando un efecto sinérgico directamente en el núcleo de la célula tumoral.
Potente en células tumorales, más suave con las células normales
Para evaluar el rendimiento del nanomodelo, el equipo expuso varias líneas celulares de glioma de alto grado—glioblastoma adulto, glioblastoma pediátrico y un modelo de glioma pontino intrínseco difuso—a los puntos de carbono cuádruple-conjugados. Incluso a concentraciones muy bajas (tan solo 50 nanomoles), la viabilidad de las células tumorales cayó hasta alrededor de la mitad respecto a los controles no tratados, y a dosis más altas, todos los conjugados probados eliminaron la mayor parte de las células tumorales. De forma importante, el nanomodelo cuádruple superó a versiones más simples de “un solo péptido”, a pesar de llevar en total menos epirrubicina. Cuando se probó en células no cancerosas de músculo liso vascular, resultó mucho menos tóxico: estas células necesitaron aproximadamente entre 25 y 40 veces más nanopartícula para mostrar una pérdida de viabilidad similar, lo que sugiere una ventana de seguridad útil impulsada por la orientación al tumor en lugar de por dosis masivas.
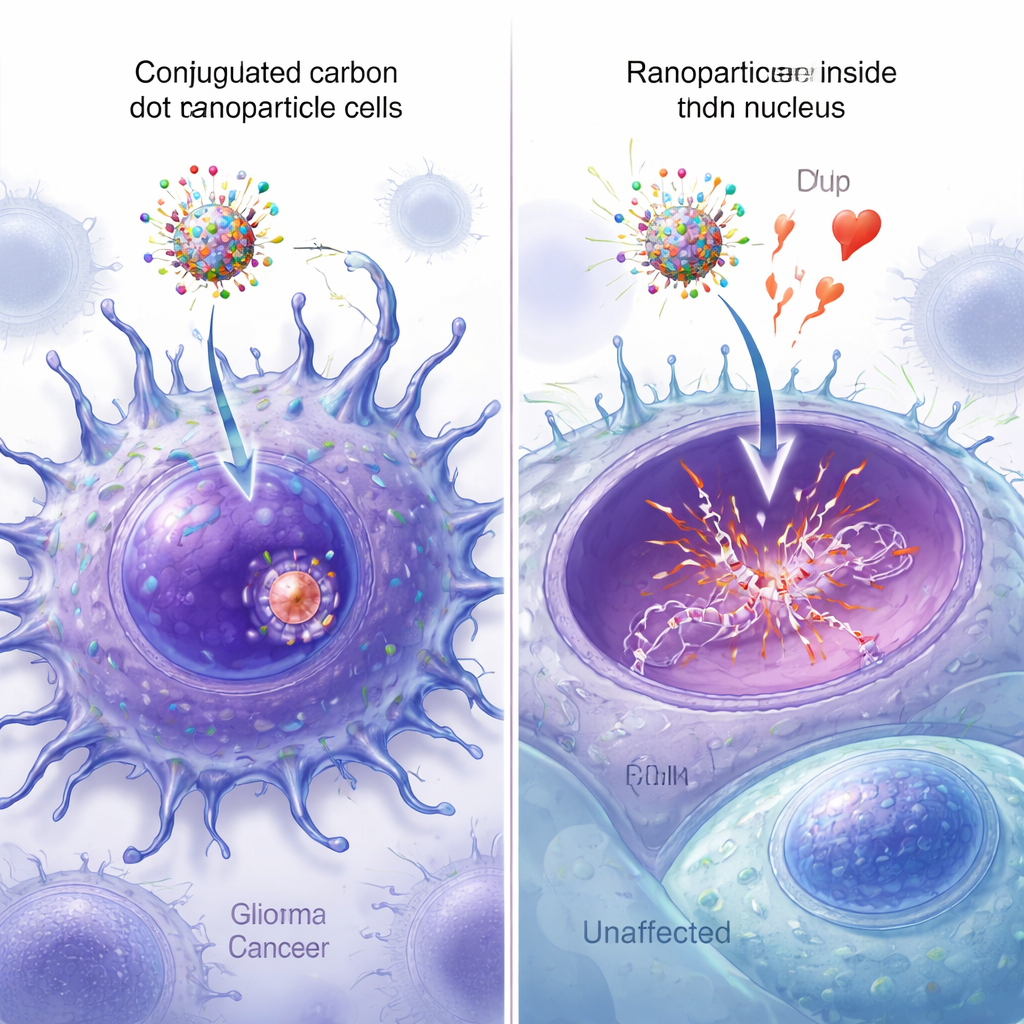
Ver que las nanopartículas alcanzan el núcleo
Versiones fluorescentes de las nanopartículas permitieron a los investigadores observar cómo cada diseño entraba en las células y alcanzaba el núcleo. Bajo el microscopio, los puntos de carbono equipados con ambos péptidos mostraron la señal más brillante repartida por las células cancerosas, con un fuerte solapamiento entre la fluorescencia verde de la nanopartícula y la tinción nuclear azul. El análisis cuantitativo de imágenes confirmó que las partículas de doble péptido tenían la mayor colocalización nuclear, superando significativamente a las partículas que llevaban solo un péptido o ninguno. Mediciones adicionales por espectroscopía, espectrometría de masas y microscopía de fuerza atómica verificaron que los cuatro componentes se unieron con éxito a los puntos de carbono y aumentaron modestamente su tamaño, sin alterar la función clave de unión al ADN de la epirrubicina.
Lo que esto podría significar para el futuro del tratamiento del cáncer cerebral
Para los pacientes, estos hallazgos siguen siendo una demostración en fase temprana en platos de cultivo y no una terapia lista para usar. Sin embargo, ponen de manifiesto un concepto prometedor: una nanopartícula pequeña, estable y relativamente fácil de fabricar, basada en carbono, que puede personalizarse rápidamente con péptidos diana y combinaciones de fármacos. Al dirigir los fármacos específicamente a las células tumorales que sobreproducen IL13Rα2 y concentrarlos en el núcleo, tales nanomedicinas podrían algún día permitir dosis más bajas, menos efectos secundarios y estrategias de tratamiento más personalizadas para tumores cerebrales altamente letales como el glioblastoma y el glioma pontino intrínseco difuso.
Cita: Cilingir, E.K., Hettiarachchi, S.D., Rathee, P. et al. Development of a quadruple-conjugated carbon dot nanomodel for targeted glioma therapy. Commun Chem 9, 96 (2026). https://doi.org/10.1038/s42004-026-01900-3
Palabras clave: glioblastoma, nanomedicina, puntos de carbono, administración dirigida de fármacos, tumores cerebrales