Clear Sky Science · es
Un ensayo generalizable para la acumulación intracelular para perfilar la entrega citosólica de fármacos en células de mamífero
Por qué importa que los fármacos entren en las células
Muchas de las medicinas más prometedoras de hoy —pequeñas moléculas, fragmentos proteicos cortos llamados péptidos y proteínas de tamaño completo— están diseñadas para actuar sobre dianas dentro de nuestras células. Pero la membrana celular es una barrera estricta. Un fármaco puede adherirse al exterior de una célula o quedar atrapado en sacos internos llamados endosomas y aun así no alcanzar el interior acuoso, el citosol, donde residen muchas dianas. Este artículo describe una nueva prueba de laboratorio, llamada ensayo CHAMP, que indica a los investigadores no solo si una molécula entra en la célula, sino si realmente llega al citosol, donde puede ejercer su función.
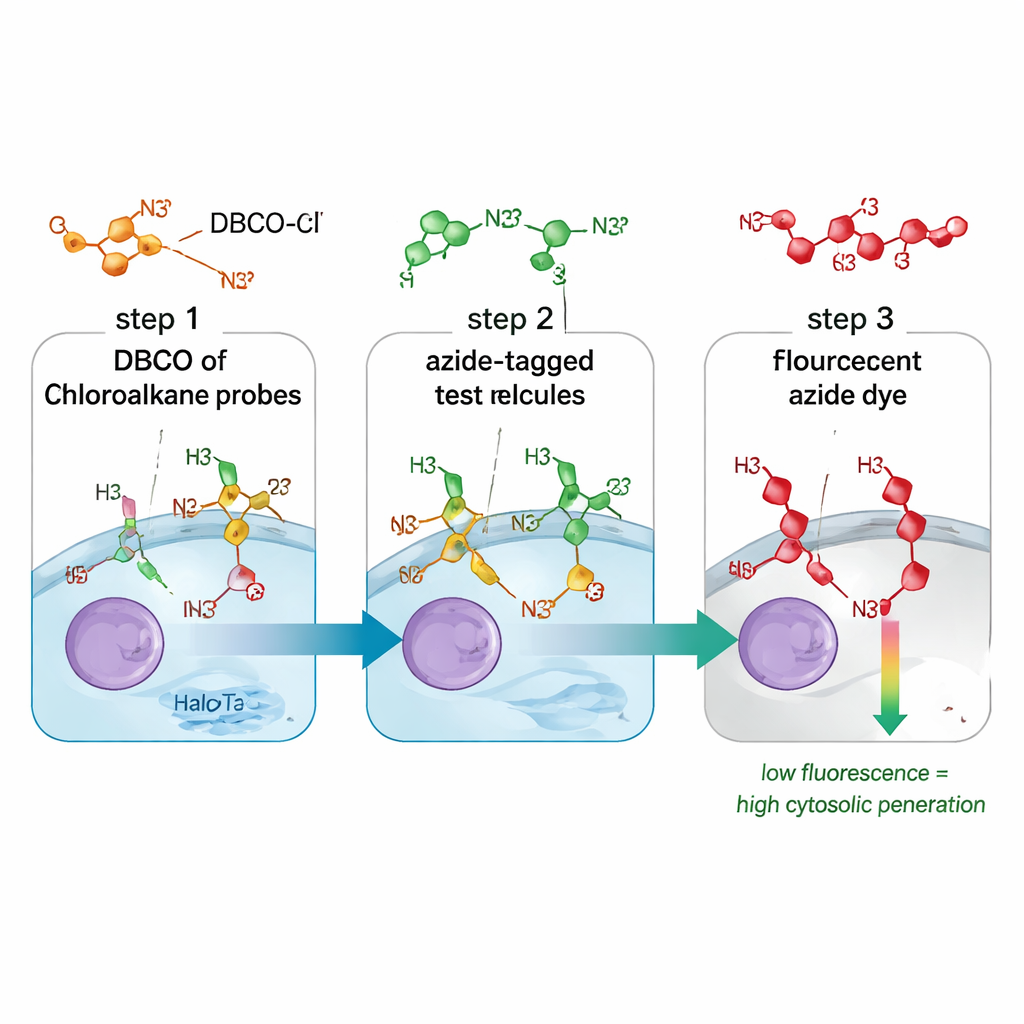
Una nueva forma de seguir la entrada de fármacos
Los métodos tradicionales para medir la captación de fármacos a menudo confunden moléculas que simplemente tocan la superficie celular, se sitúan en endosomas o alcanzan con éxito el citosol. También pueden depender de etiquetas fluorescentes voluminosas que alteran el comportamiento de la molécula. El ensayo CHAMP resuelve ambos problemas combinando un “mango” químico pequeño llamado azida con un marcador proteico denominado HaloTag, diseñado para flotar libremente en el citosol de células humanas en cultivo. Primero, se tratan las células con una molécula conectora que coloca DBCO, una forma tensada de alquino, sobre HaloTag. A continuación, los científicos añaden el compuesto de prueba, que lleva la pequeña etiqueta azida. Solo si ese compuesto cruza la membrana celular hasta el citosol podrán la azida y el DBCO reaccionar entre sí en una reacción química altamente selectiva. Una tintura fluorescente azida final revela cuántos sitios DBCO quedan: células tenues indican que el compuesto de prueba entró y ocupó la mayoría de los sitios; células brillantes indican un acceso citosólico deficiente.
Del concepto al ensayo funcional
Los autores confirmaron primero que HaloTag se producía correctamente y se localizaba en el citosol de células HeLa humanas usando un tinte estándar de cloroalquilo e imagen. Luego optimizaron cada paso de CHAMP: la cantidad de conector DBCO a añadir, el tiempo de incubación y qué tinte fluorescente azida daba una señal fuerte y específica sin dañar las células. La citometría de flujo —un instrumento que mide la fluorescencia en miles de células individuales— mostró que el ensayo era rápido, robusto y modulable. De forma crucial, el equipo demostró que la fluorescencia procedía realmente de reacciones específicas en los sitios de HaloTag y no de tintes que se adhirieran de forma inespecífica a componentes celulares, y que la pequeña etiqueta azida no alteraba de forma apreciable cómo las moléculas entraban en las células.
Lo que el ensayo revela sobre fármacos pequeños y péptidos
Con CHAMP disponible, los investigadores lo pusieron a prueba con cientos de pequeñas moléculas etiquetadas con azida y variaron sistemáticamente características como la carga, el tamaño y la flexibilidad. Observaron, por ejemplo, que convertir un ácido carboxílico cargado negativamente en una amida neutra aumentaba la acumulación citosólica, y que el grado y la posición de la N‑metilación del nitrógeno cambiaban la eficacia con la que los compuestos penetraban. Al comparar reacciones en perlas libres frente a células vivas, pudieron separar la reactividad química intrínseca de la barrera impuesta por la membrana. El equipo también aplicó CHAMP a un panel de antibióticos comunes, mostrando que algunos alcanzaban el citosol mucho mejor que otros —información importante al tratar bacterias que se ocultan dentro de células hospedadoras.
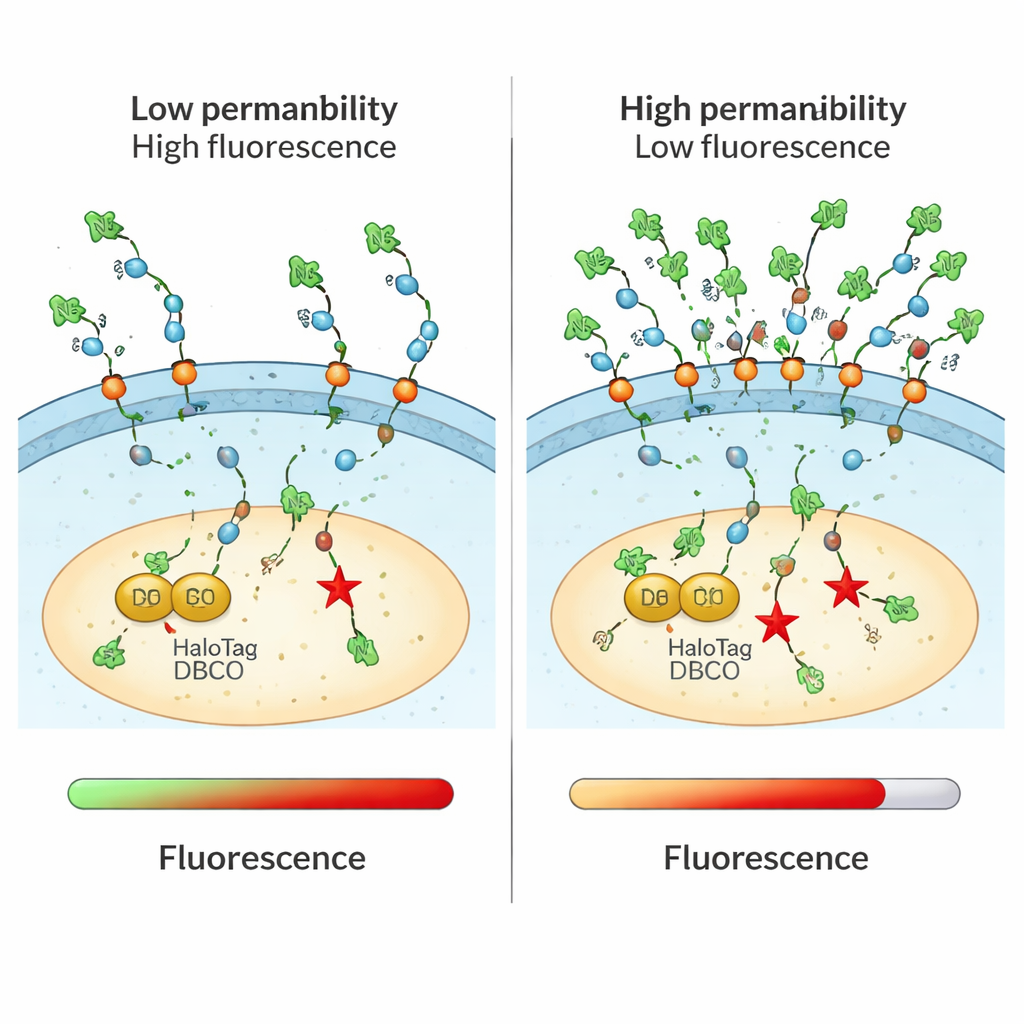
Péptidos y proteínas supercargados cruzando la barrera
El ensayo resultó especialmente potente para estudiar moléculas mayores y altamente cargadas que son difíciles de rastrear por otros métodos. Los autores examinaron péptidos penetrantes de células compuestos por múltiples residuos de arginina y confirmaron una tendencia clara: cadenas más largas y con más carga positiva entregaban más material al citosol, hasta cierto punto. Investigaron cómo invertir la quiralidad (estereoquímica) de ciertos aminoácidos alteraba la entrada, encontrando que las versiones en imagen espejo a veces se acumulaban mejor, lo que sugiere interacciones quirales sutiles con la membrana. CHAMP también mostró que las proteínas “supercargadas” —diseñadas para portar muchas cargas positivas— podían alcanzar el citosol con más eficacia que sus homólogas normales, respaldando su potencial como transportadores de cargas terapéuticas grandes.
Reglas de diseño para futuras medicinas intracelulares
Al probar sistemáticamente pequeñas moléculas, péptidos, péptidos macrocíclicos y esqueletos modificados, el estudio descubrió principios generales de diseño. Los péptidos macrocíclicos, cuyos esqueletos están cerrados en anillos, tendían a alcanzar el citosol con más facilidad que las versiones lineales y flexibles. Grupos N‑metilo colocados con cuidado en los esqueletos peptídicos aumentaban modestamente la entrada, pero un exceso podía ser contraproducente. Estas relaciones estructura–permeación, reveladas con un único ensayo estandarizado, ofrecen orientación práctica para los químicos que buscan diseñar moléculas que no solo se unan a sus dianas, sino que realmente puedan alcanzarlas dentro de las células.
Cómo ayuda esto al desarrollo de fármacos
En términos simples, el ensayo CHAMP es un contador de tráfico finamente ajustado en la puerta y los pasillos interiores de la célula. Indica a los científicos qué fármacos experimentales realmente superan la membrana y llegan al citosol, sin dejarse engañar por moléculas atrapadas en la superficie o en compartimentos internos. Dado que funciona con una amplia variedad de formas y tamaños moleculares y utiliza solo una pequeña etiqueta azida, CHAMP puede integrarse en pipelines de descubrimiento de alto rendimiento. Con el tiempo, esto debería acelerar el diseño de tratamientos más eficaces para enfermedades en las que las dianas más importantes están encerradas dentro de nuestras células.
Cita: Bhandari, S., Ongwae, G.M., Dash, R. et al. A generalizable assay for intracellular accumulation to profile cytosolic drug delivery in mammalian cells. Commun Chem 9, 94 (2026). https://doi.org/10.1038/s42004-026-01898-8
Palabras clave: entrega intracelular de fármacos, permeabilidad de la membrana celular, acumulación citosólica, péptidos penetrantes de células, química click bioortogonal