Clear Sky Science · es
Catalisis de DNAzima activada por superficies metálicas para la escisión eficiente del ADN
Metales que hacen que el ADN se corte a sí mismo
La mayoría de nosotros pensamos en el metal como algo sólido e inerte: útil para monedas, ollas y cableado, pero no para reacciones químicas en un vaso de agua. Este estudio desmonta esa intuición al mostrar que piezas desnudas de metal pueden activar diminutos catalizadores basados en ADN, llamados DNAzimas, con nada más que agua pura y aire. El trabajo revela una vía inesperada por la cual materiales cotidianos como el cobre y otros metales pueden impulsar reacciones de estilo biológico en sus superficies, insinuando nuevas herramientas para sensores, medicina e incluso química del origen de la vida. 
¿Qué son las tijeras de ADN?
Las DNAzimas son cortas cadenas de ADN que se pliegan en formas capaces de acelerar reacciones químicas específicas, de forma análoga a las enzimas proteicas. Muchas DNAzimas conocidas actúan como tijeras moleculares que cortan otras hebras de ADN o ARN, pero casi siempre necesitan iones metálicos disueltos—como cobre, zinc o magnesio—flotando en la solución para funcionar. Una de estas DNAzimas, llamada PL, es una hebra que se corta a sí misma y que normalmente depende de iones de cobre y ciertos auxiliares como la vitamina C o el peróxido de hidrógeno. Estos auxiliares participan en reacciones redox (transferencia de electrones) que generan especies reactivas de oxígeno de alta energía, que luego atacan y rompen la columna vertebral del ADN en posiciones precisas.
Cuando un alambre de cobre se convierte en cofactor
Mientras exploraban un montaje electroquímico para controlar la actividad de PL, los investigadores observaron algo sorprendente: simplemente sumergir un alambre de cobre desnudo en una solución que contenía PL y agua destilada condujo a un corte eficiente del ADN, incluso sin añadir iones de cobre, tampones o sales. La superficie de cobre por sí sola igualó o superó a las mezclas tradicionales de iones de cobre más vitamina C o peróxido de hidrógeno, y cortó el ADN exactamente en el mismo sitio. Pruebas posteriores mostraron que muchos objetos de cobre—láminas, embudos, ollas e incluso monedas de distintas divisas—podían provocar la escisión por PL, con la extensión de la reacción dependiente de cuánto área superficial metálica contactaba la gota. El cobre recién pulido funcionó algo peor que el cobre envejecido y oxidado, lo que sugiere que una delgada capa formada por la exposición al aire podría, en realidad, favorecer la reacción.
Qué superficies funcionan—y por qué
Para comprobar si esto era una curiosidad exclusiva del cobre, el equipo examinó 24 metales y 10 materiales no metálicos. Encontraron que solo ciertos metales, como cobre, tántalo y vanadio, activaban fuertemente a PL, mientras que el vidrio, el plástico, la madera y otros no metales no hacían nada. Las mediciones mostraron que pequeñas cantidades de iones metálicos se lixivian al agua desde las superficies activas, pero esos iones por sí solos eran demasiado débiles para explicar la intensa escisión del ADN. El ingrediente que faltaba resultó ser oxígeno reactivo derivado del aire disuelto. Usando captadores químicos y enzimas, los autores demostraron que el superóxido—una forma energética de oxígeno con un electrón extra—es esencial. Cuando se eliminó el oxígeno disuelto burbujeando nitrógeno, la actividad de PL casi desapareció; permitir la entrada de oxígeno restauró el corte. En conjunto, los datos apoyan un ciclo en el que la superficie metálica y sus iones lixiviados convierten el oxígeno disuelto en superóxido y peróxido de hidrógeno justo en la interfaz sólido–líquido, y estas especies luego impulsan la escisión del ADN. 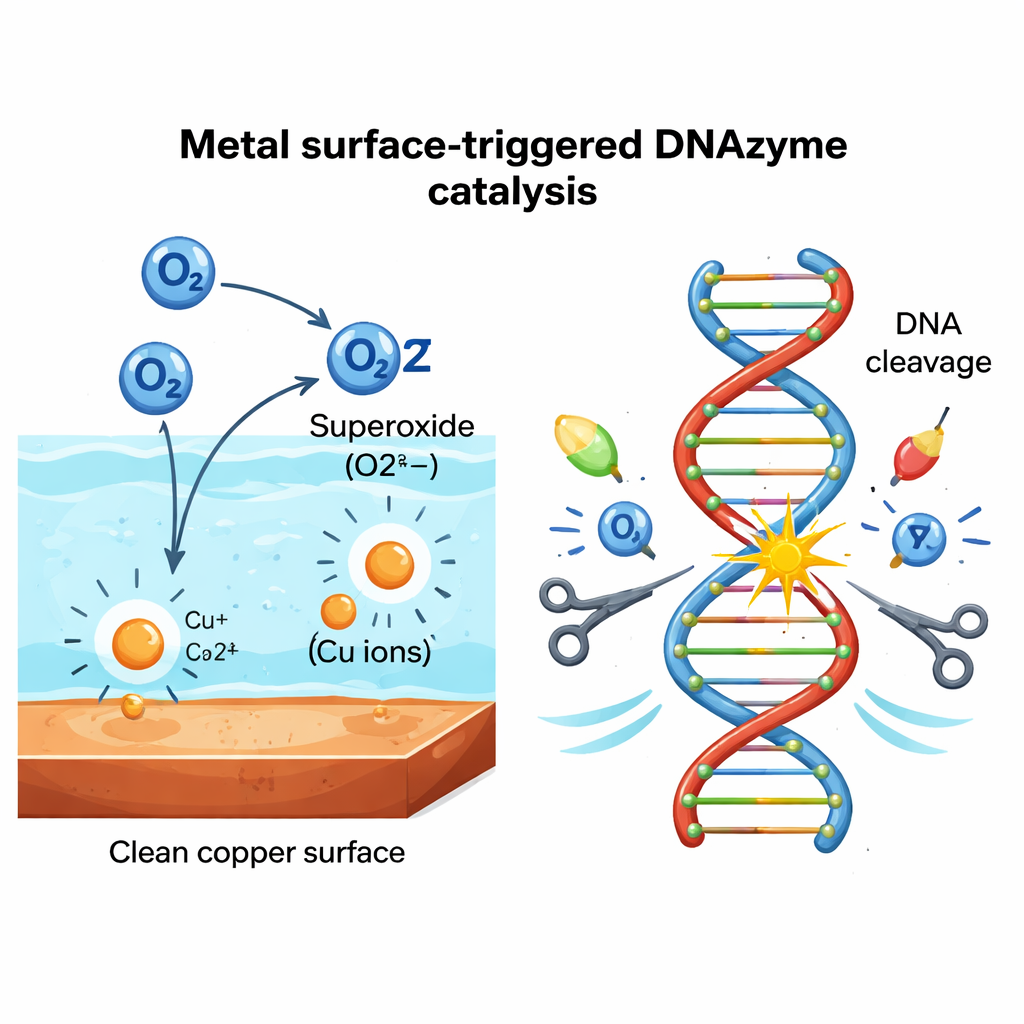
Auxiliares, bloqueadores y otras DNAzimas
La química desencadenada por la superficie pudo modularese usando moléculas conocidas. Quelantes como el EDTA, que secuestran iones metálicos, ralentizaron la reacción. La catalasa, una enzima que descompone el peróxido de hidrógeno, y tintes que absorben superóxido también redujeron el corte del ADN, confirmando el papel de estas especies reactivas de oxígeno. En contraste, compuestos pequeños como la vitamina C, el glutatión y la catecol aumentaron la actividad al alimentar el ciclo redox que produce superóxido cerca de la superficie metálica. De manera notable, el efecto no fue exclusivo de PL: otras DNAzimas que cortan ADN o ARN, incluidas F-8, Ag10c e I-R3, también se activaron por los metales a granel correspondientes (por ejemplo, plata metálica para una DNAzima dependiente de Ag y zinc metálico para una dependiente de Zn). Esto sugiere que la catálisis de ADN “activada por superficie metálica” podría ser un fenómeno amplio más que una rareza aislada.
Por qué esto importa fuera del laboratorio
Para lectores ajenos a la química, el mensaje central es que las superficies metálicas sólidas pueden actuar como socios químicos invisibles para catalizadores basados en ADN, usando solo aire y agua para generar las especies reactivas necesarias para cortar el ADN. En lugar de disolver cantidades precisas de iones metálicos, uno puede simplemente poner en contacto una superficie metálica adecuada con una solución de ADN y dejar que la interfaz haga el trabajo. Esto abre posibilidades para sensores de bajo coste que detecten objetos metálicos, herramientas para monitorear o eliminar radicales de oxígeno dañinos en células, y nuevas maneras de estudiar cómo podrían ocurrir reacciones semejantes a las de la vida en superficies minerales o metálicas. En resumen, tu moneda de cobre no es solo dinero suelto: también puede ser una pequeña fábrica química para tijeras de ADN.
Cita: Jiang, F., Dong, Y., Yu, W. et al. Metal surface-triggered DNAzyme catalysis for efficient DNA cleavage. Commun Chem 9, 91 (2026). https://doi.org/10.1038/s42004-026-01893-z
Palabras clave: DNAzima, catálisis en superficie metálica, especies reactivas de oxígeno, química en la interfaz de cobre, escisión de ADN