Clear Sky Science · es
Crecimiento esferulítico controlado de cristales a partir de mezclas salinas
Por qué los cristales de sal pueden parecer flores
La mayoría pensamos en los cristales como formas agudas y facetadas, pero en la naturaleza a menudo crecen en espectaculares esferas que recuerdan flores o bolas de nieve. Estas “esferulitas” aparecen en rocas volcánicas, cálculos renales e incluso en algunas enfermedades relacionadas con proteínas mal plegadas. Este artículo explora cómo un mineral cotidiano, el sulfato de sodio—la misma sal que se encuentra en detergentes y algunos materiales de construcción—puede inducirse a formar tales cristales esféricos intrincados, y qué revela esto sobre cómo estructuras complejas se autoensamblan a partir de ingredientes simples.
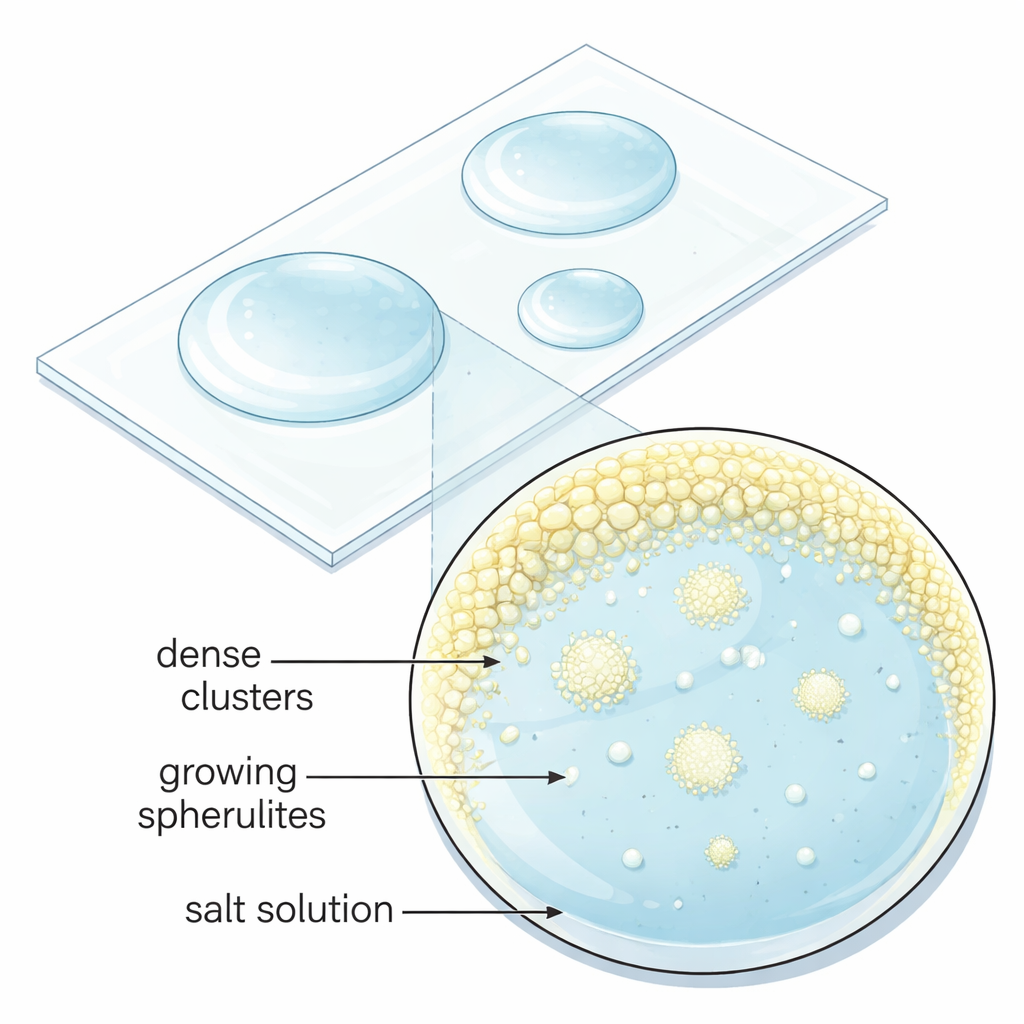
De sales simples a esferas esculpidas
Los investigadores se propusieron entender cuándo y cómo el sulfato de sodio crece en esferulitas en lugar de en cristales prismáticos ordinarios. Prepararon diminutas gotas de agua que contenían mezclas de sulfato de sodio y otras sales sulfato cuyos iones metálicos tienen carga doble, como magnesio o hierro. A medida que estas gotas—de picolitros a microlitros—evaporaban lentamente sobre portaobjetos de vidrio a temperatura ambiente, las sales disueltas se concentraban cada vez más hasta que comenzaron a formarse cristales. Variando sistemáticamente la proporción de mezcla, encontraron “puntos dulces” de composición donde el sulfato de sodio producía de forma consistente cristales esféricos con textura radial. Fuera de esos rangos, la misma solución daba lugar bien a granos facetados regulares o bien a un sólido gelatinoso sin rasgos, lo que demuestra que las formas esféricas requieren condiciones afinadas cuidadosamente.
Pequeños bolsillos líquidos que inician las esferas cristalinas
Bajo el microscopio, el equipo observó que las esferulitas no surgían directamente de una solución clara. En su lugar, la evaporación creó primero pequeños racimos líquidos densos enriquecidos en iones disueltos cerca del borde de la gota. Estos bolsillos de tamaño micrométrico persistían durante minutos antes de brotar repentinamente muchas esferulitas a la vez. Imágenes de alta resolución en microscopía electrónica de las estructuras secas revelaron que cada esferulita está construida a partir de innumerables cristales de sulfato de sodio a escala nanométrica apuntando aproximadamente hacia afuera, que posteriormente se fusionan. Este comportamiento contradice la imagen de libro de texto del crecimiento cristalino, donde un único núcleo estable crece de forma continua, y apunta en cambio a una vía de varios pasos “no clásica” en la que gotas densas y nanopartículas se ensamblan y reorganizan en su camino hacia la forma sólida final.
Cuando el agua salada adquiere consistencia de mantequilla de cacahuete
Una parte crucial de la historia es cuán espesa, o viscosa, se vuelve la solución a medida que se pierde agua. Al seguir la velocidad de expansión de las esferulitas y al medir directamente las propiedades de flujo de soluciones salinas relacionadas, los autores mostraron que las mezclas de sodio–magnesio o sodio–hierro se vuelven extraordinariamente viscosas—hasta unas 100 veces más espesas que la miel—justo cuando comienzan a formarse las esferulitas. Esta consistencia casi de “mantequilla de cacahuete” ralentiza tanto el movimiento de iones que la difusión, y no la química superficial, limita la velocidad de crecimiento de los cristales. En este entorno lento, se forman innumerables racimos y nanocristales que tienen tiempo de aglomerarse en agregados esféricos en lugar de crecer en unos pocos cristales grandes y bien formados. Los iones metálicos divalentes son clave: enlazan el agua con fuerza y se conectan en cadenas o redes cortas, lo que tanto eleva la viscosidad como contribuye a generar un fondo amorfo y tipo gel alrededor de las esferulitas en crecimiento.
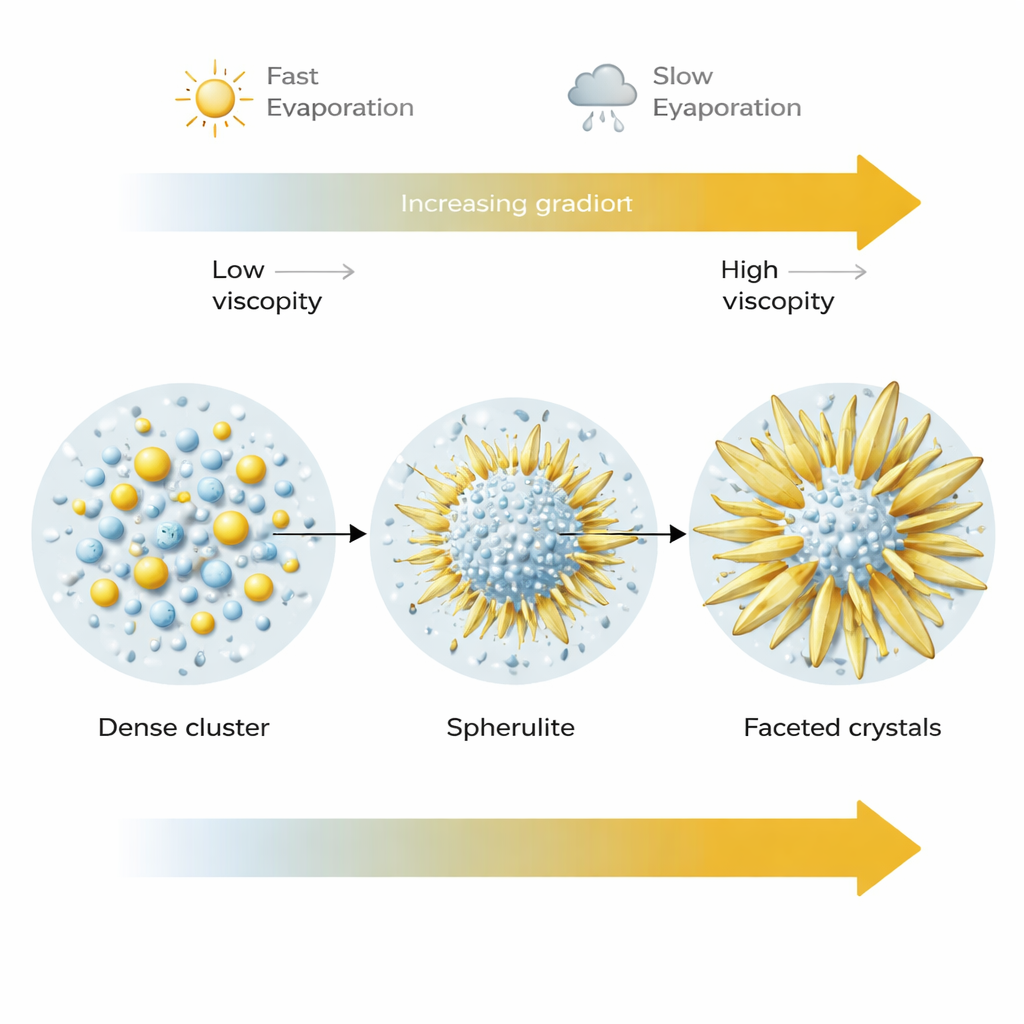
Cómo la velocidad de secado remodela los cristales finales
La velocidad de evaporación resultó ser otra perilla de control poderosa. A un secado más rápido (humedad baja), se nucleaban muchas esferulitas pero se mantenían relativamente pequeñas, atrapadas en su forma esférica metastable cuando el fluido circundante se espesaba con rapidez. A un secado más lento (humedad alta), las mismas esferas iniciales tenían más tiempo y acceso a iones disueltos. Sus pequeños bloques constructores podían reorganizarse y fusionarse en cristales más grandes, lisos y facetados, a menudo brotando apéndices en forma de cuchilla que finalmente se convertían en la forma termodinámicamente estable del sulfato de sodio. En otras palabras, las estructuras esféricas actúan como una etapa transitoria en un viaje de crecimiento que puede acabar en formas muy distintas, dependiendo de la rapidez con que se seque la solución y de lo fácilmente que el material pueda todavía moverse a través de ella.
Por qué esto importa más allá de los cristales bonitos
En términos sencillos, el estudio muestra que las esferas salinas bellas y semejantes a flores surgen cuando mezclas concentradas de sales simples se vuelven lo bastante espesas como para ralentizarlo todo, pero no tanto como para que el crecimiento se detenga por completo. En estas condiciones “justas”, bolsillos líquidos densos y enjambres de pequeños cristales se autoensamblan en racimos esféricos que luego pueden evolucionar hacia granos más estables y facetados. Entender y controlar este delicado equilibrio entre composición, viscosidad y evaporación abre la puerta a diseñar texturas cristalinas a medida para aplicaciones que van desde materiales de construcción más resistentes y mejores farmacéuticos hasta modelos más precisos de la formación cristalina geológica y biológica.
Cita: Heeremans, T., Lépinay, S., Le Dizès Castell, R. et al. Controlled spherulitic crystal growth from salt mixtures. Commun Chem 9, 90 (2026). https://doi.org/10.1038/s42004-026-01892-0
Palabras clave: esferulitas, sulfato de sodio, crecimiento cristalino, nucleación no clásica, soluciones salinas